名校
1 . 钴酸锂电池的结构稳定、比容量高,但成本非常高,常用于小型电子设备中,负极材料是嵌入锂的石墨,可以表示为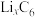 ,正极材料为
,正极材料为 ,放电时的工作原理如图所示(交换膜只允许
,放电时的工作原理如图所示(交换膜只允许 通过)。放电时,下列说法错误的是
通过)。放电时,下列说法错误的是
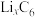 ,正极材料为
,正极材料为 ,放电时的工作原理如图所示(交换膜只允许
,放电时的工作原理如图所示(交换膜只允许 通过)。放电时,下列说法错误的是
通过)。放电时,下列说法错误的是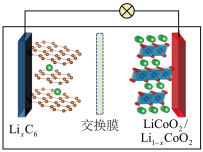
| A.主要将化学能转化为电能 |
B.正极材料中的 变为 变为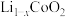 |
C. 经交换膜由左室进入右室 经交换膜由左室进入右室 |
| D.外电路中电流由正极流向负极,内电路中电流由负极流向正极 |
您最近半年使用:0次
名校
2 . 硫酸亚铁铵,俗名为莫尔盐[ ],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
 ],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
A.步骤Ⅱ到步骤Ⅲ的操作,缩短了溶液与空气接触的时间,降低 被氧化的风险 被氧化的风险 |
| B.玻璃棒缠绕铜丝的主要目的是铜丝和铁粉接触形成原电池,加快化学反应速率 |
C.步骤Ⅱ到步骤Ⅳ发生的反应方程式为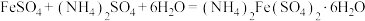 |
| D.从溶液中获得莫尔盐,可以直接经过蒸发结晶的实验操作获得纯净的莫尔盐 |
您最近半年使用:0次
2024-04-22更新
|
215次组卷
|
2卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题
3 . 根据实验目的设计方案,观察到相关现象,其中方案设计或结论正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究 的溶解平衡 的溶解平衡 | 将收集有 的试管倒立于水中 的试管倒立于水中 | 水进入试管占据试管容积四分之三 |  溶于水,达到溶解平衡 溶于水,达到溶解平衡 |
| B | 比较金属A和B的活动性强弱 | 将金属A、B分别与镁条、电压表连通后,插入稀硫酸中 |  与A连接时,电压表的示数更大 与A连接时,电压表的示数更大 | 金属活动性:A<B |
| C | 判断 的晶体类型 的晶体类型 | 将 晶体溶于水,测导电性 晶体溶于水,测导电性 |  溶液可导电 溶液可导电 |  晶体为离子晶体 晶体为离子晶体 |
| D | 探究 能否使蛋白质变性 能否使蛋白质变性 | 往装有鸡蛋清的试管中先加入少量 ,再加过量水,振荡 ,再加过量水,振荡 | 试管底部可见少量固体 |  能使蛋白质变性 能使蛋白质变性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-17更新
|
317次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
解题方法
4 . 资料显示,I2-KI溶液可以清洗银镜。某小组同学设计实验探究银镜在I2-KI溶液中的溶解情况。
已知:I2微溶于水,易溶于KI溶液,并发生反应I2+I− I
I (棕色),I2和I
(棕色),I2和I 氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
探究1:I2-KI溶液(向1mol·L−1KI溶液中加入I2至饱和)溶解银镜
【实验i】_____ 。
(2)能证明②中Ag已全部反应、未被包裹在黄色固体内的实验证据是_____ 。
探究2:I2-KI溶液能快速溶解银镜的原因
【实验ii~iv】向附着银镜的试管中加入相应试剂至浸没银镜,记录如下:
(3)ⅰi中,搅拌后银镜继续溶解的原因是_____ 。
(4)由i、iii可得到的结论是_____ 。
(5)设计iv的目的是_____ 。
探究3:I−的作用
【实验v】
说明:本实验中,检流计读数越大,说明氧化剂氧化性(或还原剂还原性)越强。
(6)步骤1接通电路后,正极的电极反应物为_____ 。
(7)补全步骤3的操作及现象:_____ ,_____ 。
(8)综合上述探究,从反应速率和物质性质的角度分析i中I2-KI溶液能快速全部溶解银镜的原因:_____ 。
已知:I2微溶于水,易溶于KI溶液,并发生反应I2+I−
 I
I (棕色),I2和I
(棕色),I2和I 氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。探究1:I2-KI溶液(向1mol·L−1KI溶液中加入I2至饱和)溶解银镜
【实验i】
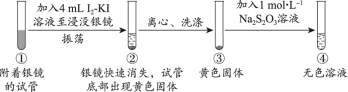
(2)能证明②中Ag已全部反应、未被包裹在黄色固体内的实验证据是
探究2:I2-KI溶液能快速溶解银镜的原因
【实验ii~iv】向附着银镜的试管中加入相应试剂至浸没银镜,记录如下:
| 序号 | 加入试剂 | 实验现象 |
| ⅰi | 4mL饱和碘水(向水中加入I2至饱和, | 30min后,银镜少部分溶解,溶液棕黄色变浅;放置24h后,与紫黑色固体接触部分银镜消失,紫黑色固体表面上有黄色固体,上层溶液接近无色;搅拌后,银镜继续溶解 |
| ⅱi | 4mL饱和碘水和0.66gKI固体(溶液中KI约1mol·L−1) | 15min后银镜部分溶解,溶液棕黄色变浅;放置24h后,试管壁上仍有未溶解的银镜,溶液无色 |
| iv | 4mL1mol·L−1KI溶液 | 放置24h,银镜不溶解,溶液无明显变化 |
(4)由i、iii可得到的结论是
(5)设计iv的目的是
探究3:I−的作用
【实验v】
| 实验装置 | 实验步骤及现象 |
| 1.按左图搭好装置,接通电路,检流计指针向 右微弱偏转,检流计读数为amA; 2.向石墨电极附近滴加饱和碘水,指针继续向 右偏转,检流计读数为bmA(b>a); 3.向左侧烧杯中加入_____,指针继续向右偏转,检流计读数cmA(c>b),有_____生成。 |
(6)步骤1接通电路后,正极的电极反应物为
(7)补全步骤3的操作及现象:
(8)综合上述探究,从反应速率和物质性质的角度分析i中I2-KI溶液能快速全部溶解银镜的原因:
您最近半年使用:0次
解题方法
5 . 资料显示,水溶液中 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。
实验记录如下:将 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。
(1) 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是___________ 。
(2)查阅资料得知,该白色沉淀是 。写出产生
。写出产生 的离子方程式:
的离子方程式:___________ 。
(3)甲同学认为:要证明 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,___________ (将操作和现象补充完整)。
(4)乙同学认为:溶液中存在 不一定是
不一定是 氧化的,体系中存在的
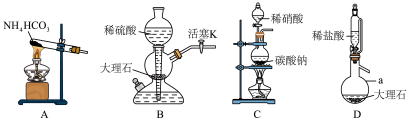
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是___________ (填字母),仪器a的名称是___________ 。
(5)丙同学认为: 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:___________ 。
(6)称取沉淀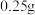 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈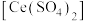 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
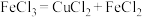 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是___________ ,沉淀中 的质量分数为
的质量分数为___________ 。
 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。实验记录如下:将
 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。(1)
 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是(2)查阅资料得知,该白色沉淀是
 。写出产生
。写出产生 的离子方程式:
的离子方程式:(3)甲同学认为:要证明
 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,(4)乙同学认为:溶液中存在
 不一定是
不一定是 氧化的,体系中存在的
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是
(5)丙同学认为:
 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:(6)称取沉淀
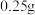 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈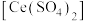 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
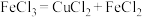 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是 的质量分数为
的质量分数为
您最近半年使用:0次
解题方法
6 . 一种钠离子电池的工作原理如图所示。充电过程中,磷酸钒钠[Na3V2(PO4)3]在外电压的作用下脱嵌部分Na+形成Na3-xV2(PO4)3,脱出的Na+进入电解液中,再传输到硬碳材料形成化合物NaxC。下列说法正确的是
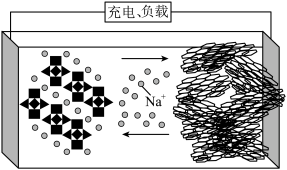

| A.充电时Na3V2(PO4)3为阴极 |
| B.充电时,电解液的质量增大 |
| C.放电时Na+由负极迁移到正极材料中 |
| D.放电时的正极反应为Na3V2(PO4)3-xe-=Na3-xV2(PO4)3+xNa+ |
您最近半年使用:0次
2024-03-16更新
|
38次组卷
|
2卷引用:陕西省安康市高新中学2023-2024学年高三12月月考理科综合试题
解题方法
7 . 我国科研工作者基于生物质平台分子糠醛开发出的一种“生物质电池”,在充、放电时分别得到高附加值的醇和羧酸盐,其工作原理如图所示。下列说法正确的是
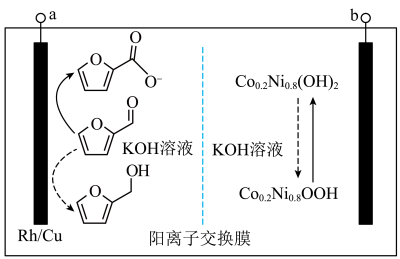

| A.充电时,a接电源正极 |
B.充电时, 由a极区移向b极区 由a极区移向b极区 |
C.放电时,消耗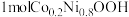 ,外电路转移1mol电子 ,外电路转移1mol电子 |
D.放电时,负极反应式为: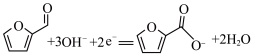 |
您最近半年使用:0次
2024-03-15更新
|
186次组卷
|
2卷引用:江西省赣州市2024届高三下学期3月摸底考试化学试题
名校
8 . 下列叙述正确的是
①当镀锡铁制品的镀层受损后,镀层仍能对铁制品起保护作用
②轮船上嵌入锌块来减缓轮船腐蚀的方法叫牺牲阳极法
③在铁制品上镀铜,铁制品为阴极,铜盐为电镀液
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
⑥锌与稀 反应时,加入少量
反应时,加入少量 溶液时,可以加快化学反应速率
溶液时,可以加快化学反应速率
①当镀锡铁制品的镀层受损后,镀层仍能对铁制品起保护作用
②轮船上嵌入锌块来减缓轮船腐蚀的方法叫牺牲阳极法
③在铁制品上镀铜,铁制品为阴极,铜盐为电镀液
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
⑥锌与稀
 反应时,加入少量
反应时,加入少量 溶液时,可以加快化学反应速率
溶液时,可以加快化学反应速率| A.3个 | B.4个 | C.5个 | D.全部 |
您最近半年使用:0次
名校
9 . 关于下列实验事实的给出的解释或结论不正确的是
| 选项 | 实验事实 | 解释或结论 |
| A. |  与 与 溶液反应产生黄色沉淀和气体( 溶液反应产生黄色沉淀和气体( ) ) | 反应生成难溶的 ,增大了 ,增大了 的还原性 的还原性 |
| B. | 将 气体通入 气体通入 溶液中,溶液先变为红棕色(含 溶液中,溶液先变为红棕色(含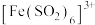 ),过一段时间又变成浅绿色 ),过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| C. | 取一定量固体于试管中,加入浓 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 | 该固体为铵盐 |
| D. | 将变黑的银器放入装满食盐水的铝盆中,一段时间后银器恢复往日光泽 | 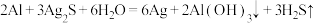 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 我国科学家设计的“海泥电池”工作原理如图所示,其中微生物代谢产物显酸性。下列说法正确的是
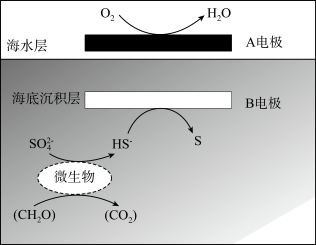

| A.电极A上发生氧化反应 |
| B.工作时,B电极附近pH变大 |
| C.质子从海水层通过交接面向海底沉积层移动 |
| D.微生物代谢反应中,氧化剂与还原剂的物质的量之比为1:2 |
您最近半年使用:0次




