名校
1 . 银铝电池具有能量密度高的优点,其工作原理如图所示,电池放电时的反应为2Al+3Ag2O+2NaOH+3H2O=2Na[Al(OH)4]+6Ag。
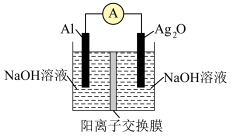
下列说法错误的是

下列说法错误的是
| A.Al为电源负极 | B.正极反应为Ag2O+2e-+H2O=2Ag+2OH- |
| C.放电时负极区pH增大 | D.放电时Na+通过交换膜向右侧移动 |
您最近一年使用:0次
2023-11-10更新
|
685次组卷
|
4卷引用:山西省晋城市第一中学校2023-2024学年高二上学期第五次调研考试化学试题
名校
2 . 锂离子电池具有比能量大,用途广等特点。如图为一种锂离子电池的结构示意图,电池反应式为
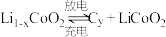 (x<1)。下列说法正确的是
(x<1)。下列说法正确的是
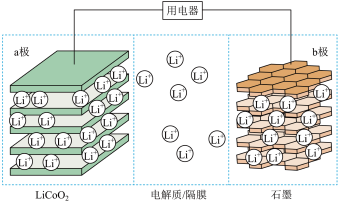

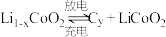 (x<1)。下列说法正确的是
(x<1)。下列说法正确的是
| A.充电时a极接外电源的负极 |
B.充电时,若转移1mol  ,石墨电极将增重7xg ,石墨电极将增重7xg |
C.放电时, 从石墨中脱嵌移向正极,嵌入钴酸锂晶体中 从石墨中脱嵌移向正极,嵌入钴酸锂晶体中 |
D.放电时, 极发生的电极反应为: 极发生的电极反应为: |
您最近一年使用:0次
2023-09-09更新
|
265次组卷
|
3卷引用:山西省运城市2023-2024学年高三上学期开学考试化学试题
名校
解题方法
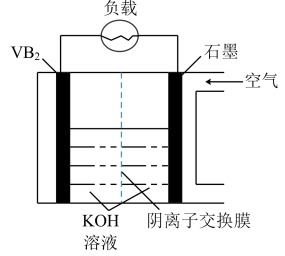
3 . 硼化钒( )一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为
)一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为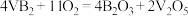 。下列说法正确的是
。下列说法正确的是
 )一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为
)一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为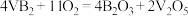 。下列说法正确的是
。下列说法正确的是
A. 电极为电池正极 电极为电池正极 |
B.电流由 极经KOH溶液流向石墨电极 极经KOH溶液流向石墨电极 |
C.当外电路转移1mol电子时,1 mol  从 从 电极移向石墨电极 电极移向石墨电极 |
D.电池工作过程中, 电极区电解质溶液浓度不变 电极区电解质溶液浓度不变 |
您最近一年使用:0次
2023-08-31更新
|
119次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期开学质量检测化学试题
名校
4 . 速率与限度是研究化学反应的重要视角,下列叙述错误的是
A.对于反应 ,其他条件不变,增加木炭的量,反应速率不变 ,其他条件不变,增加木炭的量,反应速率不变 |
| B.用锌片和稀硫酸反应制取氢气时,用粗锌比纯锌反应生成氢气的速率会加快 |
C.100 mL 2 mol·L 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
| D.在给定条件下,达到平衡时,可逆反应完成程度达到最大 |
您最近一年使用:0次
2023-05-06更新
|
292次组卷
|
2卷引用:山西省阳泉市2022-2023学年高一下学期期末考试化学试题
名校
5 . 利用反应 设计一个原电池,下列装置示意图正确的是
设计一个原电池,下列装置示意图正确的是
 设计一个原电池,下列装置示意图正确的是
设计一个原电池,下列装置示意图正确的是A.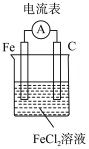 | B.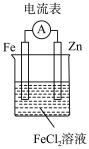 | C.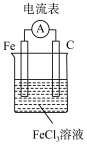 | D. |
您最近一年使用:0次
2023-05-01更新
|
450次组卷
|
3卷引用:山西省阳泉市2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . 锂-铜空气燃料电池容量高、成本低。该电池通过一种复杂的铜腐蚀“现象”产生电能,放电时发生反应: ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是
A.通空气时,铜被腐蚀,表面产生 |
B.放电时,正极的电极反应式为 |
C.当电路有 电子通过时,有 电子通过时,有 氧气参与反应 氧气参与反应 |
| D.将锂电极区有机电解质换成水溶液作电解质,可提高电池工作效率 |
您最近一年使用:0次
2023-04-24更新
|
196次组卷
|
2卷引用:山西省怀仁市第一中学2022-2023学年高一下学期6月月考化学试题
解题方法
7 . 硅是太阳能电池的重要材料。方法1是目前工业冶炼纯硅的一种原理:
粗硅冶炼:
①
精炼硅:
②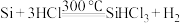
③
反应①过程中的能量变化如图所示,回答下列问题:
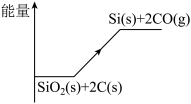
(1)①是________ 反应(填“吸热”或“放热”),结合图中信息说明判断依据__________ 。
(2)下列关于物质的性质与用途的说法均正确的是____________ 。(填字母)
A.石墨烯电阻率高,可用于制备动力电池
B.碳化硅硬度很大,用作砂纸和砂轮的磨料
C.硅单质是应用最广泛的半导体材料,其导电性介于导体和绝缘体之间
(3)工业上也曾用方法2来提纯单晶硅: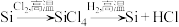 ,与方法1相比,方法2的缺点是
,与方法1相比,方法2的缺点是__________________________ 。
(4)某同学在用稀硫酸与锌制取氢气的实验中,意外地发现滴加几滴 溶液后反应速率加快了,原因可能是
溶液后反应速率加快了,原因可能是____________ 。(填字母)
a. 是催化剂 b.Zn、
是催化剂 b.Zn、 、
、 构成原电池
构成原电池
c.Zn、Cu、 构成原电池 d.上述分析均不正确
构成原电池 d.上述分析均不正确
粗硅冶炼:
①

精炼硅:
②
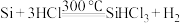
③

反应①过程中的能量变化如图所示,回答下列问题:

(1)①是
(2)下列关于物质的性质与用途的说法均正确的是
A.石墨烯电阻率高,可用于制备动力电池
B.碳化硅硬度很大,用作砂纸和砂轮的磨料
C.硅单质是应用最广泛的半导体材料,其导电性介于导体和绝缘体之间
(3)工业上也曾用方法2来提纯单晶硅:
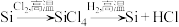 ,与方法1相比,方法2的缺点是
,与方法1相比,方法2的缺点是(4)某同学在用稀硫酸与锌制取氢气的实验中,意外地发现滴加几滴
 溶液后反应速率加快了,原因可能是
溶液后反应速率加快了,原因可能是a.
 是催化剂 b.Zn、
是催化剂 b.Zn、 、
、 构成原电池
构成原电池c.Zn、Cu、
 构成原电池 d.上述分析均不正确
构成原电池 d.上述分析均不正确
您最近一年使用:0次
解题方法
8 .  的资源化利用能有效减少
的资源化利用能有效减少 的排放,充分利用碳资源。回答下列问题:
的排放,充分利用碳资源。回答下列问题:
Ⅰ.把 转化为HCOOH是降碳并生产化工原料的常用方法。工业上利用甲酸的能量关系转换图如图所示:
转化为HCOOH是降碳并生产化工原料的常用方法。工业上利用甲酸的能量关系转换图如图所示:

(1)反应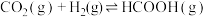 的
的
_______ 。
(2)在恒温恒容密闭容器中,对于 转化为HCOOH的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母)。
转化为HCOOH的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母)。
(3)温度为 ℃时,在初始总压为
℃时,在初始总压为 kPa的2 L恒容密闭容器中分别充入1 mol
kPa的2 L恒容密闭容器中分别充入1 mol  和1 mol
和1 mol  发生反应:
发生反应: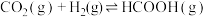 ,体系达到平衡时容器内总压强变为原来的0.75倍。
,体系达到平衡时容器内总压强变为原来的0.75倍。 ℃时,
℃时, 的平衡转化率为
的平衡转化率为_______ ;上述反应的化学平衡常数
_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。若其他条件不变,将上述起始反应物置于某恒压密闭容器中,则 的平衡转化率
的平衡转化率_______ (填“增大”“减小”或“不变”)。
Ⅱ.下图是某科研团队设计的光电催化反应器,实现了由 制得异丙醇(常温下为液态)。其中A极是Pt/CNT电极,B极是Pt/CNT电极。
制得异丙醇(常温下为液态)。其中A极是Pt/CNT电极,B极是Pt/CNT电极。

(4)A极为_______ 极(填“正”或“负”),其电极反应式为_______ 。
(5)离子交换膜是_______ (填“阴”或“阳”)离子交换膜。
(6)该反应器工作一段时间,若A、B两极分别收集到标准状况下1.12 L和2.24 L的气体,则此时理论上制得异丙醇的质量为_______ g(保留1位小数)。
 的资源化利用能有效减少
的资源化利用能有效减少 的排放,充分利用碳资源。回答下列问题:
的排放,充分利用碳资源。回答下列问题:Ⅰ.把
 转化为HCOOH是降碳并生产化工原料的常用方法。工业上利用甲酸的能量关系转换图如图所示:
转化为HCOOH是降碳并生产化工原料的常用方法。工业上利用甲酸的能量关系转换图如图所示:
(1)反应
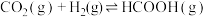 的
的
(2)在恒温恒容密闭容器中,对于
 转化为HCOOH的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母)。
转化为HCOOH的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母)。| A.混合气体的平均相对分子质量不再变化 |
| B.混合气体的密度不再变化 |
C. 和 和 的转化率之比不再变化 的转化率之比不再变化 |
D.生成HCOOH的速率与消耗 的速率相等 的速率相等 |
 ℃时,在初始总压为
℃时,在初始总压为 kPa的2 L恒容密闭容器中分别充入1 mol
kPa的2 L恒容密闭容器中分别充入1 mol  和1 mol
和1 mol  发生反应:
发生反应: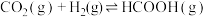 ,体系达到平衡时容器内总压强变为原来的0.75倍。
,体系达到平衡时容器内总压强变为原来的0.75倍。 ℃时,
℃时, 的平衡转化率为
的平衡转化率为
 的平衡转化率
的平衡转化率Ⅱ.下图是某科研团队设计的光电催化反应器,实现了由
 制得异丙醇(常温下为液态)。其中A极是Pt/CNT电极,B极是Pt/CNT电极。
制得异丙醇(常温下为液态)。其中A极是Pt/CNT电极,B极是Pt/CNT电极。
(4)A极为
(5)离子交换膜是
(6)该反应器工作一段时间,若A、B两极分别收集到标准状况下1.12 L和2.24 L的气体,则此时理论上制得异丙醇的质量为
您最近一年使用:0次
9 . 锌-空气电池可用作电动车的动力电源。其工作原理如图所示。下列说法中错误的是


| A.隔膜应为阳离子交换膜,允许K+通过 |
| B.放电时,电解质溶液中c(OH-)逐渐减小 |
| C.放电时,负极反应为Zn+4OH--2e-=[Zn(OH)4]2- |
| D.多孔炭可增大电极与电解质溶液的接触面积,也有利于O2扩散至电极表面 |
您最近一年使用:0次
10 . 下列叙述中错误的是
| A.生铁比纯铁易生锈 |
| B.放电时,铅酸蓄电池中硫酸浓度不断变小 |
| C.铁制品上镀铜时,铁制品为阳极,铜盐为电镀液 |
| D.外加电流法保护钢铁设备时,用惰性电极作为辅助阳极 |
您最近一年使用:0次



