名校
1 . 如图所示,A为电源,B为浸透饱和食盐水和酚酞的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
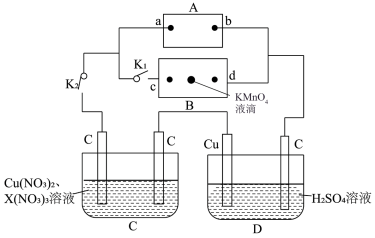
(1)闭合K1 ,断开K2 ,通电后,d端显红色,则电源a端为______ 极,若c、d为惰性电极,c端的电极反应是____________________________________
检验c端产物的方法_______________________________________________
高锰酸钾液滴现象__________________________________________________
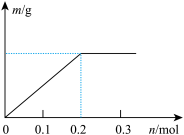
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3 ,且均为0.1 mol,断开K1,闭合K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+ 氧化能力由大到小的顺序是_______ ;
(3)D装置中反应的方程式___________________________

(1)闭合K1 ,断开K2 ,通电后,d端显红色,则电源a端为
检验c端产物的方法
高锰酸钾液滴现象
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3 ,且均为0.1 mol,断开K1,闭合K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+ 氧化能力由大到小的顺序是

(3)D装置中反应的方程式
您最近一年使用:0次
2019-11-25更新
|
326次组卷
|
2卷引用:贵州省思南中学2019-2020学年高二上学期期末考试化学试题
名校
解题方法
2 . 下列关于如图所示电化学装置的分析正确的是
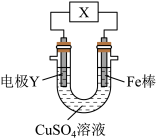

| A.若X为直流电源,Y为铜棒接正极,则Fe棒上有铜析出 |
| B.若X为直流电源,Y为碳棒接负极,则Fe棒被保护 |
C.若X为电流计,Y为锌棒,则 移向Fe棒 移向Fe棒 |
| D.若X为导线,Y为铜棒,则Fe棒发生还原反应 |
您最近一年使用:0次
2020-02-14更新
|
186次组卷
|
10卷引用:2017届贵州省凯里一中高三上第四次模拟化学试卷
3 . 一种新型动力电池( LiFePO4电池)总反应式为Li1-xFePO4+LixC6 C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
 C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是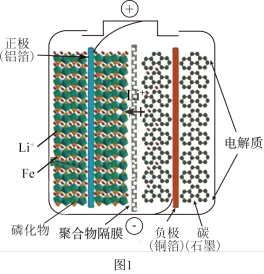
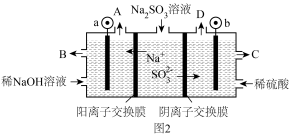
| A.电池放电时,LixC6在负极发生氧化反应 |
| B.电池放电时,正极反应式为 Lil-xFePO4+xLi-+xe-= LiFePO4 |
| C.电解时,图2的b电极反应式为2H2O-4e-=O2↑+4H+ |
| D.电解时,当转移0.2mol电子,A口产生气体的质量1.6g |
您最近一年使用:0次
2019-04-19更新
|
1857次组卷
|
3卷引用:【市级联考】贵州省毕节市2019届高三适应性监测考试(三)理科综合化学试题
13-14高三·全国·课后作业
名校
解题方法
4 . 已知铅酸蓄电池的工作原理为Pb+PbO2+2H2SO4 2PbSO4+2H2O。现用如图装置进行电解实验,测得当铅酸蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
2PbSO4+2H2O。现用如图装置进行电解实验,测得当铅酸蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:___ 极,铅酸蓄电池正极的电极反应式为__ ,放电过程中电解液的密度(忽略电解液的体积变化)__ (填“减小”“增大”或“不变”)。
(2)Ag电极的电极反应式是__ ,该电极的电极产物有__ g。
(3)Cu电极的电极反应式是__ ,CuSO4溶液的浓度__ (填“减小”“增大”或“不变”)。
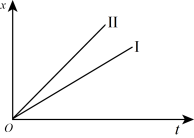
(4)如图表示电解进行过程中某个物理量x随时间t的变化曲线,其中曲线Ⅰ表示左侧U形管中的变化,曲线Ⅱ表示右侧U形管中的变化,则x表示__ (填序号)。
b.U形管中阳极质量的减少量
c.U形管中阴极质量的增加量
 2PbSO4+2H2O。现用如图装置进行电解实验,测得当铅酸蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
2PbSO4+2H2O。现用如图装置进行电解实验,测得当铅酸蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
(2)Ag电极的电极反应式是
(3)Cu电极的电极反应式是
(4)如图表示电解进行过程中某个物理量x随时间t的变化曲线,其中曲线Ⅰ表示左侧U形管中的变化,曲线Ⅱ表示右侧U形管中的变化,则x表示
b.U形管中阳极质量的减少量
c.U形管中阴极质量的增加量
您最近一年使用:0次
2020-10-13更新
|
236次组卷
|
11卷引用:贵州省余庆中学2019-2020学年上学期开学考试高三化学试题
贵州省余庆中学2019-2020学年上学期开学考试高三化学试题贵州省荔波高级中学2019-2020学年高三上学期期末考试理综化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题贵州省望黔西南布依族苗族自治州谟民族中学2019-2020学年高三上学期期末考试化学试题(已下线)2014年化学高考总复习课时演练9-2电解池金属电化学腐蚀与防护练习卷2015-2016学年内蒙古奋斗中学高二上9月质检化学试卷2015-2016学年河南省南阳部分高中高二上学期第一次联考化学试卷河南省郑州市中牟县二中2017-2018学年高二第一次月考化学试题宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用
10-11高二·山东济南·阶段练习
名校
解题方法
5 . 关于铅蓄电池的说法正确的是( )
| A.在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-=PbSO4(s) |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是PbSO4(s)+2e-=Pb(s)+SO42- (aq) |
您最近一年使用:0次
2020-02-19更新
|
923次组卷
|
32卷引用:贵州省黔东南苗族侗族自治州天柱县第二中学2019-2020学年高二上学期期末考试化学试题
贵州省黔东南苗族侗族自治州天柱县第二中学2019-2020学年高二上学期期末考试化学试题(已下线)2010—2011学年山东省济南外国语学校高二入学检测化学试卷(已下线)2010-2011年江苏省扬州中学高一下学期期末考试化学试卷(已下线)2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷(已下线)2011-2012学年山东省潍坊市三县高二上学期模块学分认定检测化学试卷(已下线)2012届安徽省淮北一中高三第三次月考化学试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2012-2013学年辽宁省实验中学分校高二12月月考化学试卷(已下线)2014届高考化学三轮复习排查 专题8电化学基础练习卷2016届湖南省衡阳市第八中学高三上学期第一次月考化学试卷2015-2016学年河北省故城高级中学高二上12月月考化学试卷2015-2016学年海南文昌中学高一下期末考化学(理)试题2016-2017学年陕西西藏民族学院附中高二上月考二化学卷2017届宁夏石嘴山三中高三上期中化学试卷2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷2015-2016学年青海省西宁市第五中学高一下学期期末(理)化学试卷(已下线)4.2 化学电源高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源山东省新汶中学2017-2018学年高二上学期第一次月考化学试题河北省衡水中学滁州分校2017-2018学年高一下学期第一次月考化学试题安徽省滁州市定远县民族中学2017-2018学年高一下学期期末考试化学试题陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题(已下线)2018年11月27日 《每日一题》人教选修4 - 二次电池的工作原理甘肃省武威市第十八中学2018-2019学年高二上学期期末考试化学试题陕西省黄陵中学2018-2019学年高二上学期期末考试化学试题云南省马关一中2018-2019学年高二下学期期末考试化学试题人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 教材帮宁夏银川市宁夏大学附属中学2021届高三上学期第一次月考化学试题黑龙江省哈尔滨工业大学附属中学2022-2023学年高一下学期期末考试化学试题天津市天津中学2022-2023学年高二上学期线上期末考试化学试题安徽省蚌埠市田家炳中学、五中2019-2020学年高二上学期期中考试化学试题上海南汇中学 2023-2024学年第一学期高二化学(等级)期末考试试卷
名校
6 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池为__________ (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为___________________________ 。
(2)丙池中F电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),F电极的电极反应式为_________________________________ 。该池总反应的化学方程式为___________________________ 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_____ mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___ (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3

(1)甲池为
(2)丙池中F电极为
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
您最近一年使用:0次
7 . 一种正投入生产的大型蓄电系统如图所示。放电前,被交换膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述不正确的是
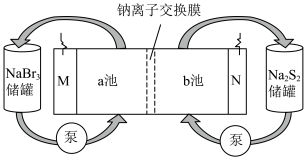

| A.放电时,负极的电极反应式为2S22――2e-===S42- |
| B.充电时,阳极的电极反应式为3Br--2e-===Br3- |
| C.放电时,Na+经过离子交换膜,由b池移向a池 |
| D.充电时,M接电源负极,N接电源正极 |
您最近一年使用:0次
2019-03-11更新
|
511次组卷
|
2卷引用:【市级联考】贵州省黔东南州2019届高三下学期第一次模拟考试理科综合化学试题
名校
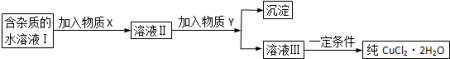
8 . (1)现用氯化铜晶体(CuCl2·2H2O,含少量FeCl2杂质)制取纯净的CuCl2·2H2O,先将其制成水溶液,后按如图步骤进行提纯:
已知:相关物质的溶度积常数见下表:
请回答下列问题:
①请从下列物质中选出第一步中需加入的X( )
a.NaClO b.H2O2 c.KMnO4 d.HNO3
②溶液Ⅱ中含有少量的Fe3+,如何检验该离子的存在:_____________________________ 。
③若此时溶液中的c(Cu2+)=0.02mol/L,为得到纯净的CuCl2·2H2O晶体,可加入CuO固体,使溶液中的Fe3+完全转化为Fe(OH)3沉淀且不沉淀Cu2+,调节pH的范围是_______ 。(通常认为残留在溶液中的离子浓度小于或等于1×10ˉ5 mol/L时就认为沉淀完全)。
④由溶液Ⅲ得到CuCl2·2H2O晶体的操作是___________________________________ 。
(2)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiO(OH)+H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
回答下列问题:
①放电时,金属Cd作_______ 极;
②充电时的阳极电极反应式为_____________________________________________ 。
③充电时,当电路中通过0.2moleˉ,阴极质量将_______ (填“增加”、“减少”)___ g。

已知:相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| Ksp | 2.0×10ˉ20 | 1.0×10ˉ38 | 1.64×10ˉ14 |
请回答下列问题:
①请从下列物质中选出第一步中需加入的X
a.NaClO b.H2O2 c.KMnO4 d.HNO3
②溶液Ⅱ中含有少量的Fe3+,如何检验该离子的存在:
③若此时溶液中的c(Cu2+)=0.02mol/L,为得到纯净的CuCl2·2H2O晶体,可加入CuO固体,使溶液中的Fe3+完全转化为Fe(OH)3沉淀且不沉淀Cu2+,调节pH的范围是
④由溶液Ⅲ得到CuCl2·2H2O晶体的操作是
(2)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiO(OH)+H2O
 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2回答下列问题:
①放电时,金属Cd作
②充电时的阳极电极反应式为
③充电时,当电路中通过0.2moleˉ,阴极质量将
您最近一年使用:0次
名校
9 . 某化学学习小组学习电化学后,设计了以甲、乙两池作原电池的实验装置。下列说法正确的是
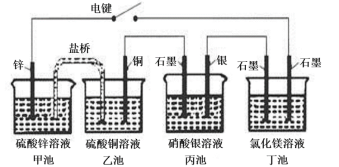

| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后一段时间,丙池中溶液的pH增大 |
| C.合上电键后,丁池中有金属镁析出 |
| D.合上电键后,甲池中锌电极为原电池负极 |
您最近一年使用:0次
2019-01-24更新
|
347次组卷
|
2卷引用:【全国百强校】贵州省都匀市都匀第一中学2018-2019学年高二上学期期末考试化学试题
10 . 某实验小组用石墨作电极进行如下实验,实验观察到:a、d处试纸变蓝;b处变红,并局部褪色:c处无明显变化。下列说法中错误的是
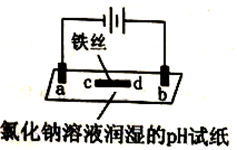

| A.a极为阴极,发生的电极反应为:2H++2e-=H2↑ |
B.b极为阳极,涉及的反应有:2Cl--2e-=C12↑、Cl2+H2O HCl+HClO HCl+HClO |
| C.电解过程中,电子流向:电源负极→a→c→d→b→电源正极 |
| D.若将铁丝改成铜丝,其余条件相同,电解一段时间后,能发现c处附近变蓝 |
您最近一年使用:0次
2019-01-24更新
|
132次组卷
|
2卷引用:【校级联考】贵州省部分重点中学2019届高三上学期高考教学质量评测(四)(期末)理科综合化学试题



