1 . 为了实现“碳中和”,研发 的利用技术成为热点。
的利用技术成为热点。
反应I:
反应Ⅱ:
请回答:
(1)反应I能够自发进行的条件是__________ 。
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入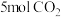 和
和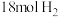 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
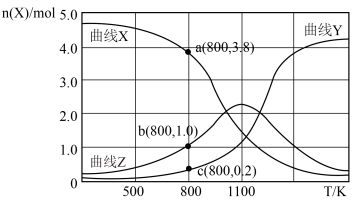
①写出曲线Y表示的含碳元素物质的化学式__________ 。
② 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
__________ [对于气相反应,用某组分 的平衡压强
的平衡压强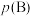 代替物质的量浓度
代替物质的量浓度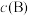 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如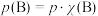 ,
, 为平衡总压强,
为平衡总压强,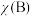 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: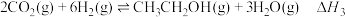 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示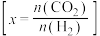 :
:

①上述反应的活化能 (正)
(正)__________  (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② 、
、 、
、 由大到小的顺序是
由大到小的顺序是__________ 。
③从平衡角度分析,随温度升高,不同投料比时 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因__________ 。
(4)科学家提出由 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为__________ 。

(5)水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:

①放电时复合膜中向 极移动的离子是
极移动的离子是__________ 。
②充电时多孔 纳米片电极的电极反应式为
纳米片电极的电极反应式为__________ 。
 的利用技术成为热点。
的利用技术成为热点。反应I:

反应Ⅱ:

请回答:
(1)反应I能够自发进行的条件是
(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入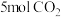 和
和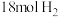 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
①写出曲线Y表示的含碳元素物质的化学式
②
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
 的平衡压强
的平衡压强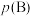 代替物质的量浓度
代替物质的量浓度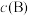 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如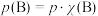 ,
, 为平衡总压强,
为平衡总压强,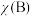 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: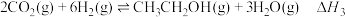 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示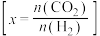 :
:
①上述反应的活化能
 (正)
(正) (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③从平衡角度分析,随温度升高,不同投料比时
 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因(4)科学家提出由
 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为
(5)水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
①放电时复合膜中向
 极移动的离子是
极移动的离子是②充电时多孔
 纳米片电极的电极反应式为
纳米片电极的电极反应式为
您最近半年使用:0次
2 . 电化学在化工、冶金、机械、电子、航空、航天、轻工、仪表、医学、材料、能源、金属腐蚀与防护、环境科学等科技领域获得了广泛的应用。
Ⅰ.电解精炼镓的装置如图所示,粗镓含 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为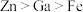 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
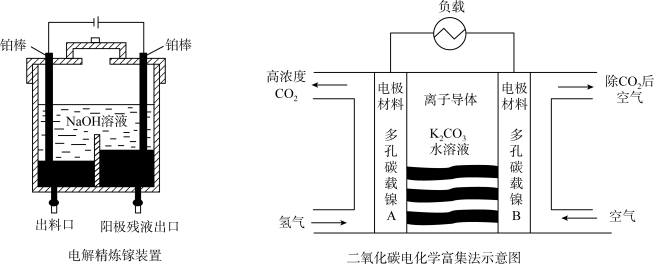
(1)电解后,电解槽底部阳极泥中所含的金属有_____ 。
(2)电解过程中阴极的电极反应式是_____ 。
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中, 向多孔碳载镍
向多孔碳载镍_____ (填“A”或“B”)电极移动。
(4)负极的电极反应式是_____ 。
(5)在多孔碳载镍A电极上消耗1
 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是_____ L。
Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。
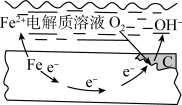
(6)钢铁吸氧腐蚀的正极反应式是_____ 。
(7)下列关于金属腐蚀的防护说法正确的是_____ 。
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
Ⅰ.电解精炼镓的装置如图所示,粗镓含
 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为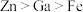 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
(1)电解后,电解槽底部阳极泥中所含的金属有
(2)电解过程中阴极的电极反应式是
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中,
 向多孔碳载镍
向多孔碳载镍(4)负极的电极反应式是
(5)在多孔碳载镍A电极上消耗1

 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。

(6)钢铁吸氧腐蚀的正极反应式是
(7)下列关于金属腐蚀的防护说法正确的是
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
您最近半年使用:0次
名校
解题方法
3 . 下列装置可分离废水中的Co2+和Ni2+。已知Ni2+和Co2+性质相似,Co2+和乙酰丙酮不反应。下列说法正确的是

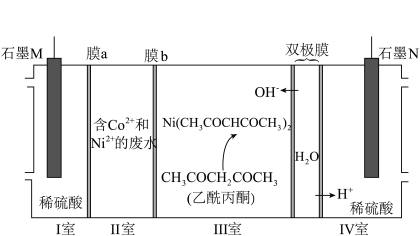


| A.M电极接太阳能电池的P电极 |
| B.通电一段时间后,I、IV室内溶液pH均减小 |
| C.膜a、膜b分别为阳离子交换膜和阴离子交换膜 |
D.每生成1molSO ,理论上双极膜至少解离7molH2O ,理论上双极膜至少解离7molH2O |
您最近半年使用:0次
2023-03-03更新
|
1379次组卷
|
3卷引用:山东省淄博市2022-2023学年高三第一次模拟考试化学试题
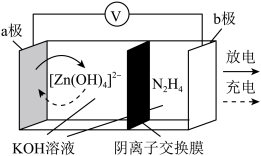
4 . 科学家近日发明了一种无污染、无需净化高效产氢的可充电电池,电池示意图如下。电极为金属锌和选择性催化材料,实现了阴极析氢和 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
A.充电时,阴极区溶液 减小 减小 |
B.放电时, 由b极区向a极区迁移 由b极区向a极区迁移 |
| C.充电时,b极反应式为N2H4-4e-+4OH-=N2+4H2O |
D.产生 ,a极质量增大 ,a极质量增大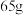 |
您最近半年使用:0次
5 . 各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:______ ;
②充电时,电源正极与______ (填“Pb”或“ ”)连接,溶液的pH会
”)连接,溶液的pH会______ (填“增大”、“减小”或“不变”)。
(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。
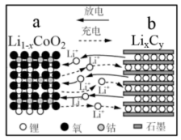
总反应式为:
①放电时,电极b是______ 极,a电极反应式为______ ;
②充电时,当导线中通过2mol 时,阴极的固体质量增加
时,阴极的固体质量增加______ g。
③与传统的铅蓄电池相比,锂电池具有的优点有:______ (一点即可)。
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
①a处通入的气体是______ ;
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为______ 。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:
②充电时,电源正极与
 ”)连接,溶液的pH会
”)连接,溶液的pH会(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。

总反应式为:

①放电时,电极b是
②充电时,当导线中通过2mol
 时,阴极的固体质量增加
时,阴极的固体质量增加③与传统的铅蓄电池相比,锂电池具有的优点有:
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:

①a处通入的气体是
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为
您最近半年使用:0次
名校
6 . 利用膜技术可以实现含苯酚废水的无害化处理和海水(含 等)淡化,装置如图所示。下列说法错误的是
等)淡化,装置如图所示。下列说法错误的是

 等)淡化,装置如图所示。下列说法错误的是
等)淡化,装置如图所示。下列说法错误的是
| A.Y膜为阳离子交换膜 |
| B.产生水垢最多的是甲室 |
| C.淡水的出口为c |
D.电池负极的电极反应为: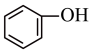  |
您最近半年使用:0次
2022-11-09更新
|
543次组卷
|
4卷引用:山东省潍坊市2022-2023学年高三上学期期中考试化学考试题
7 . 利用如图装置(电极材料均为石墨,右侧装置为原电池)从废旧锂离子电池正极材料 中回收金属钴。工作时借助细菌降解乙酸盐生成
中回收金属钴。工作时借助细菌降解乙酸盐生成 ,将
,将 转化为
转化为 ,并定时将乙室溶液转移至甲室。下列说法不正确的是
,并定时将乙室溶液转移至甲室。下列说法不正确的是

 中回收金属钴。工作时借助细菌降解乙酸盐生成
中回收金属钴。工作时借助细菌降解乙酸盐生成 ,将
,将 转化为
转化为 ,并定时将乙室溶液转移至甲室。下列说法不正确的是
,并定时将乙室溶液转移至甲室。下列说法不正确的是
| A.b电极为电解池的阴极,d电极为原电池的正极 |
B.c电极反应式为 |
| C.为保持细菌所在环境pH稳定,两池均应选择阳离子交换膜 |
D.若甲室 减少100mg,乙室 减少100mg,乙室 增加150mg,则此时还未进行过溶液转移 增加150mg,则此时还未进行过溶液转移 |
您最近半年使用:0次
8 . 通过电解 、
、 的混合溶液得到普通干电池中的锌与
的混合溶液得到普通干电池中的锌与 ,某研究小组设计了如下图所示的实验探究装置。
,某研究小组设计了如下图所示的实验探究装置。
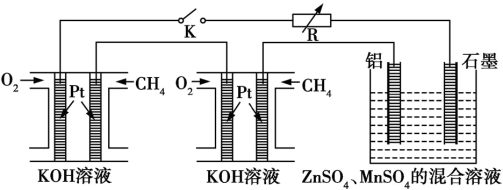
回答下列问题:
(1)燃料电池的优点是_______ ,图中是将两个甲烷燃料电池串联后作为电源,负极的电极反应为_______ 。
(2)闭合开关 后,铝电极上的产物是
后,铝电极上的产物是_______ ,一段时间后阳极附近溶液的pH_______ (填“增大”、“不变”或“减小”),电解 、
、 的混合溶液的阳极反应式为
的混合溶液的阳极反应式为_______
(3)假定燃料电池中的化学能完全转化为电能,负极每消耗2.24L(标况) ,电解池中回收制得
,电解池中回收制得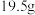 单质
单质 ,电解池的能量利用率为
,电解池的能量利用率为_______ 。
 、
、 的混合溶液得到普通干电池中的锌与
的混合溶液得到普通干电池中的锌与 ,某研究小组设计了如下图所示的实验探究装置。
,某研究小组设计了如下图所示的实验探究装置。
回答下列问题:
(1)燃料电池的优点是
(2)闭合开关
 后,铝电极上的产物是
后,铝电极上的产物是 、
、 的混合溶液的阳极反应式为
的混合溶液的阳极反应式为(3)假定燃料电池中的化学能完全转化为电能,负极每消耗2.24L(标况)
 ,电解池中回收制得
,电解池中回收制得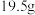 单质
单质 ,电解池的能量利用率为
,电解池的能量利用率为
您最近半年使用:0次
名校
解题方法
9 . 铁-铬液流电池的装置如下图所示,下列说法错误的是


A.放电时, 通过质子交换膜向Y电极移动 通过质子交换膜向Y电极移动 |
B.通过该原电池反应可知氧化性: |
C.充电时,X电极的电极反应式为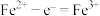 |
| D.充电完成后,可将电解质溶液泵回储液罐,将能量储存起来 |
您最近半年使用:0次
2022-09-03更新
|
190次组卷
|
2卷引用:山东省日照市2022-2023学年高二上学期8月校际联考化学试题
解题方法
10 . 铜基配合物电催化还原CO2的装置原理如图所示,下列说法不正确的是
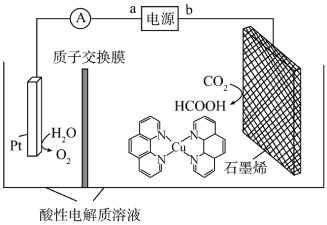
| A.石墨烯为阳极,发生电极反应为CO2+2e-+2H+=HCOOH |
| B.Pt电极附近溶液的pH值减小 |
| C.每转移2mol电子,阳极室、阴极室溶液质量变化量的差值为28g |
| D.该装置可减少CO2在大气中累积和实现可再生能源有效利用 |
您最近半年使用:0次



