1 . 过渡元素锰能形成很多重要的化合物。回答下列问题:
(1)三醋酸锰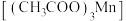 是一种有机反应氧化剂。Mn在元素周期表中的位置为
是一种有机反应氧化剂。Mn在元素周期表中的位置为___________ 。下列表示锰原子处于激发态的有___________ (填标号,下同),其中能量较高的是___________ 。
a.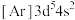 b.
b.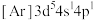 c.
c.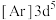 d.
d.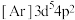
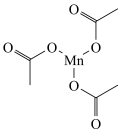
(2)三醋酸锰是一种配合物,其结构如图所示,所含 键和
键和 键个数之比为
键个数之比为___________ 。羧酸可表示为A―H, 、
、 和
和 酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是___________ 。
(3)锰酸锂( )可作为锂离子电池的正极材料,通过
)可作为锂离子电池的正极材料,通过 嵌入或脱嵌实现充放电。
嵌入或脱嵌实现充放电。
①锰酸锂可充电电池的总反应为: 。
。 从锰酸锂中脱嵌的过程为
从锰酸锂中脱嵌的过程为___________ 。(填“放电”或“充电”)过程,对应的电极反应式为___________ 。
② 晶胞可看成由图1中A、B单元按图2方式构成。图1中“
晶胞可看成由图1中A、B单元按图2方式构成。图1中“ ”表示
”表示 ,则“
,则“ ”表示的微粒是
”表示的微粒是___________ 。(填离子符号)。

(1)三醋酸锰
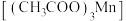 是一种有机反应氧化剂。Mn在元素周期表中的位置为
是一种有机反应氧化剂。Mn在元素周期表中的位置为a.
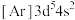 b.
b.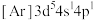 c.
c.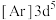 d.
d.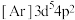
(2)三醋酸锰是一种配合物,其结构如图所示,所含
 键和
键和 键个数之比为
键个数之比为 、
、 和
和 酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
(3)锰酸锂(
 )可作为锂离子电池的正极材料,通过
)可作为锂离子电池的正极材料,通过 嵌入或脱嵌实现充放电。
嵌入或脱嵌实现充放电。①锰酸锂可充电电池的总反应为:
 。
。 从锰酸锂中脱嵌的过程为
从锰酸锂中脱嵌的过程为②
 晶胞可看成由图1中A、B单元按图2方式构成。图1中“
晶胞可看成由图1中A、B单元按图2方式构成。图1中“ ”表示
”表示 ,则“
,则“ ”表示的微粒是
”表示的微粒是
您最近一年使用:0次
解题方法
2 . 中国科学家将I2分子引入电解质中制作高功率可充电Li-SOCl2电池,I2调整充电和放电反应途径如图所示。下列说法错误的是
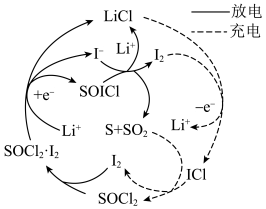

| A.电池使用过程中无需补充I2 |
| B.充电时,阴极Li+得电子发生还原反应 |
| C.放电时总反应:4Li+2SOCl2=4LiCl+S+SO2↑ |
| D.充电时,Li电极质量增加7 g时电极反应消耗的I2的质量为254 g |
您最近一年使用:0次
解题方法
3 . 某种新型可充电电池具有较高的循环使用寿命,工作原理如图所示。下列说法错误的是


| A.放电时,A极为正极 |
B.放电过程中转移1mol ,正极质量增加14g ,正极质量增加14g |
C.充电时B极电极反应式为 |
D.充电过程中转移0.5mol ,理论上有0.5molKOH被消耗 ,理论上有0.5molKOH被消耗 |
您最近一年使用:0次
4 .  是新能源汽车的动力电池之一,一种以锂磷矿石[
是新能源汽车的动力电池之一,一种以锂磷矿石[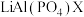 (
(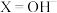 或
或 ),含
),含 、
、 、
、 、
、 、
、 等杂质]来制备
等杂质]来制备 的工艺流程如下:
的工艺流程如下:
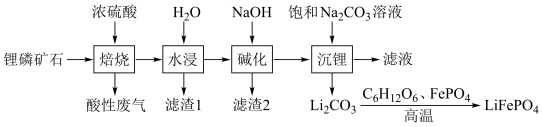
已知:一些难溶物质的溶度积常数如下表:
回答下列问题:
(1)“酸性废气”为___________ (填化学式),“滤渣1”的主要成分为 、磷酸盐及
、磷酸盐及___________ (填化学式)。
(2)“碱化”时,当 时,调节
时,调节 为11,此时
为11,此时
___________  。
。
(3)“碱化”时,逐滴加入 溶液,若
溶液,若 、
、 、
、 浓度相近,则析出的顺序依次为
浓度相近,则析出的顺序依次为___________ (填元素符号)。
(4)“沉锂”时,所得“滤液”的成分为___________ (填化学式)。
(5)在高温条件下,由 制备
制备 时同时生成
时同时生成 和
和 ,该反应的化学方程式为:
,该反应的化学方程式为:___________ 。
(6)一种新型的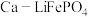 可充电电池的工作示意图如图所示,其中锂离子导体膜只允许
可充电电池的工作示意图如图所示,其中锂离子导体膜只允许 通过。放电时正极的电极反应式为:
通过。放电时正极的电极反应式为:___________ ;充电时,每转移 电子,左室中电解质的质量减轻
电子,左室中电解质的质量减轻___________  。
。
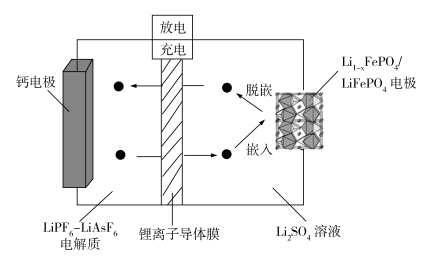
 是新能源汽车的动力电池之一,一种以锂磷矿石[
是新能源汽车的动力电池之一,一种以锂磷矿石[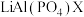 (
(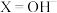 或
或 ),含
),含 、
、 、
、 、
、 、
、 等杂质]来制备
等杂质]来制备 的工艺流程如下:
的工艺流程如下:
已知:一些难溶物质的溶度积常数如下表:
| 物质 |  |  |  |  |
 | 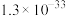 | 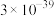 | 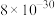 | 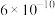 |
(1)“酸性废气”为
 、磷酸盐及
、磷酸盐及(2)“碱化”时,当
 时,调节
时,调节 为11,此时
为11,此时
 。
。(3)“碱化”时,逐滴加入
 溶液,若
溶液,若 、
、 、
、 浓度相近,则析出的顺序依次为
浓度相近,则析出的顺序依次为(4)“沉锂”时,所得“滤液”的成分为
(5)在高温条件下,由
 制备
制备 时同时生成
时同时生成 和
和 ,该反应的化学方程式为:
,该反应的化学方程式为:(6)一种新型的
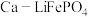 可充电电池的工作示意图如图所示,其中锂离子导体膜只允许
可充电电池的工作示意图如图所示,其中锂离子导体膜只允许 通过。放电时正极的电极反应式为:
通过。放电时正极的电极反应式为: 电子,左室中电解质的质量减轻
电子,左室中电解质的质量减轻 。
。
您最近一年使用:0次
2024-02-02更新
|
105次组卷
|
2卷引用:山东省济南市2023-2024学年高二上学期1月期末化学试题
5 . 液流电池是电化学储能领域的研究热点,其电解液置于电堆外部,在循环泵的推动下流经电堆,实现化学能与电能的转换。下图是全钒液流电池的结构及工作原理示意图。

下列说法正确的是

下列说法正确的是
| A.充电时M极应与电源的负极相连 |
B.充电时总反应: |
C.放电时每转移 ,有 ,有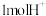 通过交换膜移向N极区 通过交换膜移向N极区 |
D.放电时正极反应式: |
您最近一年使用:0次
名校
解题方法
6 . 下列装置可分离废水中的Co2+和Ni2+。已知Ni2+和Co2+性质相似,Co2+和乙酰丙酮不反应。下列说法正确的是

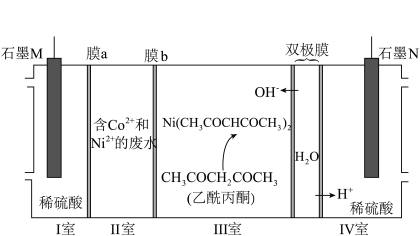


| A.M电极接太阳能电池的P电极 |
| B.通电一段时间后,I、IV室内溶液pH均减小 |
| C.膜a、膜b分别为阳离子交换膜和阴离子交换膜 |
D.每生成1molSO ,理论上双极膜至少解离7molH2O ,理论上双极膜至少解离7molH2O |
您最近一年使用:0次
2023-03-03更新
|
1384次组卷
|
3卷引用:山东省青岛市第二中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
7 . 请按要求回答下列问题。
(1) ,
, 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度约为
浓度约为______  。
。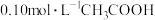 溶液加适量的水稀释,下列表达式的数值变大的是
溶液加适量的水稀释,下列表达式的数值变大的是______ (填标号)。
A. B.
B. C.
C. D.
D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
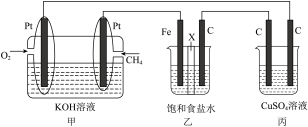
①甲装置中负极反应式为________ 。
②乙装置中石墨电极上生成的气体为________ (填化学式)。
③丙装置中 足量,工作一段时间后,溶液的
足量,工作一段时间后,溶液的
________ (填“变大”、“变小”或“不变”),反应的化学方程式为________ ,若要将电解后的溶液复原,需加入一定量的________ (填化学式)。
(1)
 ,
, 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度约为
浓度约为 。
。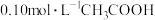 溶液加适量的水稀释,下列表达式的数值变大的是
溶液加适量的水稀释,下列表达式的数值变大的是A.
 B.
B. C.
C. D.
D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
A.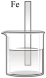 | B. | C.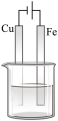 | D.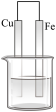 |

①甲装置中负极反应式为
②乙装置中石墨电极上生成的气体为
③丙装置中
 足量,工作一段时间后,溶液的
足量,工作一段时间后,溶液的
您最近一年使用:0次
2023-02-13更新
|
830次组卷
|
6卷引用:山东省泰安市部分学校2023-2024学年高二上学期期末调研化学试题
解题方法
8 . 处理含甲醇的废水并进行粗铜精炼的装置如图所示。下列说法错误的是
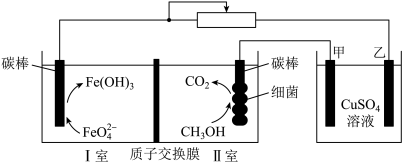

| A.甲电极应为粗铜 |
| B.理论上每产生标准状况下1.12LCO2,甲电极增重9.6g |
| C.装置工作一段时间后,I室中溶液的pH变小 |
| D.原电池负极反应式为CH3OH+H2O-6e-=CO2+6H+ |
您最近一年使用:0次
9 . 全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长,利用该电池电解处理含 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
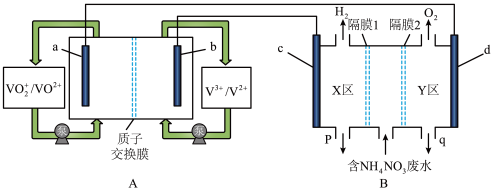
回答下列问题:
(1)a电极为_______ (填“正极”或“负极”),其电极反应式为_______ 。
(2)隔膜1为_______ 交换膜(填“阴离子”或“阳离子”),q口流出液含有的溶质为_______ (填化学式),d电极的电极反应式为_______ 。
(3)B装置中产生的气体总量为336 mL(标准状况下)时,通过质子交换膜的 的物质的量为
的物质的量为_______ mol。
 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
回答下列问题:
(1)a电极为
(2)隔膜1为
(3)B装置中产生的气体总量为336 mL(标准状况下)时,通过质子交换膜的
 的物质的量为
的物质的量为
您最近一年使用:0次
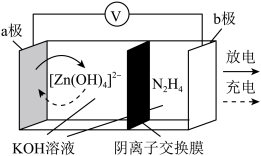
10 . 科学家近日发明了一种无污染、无需净化高效产氢的可充电电池,电池示意图如下。电极为金属锌和选择性催化材料,实现了阴极析氢和 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
 氧化两个独立的反应,可稳定循环600次。下列说法错误的是
氧化两个独立的反应,可稳定循环600次。下列说法错误的是
A.充电时,阴极区溶液 减小 减小 |
B.放电时, 由b极区向a极区迁移 由b极区向a极区迁移 |
| C.充电时,b极反应式为N2H4-4e-+4OH-=N2+4H2O |
D.产生 ,a极质量增大 ,a极质量增大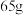 |
您最近一年使用:0次



