解题方法
1 . 双极膜是一种复合膜,在直流电作用下,能把中间界面内的H2O解离为H+和OH-,并使离子定向通过。

以铅蓄电池为电源(放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O),利用双极膜电解获得NaOH与H3PO4的原理如图所示。下列说法正确的是

以铅蓄电池为电源(放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O),利用双极膜电解获得NaOH与H3PO4的原理如图所示。下列说法正确的是
| A.N膜为阳离子交换膜 |
| B.产品室2中溶液pH逐渐增大 |
C.产品室1中反应为 +2OH-= +2OH-= +2H2O +2H2O |
| D.双极膜共解离4molH2O时,理论上铅蓄电池中生成2molPbSO4 |
您最近一年使用:0次
2 . 实现“碳达峰”“碳中和”是国家的重要战略目标,是实现中华民族永续发展的必然选择。
Ⅰ.我国科学家以 和
和 为催化剂,用
为催化剂,用 将
将 还原为
还原为 。
。
(1)基态镍原子价电子排布式为_______ 。
(2)已知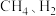 的燃烧热
的燃烧热 分别为
分别为 ,写出
,写出 和
和 下
下 与
与 反应生成
反应生成 和液态
和液态 的热化学方程式
的热化学方程式_______ 。
(3)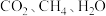 三种分子中键角由大到小排列的顺序是
三种分子中键角由大到小排列的顺序是_______ , 的
的 模型名称为
模型名称为_______ 。
(4)已知 的晶体结构与
的晶体结构与 相似(晶体结构如下图所示),其摩尔质量为
相似(晶体结构如下图所示),其摩尔质量为 ,晶体密度为
,晶体密度为 ,则
,则 和O之间的最近距离为
和O之间的最近距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。已知某氧化镍样品组成为
为阿伏加德罗常数的值)。已知某氧化镍样品组成为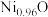 ,该晶体中
,该晶体中 与
与 的个数之比为
的个数之比为_______ 。

Ⅱ.基于亲电微生物催化的 甲烷化反应也是一种清洁高效的可持续生产方式,其原理如图所示。
甲烷化反应也是一种清洁高效的可持续生产方式,其原理如图所示。

(5)电极Ⅰ是_______ 极,电极Ⅱ的电极反应式为_______ 。
Ⅲ.二氧化碳催化加氢生成甲醇和水,也有利于减少温室效应。其总反应分为以下两步:
第一步:

第二步: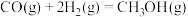

(6)已知 ,第一步反应为决定速率的反应。请在下图中补全上述总反应过程的“能量变化-反应历程”示意图
,第一步反应为决定速率的反应。请在下图中补全上述总反应过程的“能量变化-反应历程”示意图_______ 。

Ⅰ.我国科学家以
 和
和 为催化剂,用
为催化剂,用 将
将 还原为
还原为 。
。(1)基态镍原子价电子排布式为
(2)已知
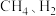 的燃烧热
的燃烧热 分别为
分别为 ,写出
,写出 和
和 下
下 与
与 反应生成
反应生成 和液态
和液态 的热化学方程式
的热化学方程式(3)
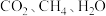 三种分子中键角由大到小排列的顺序是
三种分子中键角由大到小排列的顺序是 的
的 模型名称为
模型名称为(4)已知
 的晶体结构与
的晶体结构与 相似(晶体结构如下图所示),其摩尔质量为
相似(晶体结构如下图所示),其摩尔质量为 ,晶体密度为
,晶体密度为 ,则
,则 和O之间的最近距离为
和O之间的最近距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。已知某氧化镍样品组成为
为阿伏加德罗常数的值)。已知某氧化镍样品组成为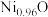 ,该晶体中
,该晶体中 与
与 的个数之比为
的个数之比为
Ⅱ.基于亲电微生物催化的
 甲烷化反应也是一种清洁高效的可持续生产方式,其原理如图所示。
甲烷化反应也是一种清洁高效的可持续生产方式,其原理如图所示。
(5)电极Ⅰ是
Ⅲ.二氧化碳催化加氢生成甲醇和水,也有利于减少温室效应。其总反应分为以下两步:
第一步:


第二步:
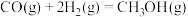

(6)已知
 ,第一步反应为决定速率的反应。请在下图中补全上述总反应过程的“能量变化-反应历程”示意图
,第一步反应为决定速率的反应。请在下图中补全上述总反应过程的“能量变化-反应历程”示意图
您最近一年使用:0次
名校
解题方法
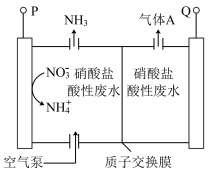
3 . 硝酸盐电解还原生成氨是实现硝酸盐废水资源化利用的有效途径。一种采用双室电解法电解硝酸盐酸性废水生成 的装置如图所示,P、Q均连接惰性电极,下列说法不正确的是
的装置如图所示,P、Q均连接惰性电极,下列说法不正确的是
 的装置如图所示,P、Q均连接惰性电极,下列说法不正确的是
的装置如图所示,P、Q均连接惰性电极,下列说法不正确的是
| A.P连接外接电源的负极 |
B.电解一段时间后,左室溶液的 将增大 将增大 |
C.生成的 与气体A可作为硝酸工业的原料 与气体A可作为硝酸工业的原料 |
D.理论上每转化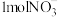 时,有 时,有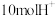 通过质子交换膜 通过质子交换膜 |
您最近一年使用:0次
2023-12-02更新
|
312次组卷
|
2卷引用:广东省肇庆市2024届高三上学期毕业班第一次教学质量检测化学试题
解题方法
4 . 我国将在2030年前实现碳达峰、2060年前实现碳中和。 的资源化利用能有效减少
的资源化利用能有效减少 排放,某研究小组利用工业废气中的
排放,某研究小组利用工业废气中的 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应:
已知:Ⅰ.
Ⅱ.
(1)根据以上化学反应方程式,计算反应热
_______ 。
(2)下列有关合成甲醇的说法中正确的是_______(填标号)。
(3)反应温度和催化剂组成与反应物 的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
注:“甲醇选择性”是指生成甲醇的二氧化碳占所有参与反应的二氧化碳的百分比。
结合表中数据可知,用 生产甲醇的最优条件为
生产甲醇的最优条件为_______ (填实验编号)。
(4)下图为一定温度下, 时,氢气的转化率
时,氢气的转化率 与投料比
与投料比
 的关系图像,请在图中画出相同温度下,压强为
的关系图像,请在图中画出相同温度下,压强为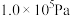 时对应的变化曲线。
时对应的变化曲线。_________

(5)某研究小组采用甲醇燃料电池,以石墨为电极材料进行电解饱和NaCl溶液的实验,装置如图所示:

①甲醇燃料电池工作时,甲醇应由_______ (填“a”或“b”)口通入。该燃料电池的正极反应式为_______ 。
②电解一段时间后,c1、c2电极上均有气体产生,其中c2电极上得到的是_______ ,电解NaCl溶液的离子方程式为_______ 。
 的资源化利用能有效减少
的资源化利用能有效减少 排放,某研究小组利用工业废气中的
排放,某研究小组利用工业废气中的 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应:
已知:Ⅰ.

Ⅱ.

(1)根据以上化学反应方程式,计算反应热

(2)下列有关合成甲醇的说法中正确的是_______(填标号)。
| A.增大氢气的浓度,有利于提高甲醇的产率 |
| B.选择合适的催化剂,有利于平衡正向移动 |
| C.低温有利于平衡正向移动,因此实际生产中温度越低越好 |
| D.高压有利于平衡正向移动,因此实际生产中压强越高越好 |
 的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:| 实验编号 | 温度/℃ | 催化剂组成 |  转化率/% 转化率/% | 甲醇选择性/% |
| 甲 | 250 | 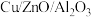 | 12.3 | 42.3 |
| 乙 | 250 | 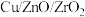 | 30.3 | 87.2 |
| 丙 | 300 | 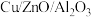 | 15.3 | 38.5 |
| 丁 | 300 | 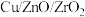 | 30.5 | 60.2 |
结合表中数据可知,用
 生产甲醇的最优条件为
生产甲醇的最优条件为(4)下图为一定温度下,
 时,氢气的转化率
时,氢气的转化率 与投料比
与投料比
 的关系图像,请在图中画出相同温度下,压强为
的关系图像,请在图中画出相同温度下,压强为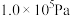 时对应的变化曲线。
时对应的变化曲线。
(5)某研究小组采用甲醇燃料电池,以石墨为电极材料进行电解饱和NaCl溶液的实验,装置如图所示:

①甲醇燃料电池工作时,甲醇应由
②电解一段时间后,c1、c2电极上均有气体产生,其中c2电极上得到的是
您最近一年使用:0次
5 . 2022年11月10日,中国科学院成功开发出能量密度高、可逆性高的Cd-Mn混合型液流电池。该电池放电时的工作原理如下图所示,下列说法正确的是
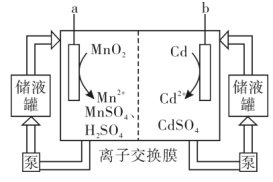

| A.放电时,a极发生氧化反应 |
B.放电时,b极区电解质溶液中 减小 减小 |
C.充电时,a极发生的电极反应为 |
D.充电时,b极区溶液减重20.8g时,外电路理论上通过 个电子 个电子 |
您最近一年使用:0次
名校
6 . 氢气是一种清洁能源,水和甲烷都是常见的制氢原料。
(1)下列有关 与
与 的说法正确的是______(填标号)。
的说法正确的是______(填标号)。
Ⅰ.水制氢
(2)已知 的燃烧热
的燃烧热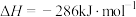 ,电解液态水制氢的热化学方程式为
,电解液态水制氢的热化学方程式为__________ 。
(3)一种以水为原料制氢的原理示意图如下。催化剂在太阳能的作用下产生电子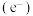 和空穴
和空穴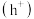 ,电子和空穴分别与
,电子和空穴分别与 和
和 发生反应。用离子方程式表示氧气的产生原理
发生反应。用离子方程式表示氧气的产生原理______ ;氢气在______ (填“阴”或“阳”)极生成。

Ⅱ.甲烷制氢
(4)甲烷水蒸气重整涉及以下反应:



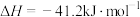
则 的
的
__________  。
。
(5)甲烷化学链重整技术包括两个步骤。
第一步:金属氧化物(用 表示)与甲烷发生部分氧化反应,生成
表示)与甲烷发生部分氧化反应,生成 与合成气(
与合成气( 与
与 的混合气体)。
的混合气体)。
第二步: 作为氧化剂,将
作为氧化剂,将 氧化再生为
氧化再生为 。
。
如图为一定条件下,气流比 和
和 对合成气物质的量之比
对合成气物质的量之比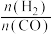 的影响。由图可知:①
的影响。由图可知:①__________ ;②__________ 。

(1)下列有关
 与
与 的说法正确的是______(填标号)。
的说法正确的是______(填标号)。| A.均为极性分子 | B. 模型均为四面体形 模型均为四面体形 |
| C.均可以作为配合物的配体 | D.均存在分子间氢键 |
Ⅰ.水制氢
(2)已知
 的燃烧热
的燃烧热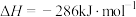 ,电解液态水制氢的热化学方程式为
,电解液态水制氢的热化学方程式为(3)一种以水为原料制氢的原理示意图如下。催化剂在太阳能的作用下产生电子
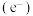 和空穴
和空穴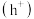 ,电子和空穴分别与
,电子和空穴分别与 和
和 发生反应。用离子方程式表示氧气的产生原理
发生反应。用离子方程式表示氧气的产生原理
Ⅱ.甲烷制氢
(4)甲烷水蒸气重整涉及以下反应:



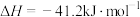
则
 的
的
 。
。(5)甲烷化学链重整技术包括两个步骤。
第一步:金属氧化物(用
 表示)与甲烷发生部分氧化反应,生成
表示)与甲烷发生部分氧化反应,生成 与合成气(
与合成气( 与
与 的混合气体)。
的混合气体)。第二步:
 作为氧化剂,将
作为氧化剂,将 氧化再生为
氧化再生为 。
。如图为一定条件下,气流比
 和
和 对合成气物质的量之比
对合成气物质的量之比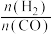 的影响。由图可知:①
的影响。由图可知:①
您最近一年使用:0次
2022-11-13更新
|
190次组卷
|
2卷引用:广东省肇庆市肇庆一中2023届高中毕业班第一次教学质量检测化学试题
名校
7 . 磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的循环寿命,放电时的反应为:LixC6+Li1-xFePO4=6C+LiFePO4。某磷酸铁锂电池的切面如图所示。下列说法错误 的是


| A.放电时Li+脱离石墨,经电解质嵌入正极 |
| B.隔膜在反应过程中只允许Li+通过 |
| C.充电时电池正极上发生的反应为:LiFePO4-xe-=Li1-xFePO4+xLi+ |
| D.充电时电子从电源正极经铝箔流入正极材料 |
您最近一年使用:0次
2022-04-11更新
|
239次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
8 . 电化学装置可实现化学能与电能的直接转化,是助力实现“30、60”双碳目标的一种重要路径。回答下列问题:
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。图1装置中盐桥中装的是含有琼脂的 饱和溶液,电池工作时,
饱和溶液,电池工作时, 移向
移向___________ (填“左”或“右”)池, 电极上的电极反应式为
电极上的电极反应式为___________ 。
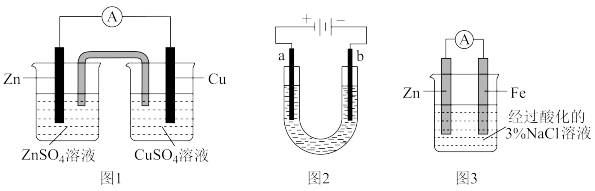
②将图1右池中的 电极材料换成
电极材料换成___________ ,电解质溶液换成___________ ,可实现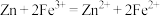 中能量直接转化为电能。若起始时两电极质量相等,当电路中通过
中能量直接转化为电能。若起始时两电极质量相等,当电路中通过 电子时,左右两侧电极质量差为
电子时,左右两侧电极质量差为___________ 。
(2)电解池在工业及生产中广泛应用,其原理如图2所示。
①电镀时,a电极应为___________ (选填“待镀金属”或“镀层金属”);精炼铜时, 在电解质溶液中由
在电解质溶液中由___________ (填“a”或“b”,下同)电极移向___________ 电极。
②氯碱工业中,b电极上发生的电极反应式为___________ 。
(3)钢铁的腐蚀过程中会产生腐蚀电流。可采用图3所示装置对 进行保护。请设计实验探究该装置是否能有效防止
进行保护。请设计实验探究该装置是否能有效防止 发生腐蚀:
发生腐蚀:___________ 。
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。图1装置中盐桥中装的是含有琼脂的
 饱和溶液,电池工作时,
饱和溶液,电池工作时, 移向
移向 电极上的电极反应式为
电极上的电极反应式为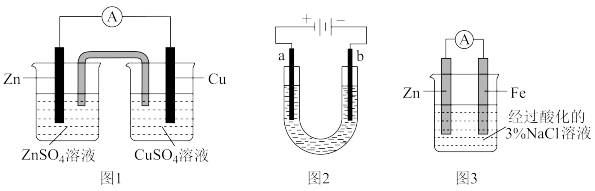
②将图1右池中的
 电极材料换成
电极材料换成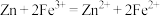 中能量直接转化为电能。若起始时两电极质量相等,当电路中通过
中能量直接转化为电能。若起始时两电极质量相等,当电路中通过 电子时,左右两侧电极质量差为
电子时,左右两侧电极质量差为(2)电解池在工业及生产中广泛应用,其原理如图2所示。
①电镀时,a电极应为
 在电解质溶液中由
在电解质溶液中由②氯碱工业中,b电极上发生的电极反应式为
(3)钢铁的腐蚀过程中会产生腐蚀电流。可采用图3所示装置对
 进行保护。请设计实验探究该装置是否能有效防止
进行保护。请设计实验探究该装置是否能有效防止 发生腐蚀:
发生腐蚀:
您最近一年使用:0次
9 . 二甲醚( )燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质
)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质 的原理如图所示(反应中Ⅱ室
的原理如图所示(反应中Ⅱ室 溶液浓度变大)。下列说法正确的是
溶液浓度变大)。下列说法正确的是

 )燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质
)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质 的原理如图所示(反应中Ⅱ室
的原理如图所示(反应中Ⅱ室 溶液浓度变大)。下列说法正确的是
溶液浓度变大)。下列说法正确的是
| A.b为燃料电池的负极 |
| B.m为阴离子交换膜 |
C.电解池阴极的电极反应式为 |
| D.当有2.24L二甲醚参与反应时,理论上镍棒质量增加70.8g |
您最近一年使用:0次
10 . 用如图甲所示装置模拟对含高浓度Cl-的工业废水进行脱氮,该溶液中ClO-的浓度随时间变化的关系如图乙所示。一段时间后溶液中所有氮原子均转化为N2被脱去。

下列说法错误的是

下列说法错误的是
| A.b接电源负极 |
B.开始时ClO-的浓度增长较慢的原因可能是氧化溶液中的 |
| C.电解过程中,a极附近pH降低 |
D.理论上溶液中的 先被脱尽 先被脱尽 |
您最近一年使用:0次
2022-01-22更新
|
496次组卷
|
3卷引用:广东省肇庆市2021-2022学年高三第二次模拟考试化学试题
广东省肇庆市2021-2022学年高三第二次模拟考试化学试题广东省2021-2022学年高三一轮复习质量检测化学试题(已下线)押广东卷化学第16题 电解池-备战2022年高考化学临考题号押题(广东卷)



