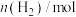名校
解题方法
1 . 下列化学反应表示不正确的是
A.硝酸受热分解的化学反应方程式: |
B.ICl与 溶液反应: 溶液反应: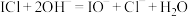 |
C. 溶于 溶于 溶液: 溶液: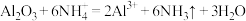 |
D.工业上,可通过电解KF的无水HF溶液(含 和 和 )制取 )制取 ,则 ,则 在阴极放电反应为 在阴极放电反应为 |
您最近半年使用:0次
昨日更新
|
97次组卷
|
2卷引用:湖南省长沙市第一中学2023-2024学年高三下学期4月月考化学试题
名校
2 . I.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)CO 的空间结构是
的空间结构是_______ 。
(2) 溶液呈
溶液呈_______ (填“酸性”“碱性”或“中性”)。
(3)物质的量浓度均为0.1mol·L−1的下列四种溶液:pH由小到大 排列的顺序是_______ 。(填序号)
①CH3COONa②Na2CO3③NaClO④NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_______ 。
II.为实现“双碳”目标,用二氧化碳制备甲醇可实现二氧化碳资源化利用、降低碳排放。回答下列问题:
已知:反应1:

反应2:
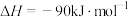
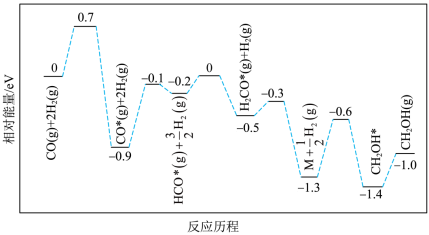
(5)则反应3: 催化加氢制取
催化加氢制取 的热化学方程式为
的热化学方程式为_______ 。
(6)反应2的反应历程如下图所示,其中吸附在催化剂表面的物种用*标注。_______ 。
III.为了探究电解池的工作原理,某研究性学习小组用下图所示的装置进行实验。实验时该小组同学发现两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
(7)电解过程中,Y极发生的电极反应为_______ 、_______ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.810−5 | Kal=4.310−7、Ka2=5.610−11 | Ka=3.010−8 |
 的空间结构是
的空间结构是(2)
 溶液呈
溶液呈(3)物质的量浓度均为0.1mol·L−1的下列四种溶液:pH
①CH3COONa②Na2CO3③NaClO④NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
II.为实现“双碳”目标,用二氧化碳制备甲醇可实现二氧化碳资源化利用、降低碳排放。回答下列问题:
已知:反应1:


反应2:

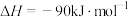
(5)则反应3:
 催化加氢制取
催化加氢制取 的热化学方程式为
的热化学方程式为(6)反应2的反应历程如下图所示,其中吸附在催化剂表面的物种用*标注。
III.为了探究电解池的工作原理,某研究性学习小组用下图所示的装置进行实验。实验时该小组同学发现两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(7)电解过程中,Y极发生的电极反应为
您最近半年使用:0次
名校
3 . 钛被称为“二十一世纪的金属”,绿矾是重要的化工原料,用钛铁矿[主要成分是钛酸亚铁( ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: (无色)、
(无色)、 (紫色)形式存在。
(紫色)形式存在。
请回答下列问题:
(1)硫酸与 反应生成
反应生成 的化学方程式是
的化学方程式是______ 。向滤液1中加入适量铁粉,至刚好出现紫色为止,此时溶液仍呈强酸性。已知:氧化性: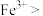
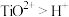 ,则加入适量铁粉的原因是
,则加入适量铁粉的原因是______ 。
(2)系列操作具体为______ ,经系列操作后,再对所得到的绿矾晶体用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为______ 。
(3)滤液2中加入适量的试剂A,A可选用______ (填标号)。
a.稀硫酸 b.碳酸镁 c.二氧化碳 d.鼓入空气
(4)用石墨作阳极、钛网作阴极、熔融 -CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:______ 。 中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
______ kg。
(6)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为______ 。
 ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: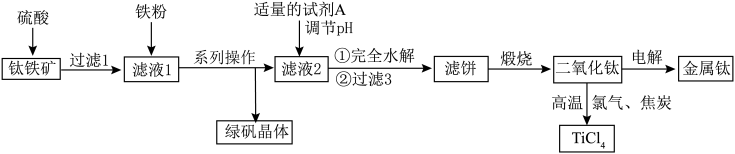
 (无色)、
(无色)、 (紫色)形式存在。
(紫色)形式存在。请回答下列问题:
(1)硫酸与
 反应生成
反应生成 的化学方程式是
的化学方程式是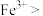
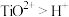 ,则加入适量铁粉的原因是
,则加入适量铁粉的原因是(2)系列操作具体为
(3)滤液2中加入适量的试剂A,A可选用
a.稀硫酸 b.碳酸镁 c.二氧化碳 d.鼓入空气
(4)用石墨作阳极、钛网作阴极、熔融
 -CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
 中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
(6)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近半年使用:0次
解题方法
4 . 如图是一个用石墨作电极,电解稀 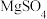 溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的
溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的  范围是
范围是  ,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。___________ (填序号)。
①A管溶液由红色变为黄色 ②B管溶液由红色变为黄色
③A管溶液不变色 ④B管溶液不变色
(2)写出 管中发生的电极反应:
管中发生的电极反应:___________ ;
(3)写出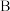 管中发生的电极反应:
管中发生的电极反应:___________ ;
(4)检验 管中气体的方法是
管中气体的方法是___________ ;
(5)若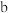 管中生成标况下气体
管中生成标况下气体  ,则该装置电解过程中转移的电子数目为
,则该装置电解过程中转移的电子数目为___________ 。
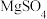 溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的
溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的  范围是
范围是  ,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。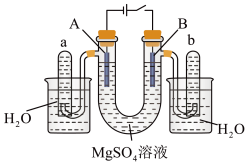
①A管溶液由红色变为黄色 ②B管溶液由红色变为黄色
③A管溶液不变色 ④B管溶液不变色
(2)写出
 管中发生的电极反应:
管中发生的电极反应:(3)写出
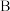 管中发生的电极反应:
管中发生的电极反应:(4)检验
 管中气体的方法是
管中气体的方法是(5)若
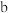 管中生成标况下气体
管中生成标况下气体  ,则该装置电解过程中转移的电子数目为
,则该装置电解过程中转移的电子数目为
您最近半年使用:0次
5 . 用 制备
制备 有利于实现“双碳”目标。涉及的主要反应为:
有利于实现“双碳”目标。涉及的主要反应为:
Ⅰ.2CO2(g)+6H2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g) 
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 
(1)已知 时,部分物质的相对能量如下表所示(忽略
时,部分物质的相对能量如下表所示(忽略 随温度的变化):则
随温度的变化):则
___________  。
。
(2)在一定条件下的密闭容器中发生上述反应,若要提高反应Ⅰ中 的平衡转化率并加快反应速率,可以采取的措施有___________(填标号)。
的平衡转化率并加快反应速率,可以采取的措施有___________(填标号)。
(3)向某刚性容器中按投料比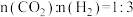 充入
充入 和
和 ,在不同催化剂(M、N)下发生上述反应。一段时间后,测得
,在不同催化剂(M、N)下发生上述反应。一段时间后,测得 的转化率、
的转化率、 的选择性(含碳生成物中
的选择性(含碳生成物中 的百分含量)随温度的变化如图所示。
的百分含量)随温度的变化如图所示。___________ 的催化效果好(填“M”或“N”)。
②500~800K之间,乙烯的选择性随温度变化的原因是___________ 。
(4)在一定条件下,向密闭容器中充入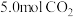 和
和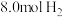 ,发生反应2CO2(g)+6H2(g)
,发生反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g) 。测得相同时间内,
C2H4(g)+4H2O(g) 。测得相同时间内, 的转化率随温度的变化如图所示(虚线表示
的转化率随温度的变化如图所示(虚线表示 的平衡转化率随温度的变化)。
的平衡转化率随温度的变化)。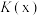
___________ 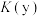 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②已知z点体系的压强为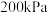 ,则
,则 时,该反应的标准平衡常数
时,该反应的标准平衡常数
___________ (保留2位小数,已知:分压=总压×该组分物质的量分数,对于反应的dD(g)+eE(g) gG(g)+ hH (g),
gG(g)+ hH (g),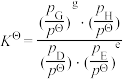 ,其中
,其中 ,
,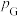 、
、 、
、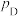 、
、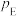 为各组分的平衡分压)。
为各组分的平衡分压)。
(5)利用电解法制取乙烯的装置如图所示,则电极a为电解池的___________ 极,a极反应式为___________ 。
 制备
制备 有利于实现“双碳”目标。涉及的主要反应为:
有利于实现“双碳”目标。涉及的主要反应为:Ⅰ.2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g) 
Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g) 
(1)已知
 时,部分物质的相对能量如下表所示(忽略
时,部分物质的相对能量如下表所示(忽略 随温度的变化):则
随温度的变化):则
 。
。| 物质 |  | 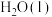 |  |  |  |  |
| 相对能量(kJ/mol) | -393 | -286 | -242 | -110 | 0 | 52 |
(2)在一定条件下的密闭容器中发生上述反应,若要提高反应Ⅰ中
 的平衡转化率并加快反应速率,可以采取的措施有___________(填标号)。
的平衡转化率并加快反应速率,可以采取的措施有___________(填标号)。| A.增大压强 | B.增大 浓度 浓度 |
| C.降低温度 | D.液化分离出水蒸气 |
(3)向某刚性容器中按投料比
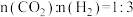 充入
充入 和
和 ,在不同催化剂(M、N)下发生上述反应。一段时间后,测得
,在不同催化剂(M、N)下发生上述反应。一段时间后,测得 的转化率、
的转化率、 的选择性(含碳生成物中
的选择性(含碳生成物中 的百分含量)随温度的变化如图所示。
的百分含量)随温度的变化如图所示。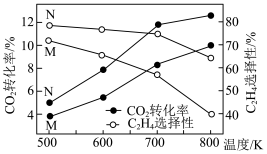
②500~800K之间,乙烯的选择性随温度变化的原因是
(4)在一定条件下,向密闭容器中充入
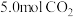 和
和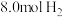 ,发生反应2CO2(g)+6H2(g)
,发生反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g) 。测得相同时间内,
C2H4(g)+4H2O(g) 。测得相同时间内, 的转化率随温度的变化如图所示(虚线表示
的转化率随温度的变化如图所示(虚线表示 的平衡转化率随温度的变化)。
的平衡转化率随温度的变化)。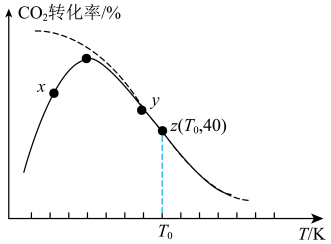
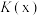
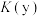 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②已知z点体系的压强为
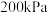 ,则
,则 时,该反应的标准平衡常数
时,该反应的标准平衡常数
 gG(g)+ hH (g),
gG(g)+ hH (g),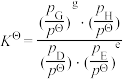 ,其中
,其中 ,
,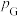 、
、 、
、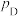 、
、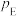 为各组分的平衡分压)。
为各组分的平衡分压)。(5)利用电解法制取乙烯的装置如图所示,则电极a为电解池的
您最近半年使用:0次
6 . 从废旧锌锰电池处理后的废料[含 、
、 、
、 、Fe等]制备Zn和
、Fe等]制备Zn和 的一种工艺流程如图:
的一种工艺流程如图: 在pH大于5.5时易被氧化。
在pH大于5.5时易被氧化。
下列说法不正确的是
 、
、 、
、 、Fe等]制备Zn和
、Fe等]制备Zn和 的一种工艺流程如图:
的一种工艺流程如图: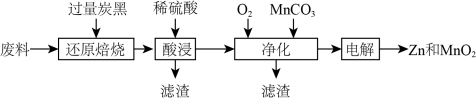
 在pH大于5.5时易被氧化。
在pH大于5.5时易被氧化。下列说法不正确的是
| A.“还原焙烧”的主要作用是还原锰元素,有利于“酸浸”时溶出 |
| B.“酸浸”过程得到的滤渣主要成分为炭黑 |
C.“净化”时应该先通氧气氧化亚铁离子,后加入 调节溶液的pH小于5.5,使 调节溶液的pH小于5.5,使 沉淀 沉淀 |
D.“电解”时阳极反应式为 |
您最近半年使用:0次
7 . 研究氮氧化物污染及其治理是环保的一项重要工作,将 污染物转化为无害的
污染物转化为无害的 或高附加值的含氮化学品具有重要意义。
或高附加值的含氮化学品具有重要意义。
(1)氢气可以消除氮氧化物污染,其中 反应体系能量随反应过程的变化情况如图:
反应体系能量随反应过程的变化情况如图:__________ (填“吸热”或“放热”)反应;
②已知: 、
、 、
、 、
、 中的化学键全部断裂形成气态原子所需要的能量如下表所示:
中的化学键全部断裂形成气态原子所需要的能量如下表所示:
当该反应消耗 的能量变化为
的能量变化为__________ kJ(用含a、b、c、d的代数式表示).
(2)经实验证明, 的正反应速率可以表示为
的正反应速率可以表示为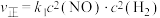 ,逆反应速率可以表示为
,逆反应速率可以表示为 (
( 、
、 为速率常数.其大小与浓度变化无关);若压缩容器的容积,
为速率常数.其大小与浓度变化无关);若压缩容器的容积,
__________ (填“增大”“减小”或“不变”,下同),
__________ ;速率的变化量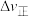
__________ 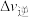 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)在 恒容密闭的恒温容器中,投入
恒容密闭的恒温容器中,投入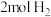 和
和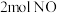 发生
发生 ,其中
,其中 随时间的变化如下表:
随时间的变化如下表:
该反应条件下反应达到平衡时,NO的转化率为__________ ; 的体积百分含量为
的体积百分含量为__________ %(保留2位有效数字)。
(4)直接电催化NO使其转化为有价值的 是一种有吸引力的策略,装置如图所示,双极膜由阴离子交换膜和阳离子交换膜组成,放电时,双极膜中间层的
是一种有吸引力的策略,装置如图所示,双极膜由阴离子交换膜和阳离子交换膜组成,放电时,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移;
,并向两极迁移;__________ 反应(填“氧化”或“还原”);
②写出负极的电极反应式:__________ 。
 污染物转化为无害的
污染物转化为无害的 或高附加值的含氮化学品具有重要意义。
或高附加值的含氮化学品具有重要意义。(1)氢气可以消除氮氧化物污染,其中
 反应体系能量随反应过程的变化情况如图:
反应体系能量随反应过程的变化情况如图:
②已知:
 、
、 、
、 、
、 中的化学键全部断裂形成气态原子所需要的能量如下表所示:
中的化学键全部断裂形成气态原子所需要的能量如下表所示:物质 |
|
|
|
|
能量 | a | b | c | d |
 的能量变化为
的能量变化为(2)经实验证明,
 的正反应速率可以表示为
的正反应速率可以表示为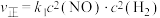 ,逆反应速率可以表示为
,逆反应速率可以表示为 (
( 、
、 为速率常数.其大小与浓度变化无关);若压缩容器的容积,
为速率常数.其大小与浓度变化无关);若压缩容器的容积,

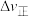
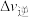 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)在
 恒容密闭的恒温容器中,投入
恒容密闭的恒温容器中,投入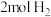 和
和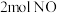 发生
发生 ,其中
,其中 随时间的变化如下表:
随时间的变化如下表:时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 2.00 | 1.80 | 1.50 | 1.44 | 1.40 | 1.40 |
 的体积百分含量为
的体积百分含量为(4)直接电催化NO使其转化为有价值的
 是一种有吸引力的策略,装置如图所示,双极膜由阴离子交换膜和阳离子交换膜组成,放电时,双极膜中间层的
是一种有吸引力的策略,装置如图所示,双极膜由阴离子交换膜和阳离子交换膜组成,放电时,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移;
,并向两极迁移;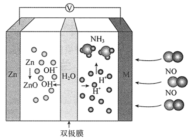
②写出负极的电极反应式:
您最近半年使用:0次
名校
解题方法
8 . 一种以氨基钾(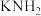 )作电解质,电解液氨制氢气的装置如图所示,下列说法错误的是
)作电解质,电解液氨制氢气的装置如图所示,下列说法错误的是
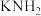 )作电解质,电解液氨制氢气的装置如图所示,下列说法错误的是
)作电解质,电解液氨制氢气的装置如图所示,下列说法错误的是
A.阴极上的电极反应式为 |
B.电解过程中,阳极 浓度增大 浓度增大 |
| C.氨基钾的作用是提高液氨的导电能力 |
D.制得3mol 需要消耗2mol液氨 需要消耗2mol液氨 |
您最近半年使用:0次
9 . 下列反应的离子方程式不正确的是
A.金属铅溶于 溶液: 溶液: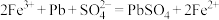 |
B.铅酸蓄电池充电时的阴极反应: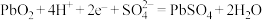 |
C.普通锌锰干电池(电解质主要成分为氯化铵)的正极反应: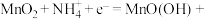  |
D.实验室用 水解制备 水解制备 |
您最近半年使用:0次
名校
解题方法
10 . 党的二十大报告中强调“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。
 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:
Ⅰ.利用 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
①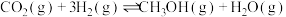
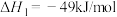
②
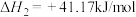
③

(1)反应③中活化能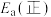
__________ (填“>”或“<”)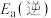 。
。
(2)在催化剂作用下,按 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示: 。
。
①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因__________ ,在实际工业生产中压强不能过高也不能过低的原因是______________________________ 。
② 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=__________ MPa,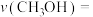
__________ MPa/min,反应②的
__________ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
Ⅱ.近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: ,则该电极反应式为
,则该电极反应式为____________________ 。

 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:Ⅰ.利用
 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:①
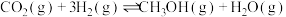
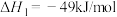
②

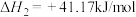
③


(1)反应③中活化能
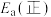
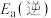 。
。(2)在催化剂作用下,按
 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
 。
。①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因
②
 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=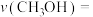

 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。Ⅱ.近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: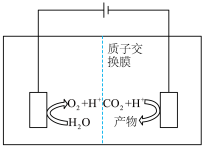
 ,则该电极反应式为
,则该电极反应式为
您最近半年使用:0次