名校
1 . 以 为原料制备氧钒(Ⅳ)碱式碳酸铵
为原料制备氧钒(Ⅳ)碱式碳酸铵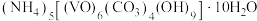 。其过程为:
。其过程为:
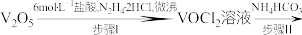 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知 能被
能被 氧化,回答下列问题:
氧化,回答下列问题:
(1)步骤I的反应装置如图(夹持及加热装置略去)
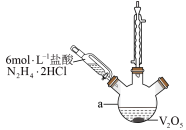
①仪器a的名称为___________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为___________ 。
(2)步骤Ⅱ可在如下图装置中进行。
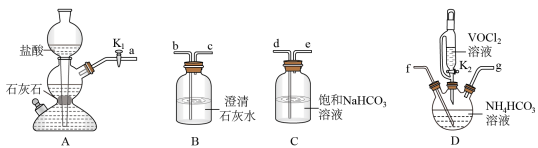
①接口的连接顺序为a→___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是___________ 。当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取mg氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(Ⅴ)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
①产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
②下列情况会导致产品纯度偏小的是___________ (填标号)。
A.滴定达终点时,俯视刻度线读数
B.用标准液润洗滴定管后,液体从上口倒出
C.滴定达终点时,发现滴定管尖嘴内有气泡生成
(4)一种以 和Zn为电极、
和Zn为电极、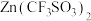 水溶液为电解质的电池,其示意图如下所示。放电时,
水溶液为电解质的电池,其示意图如下所示。放电时, 可插入
可插入 层间形成
层间形成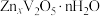 。
。
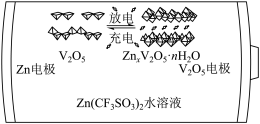
则其充电时阳极的电极反应式为___________ 。
 为原料制备氧钒(Ⅳ)碱式碳酸铵
为原料制备氧钒(Ⅳ)碱式碳酸铵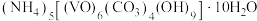 。其过程为:
。其过程为: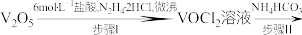 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知
 能被
能被 氧化,回答下列问题:
氧化,回答下列问题:(1)步骤I的反应装置如图(夹持及加热装置略去)

①仪器a的名称为
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行。

①接口的连接顺序为a→
②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取mg氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(Ⅴ)元素均以
 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)①产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为②下列情况会导致产品纯度偏小的是
A.滴定达终点时,俯视刻度线读数
B.用标准液润洗滴定管后,液体从上口倒出
C.滴定达终点时,发现滴定管尖嘴内有气泡生成
(4)一种以
 和Zn为电极、
和Zn为电极、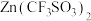 水溶液为电解质的电池,其示意图如下所示。放电时,
水溶液为电解质的电池,其示意图如下所示。放电时, 可插入
可插入 层间形成
层间形成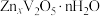 。
。
则其充电时阳极的电极反应式为
您最近一年使用:0次
2 . 西北工业大学推出一种新型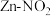 电池。该电池能有效地捕获NO2,将其转化为
电池。该电池能有效地捕获NO2,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法错误的是
电解制氨,过程如图所示。下列说法错误的是

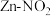 电池。该电池能有效地捕获NO2,将其转化为
电池。该电池能有效地捕获NO2,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法错误的是
电解制氨,过程如图所示。下列说法错误的是
A. 电极为电解池的阳极 电极为电解池的阳极 |
B.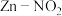 电池总反应式为: 电池总反应式为: |
C. 极区溶液的 极区溶液的 升高 升高 |
D.电路中转移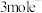 时,理论上能得到 时,理论上能得到 |
您最近一年使用:0次
名校
解题方法
3 . 某一课题组揭示了密封的碱性水系电池中的氧气循环过程,如图所示。下列叙述错误的是
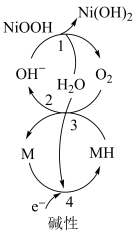

A.过程1阳极发生反应: |
B.过程1中阴极生成 后阴极区的pH升高 后阴极区的pH升高 |
| C.过程3中MH发生氧化反应 |
| D.过程4生成1 mol MH时,迁移2 mol阴离子 |
您最近一年使用:0次
2024-02-05更新
|
46次组卷
|
2卷引用:湖南省张家界市2023-2024学年高三上学期期末联考化学试题
解题方法
4 . 电化学原理在工业生产中有重要的应用,根据电化学原理完成下列问题。
(1)用 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)

①图中a极要连接电源的(填“正”或“负”)___________ 极,C口流出的物质是___________ 。
② 放电的电极反应式为
放电的电极反应式为___________ 。
(2)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①生成锂单质的电极反应式是___________ 。
②理论分析,阳极电解产物可能有 。生成
。生成 的电极反应式是
的电极反应式是___________ 。
(1)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)
①图中a极要连接电源的(填“正”或“负”)
②
 放电的电极反应式为
放电的电极反应式为(2)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①生成锂单质的电极反应式是
②理论分析,阳极电解产物可能有
 。生成
。生成 的电极反应式是
的电极反应式是
您最近一年使用:0次
解题方法
5 . I.能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是___________ (填字母)。
A.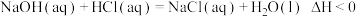
B.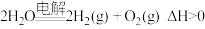
C.
若以稀硫酸为电解质溶液,则该原电池的正极反应式为___________ 。
(2)依据反应 设计原电池装置,负极材料为
设计原电池装置,负极材料为___________ 。
Ⅱ.如图所示的装置, 都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在
都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在 极附近显红色。试回答下列问题:
极附近显红色。试回答下列问题:

(3)甲装置是甲烷燃料电池(电解质溶液为 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是___________ (填“ ”或“
”或“ ”)。
”)。
(4)在乙装置中,总反应的离子方程式是___________ 。
(5)工作一段时间之后,如果丙装置中精铜电极的质量增加了 ,则甲装置中消耗的甲烷的质量为
,则甲装置中消耗的甲烷的质量为___________ g。
(6)丁装置中在通电一段时间后, 电极上发生的电极反应是
电极上发生的电极反应是___________ 。
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.
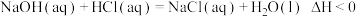
B.
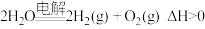
C.

若以稀硫酸为电解质溶液,则该原电池的正极反应式为
(2)依据反应
 设计原电池装置,负极材料为
设计原电池装置,负极材料为Ⅱ.如图所示的装置,
 都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在
都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在 极附近显红色。试回答下列问题:
极附近显红色。试回答下列问题:
(3)甲装置是甲烷燃料电池(电解质溶液为
 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是 ”或“
”或“ ”)。
”)。(4)在乙装置中,总反应的离子方程式是
(5)工作一段时间之后,如果丙装置中精铜电极的质量增加了
 ,则甲装置中消耗的甲烷的质量为
,则甲装置中消耗的甲烷的质量为(6)丁装置中在通电一段时间后,
 电极上发生的电极反应是
电极上发生的电极反应是
您最近一年使用:0次
6 . 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空:

(1)写出电解饱和食盐水的离子方程式_________ 。
(2)离子交换膜的作用除了能得到纯度更高的氢氧化钠溶液外,还可以______ 。
(3)精制饱和食盐水从图中_____ 位置补充,氢氧化钠溶液从图中_____ 位置流出。(选填“a”、“b”、“c”或“d”)
(4)氢气是很有前景的新能源,氢氧燃料电池的能量转化率高。下图是氢氧燃料碱性电池装置图,电解质溶液为氢氧化钾溶液,写出负极的电极反应式_______ 。

(5)氯碱工业制得的化工产品KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(6)ClO2是高效的消毒杀菌剂,消毒反应原理是高价氯还原为−1价的氯离子。现有1molClO2,其杀菌能力相当于____ L标况下Cl2 的杀菌能力(杀菌能力仅按得电子的物质的量计)。

(1)写出电解饱和食盐水的离子方程式
(2)离子交换膜的作用除了能得到纯度更高的氢氧化钠溶液外,还可以
(3)精制饱和食盐水从图中
(4)氢气是很有前景的新能源,氢氧燃料电池的能量转化率高。下图是氢氧燃料碱性电池装置图,电解质溶液为氢氧化钾溶液,写出负极的电极反应式

(5)氯碱工业制得的化工产品KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(6)ClO2是高效的消毒杀菌剂,消毒反应原理是高价氯还原为−1价的氯离子。现有1molClO2,其杀菌能力相当于
您最近一年使用:0次
名校
解题方法
7 . 从衣食住行到探索浩瀚宇宙,都有氮及其化合物的参与,但同时有毒含氮化合物的排放,也对环境产生污染。如何实现环境保护与资源利用的和谐统一,已成为我们的重要研究课题。
(1)工业上利用 和
和 可以合成
可以合成 ,
, 又可以进一步制备火箭燃料肼
又可以进一步制备火箭燃料肼 。已知:
。已知:
①
②
③
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:___________ 。
(2) 的水溶液呈弱碱性,室温下其电离常数
的水溶液呈弱碱性,室温下其电离常数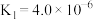 ,则
,则 的
的 水溶液
水溶液 等于
等于___________ (忽略 的二级电离和
的二级电离和 的电离,
的电离, )。
)。
(3)利用测压法在刚性密闭容器中研究 时
时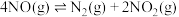 的分解反应,现将一定量的
的分解反应,现将一定量的 充入该密闭容器中,测得体系的总压强随时间的变化如表所示:
充入该密闭容器中,测得体系的总压强随时间的变化如表所示:
① 时,
时,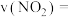
___________  。
。
② 时
时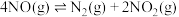 反应的平衡常数
反应的平衡常数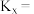
___________ ( 为以物质的量分数表示的平衡常数)。若升高温度,
为以物质的量分数表示的平衡常数)。若升高温度, 减小,则
减小,则
___________ 0(填“大于”“小于”或“等于”)。
(4)将等物质的量的 和
和 分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应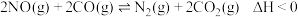 ,经过相同时间测得
,经过相同时间测得 的转化率如图所示,图中cd段转化率下降的可能原因是
的转化率如图所示,图中cd段转化率下降的可能原因是___________ 。

(5)电化学降解法可用于治理水中硝酸盐污染,电化学降解 中性溶液的原理如图所示:
中性溶液的原理如图所示:

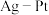 电极上的电极反应为
电极上的电极反应为___________ 。
(1)工业上利用
 和
和 可以合成
可以合成 ,
, 又可以进一步制备火箭燃料肼
又可以进一步制备火箭燃料肼 。已知:
。已知:①

②

③

写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
(2)
 的水溶液呈弱碱性,室温下其电离常数
的水溶液呈弱碱性,室温下其电离常数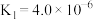 ,则
,则 的
的 水溶液
水溶液 等于
等于 的二级电离和
的二级电离和 的电离,
的电离, )。
)。(3)利用测压法在刚性密闭容器中研究
 时
时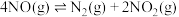 的分解反应,现将一定量的
的分解反应,现将一定量的 充入该密闭容器中,测得体系的总压强随时间的变化如表所示:
充入该密闭容器中,测得体系的总压强随时间的变化如表所示:| 反应时间/min | 0 | 10 | 20 | 30 | 40 |
压强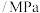 | 15.00 | 14.02 | 13.20 | 12.50 | 12.50 |
 时,
时,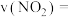
 。
。②
 时
时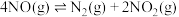 反应的平衡常数
反应的平衡常数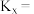
 为以物质的量分数表示的平衡常数)。若升高温度,
为以物质的量分数表示的平衡常数)。若升高温度, 减小,则
减小,则
(4)将等物质的量的
 和
和 分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应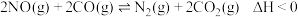 ,经过相同时间测得
,经过相同时间测得 的转化率如图所示,图中cd段转化率下降的可能原因是
的转化率如图所示,图中cd段转化率下降的可能原因是
(5)电化学降解法可用于治理水中硝酸盐污染,电化学降解
 中性溶液的原理如图所示:
中性溶液的原理如图所示:
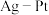 电极上的电极反应为
电极上的电极反应为
您最近一年使用:0次
8 . 化学反应与能量变化是化学家研究的永恒话题。回答下列问题:
(1)氢气是一种理想的绿色能源。在 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出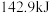 的热量。表示氢气燃烧热的热化学方程式为
的热量。表示氢气燃烧热的热化学方程式为___________ 。
(2)一定温度、催化剂条件下,向容积为2L的恒容密闭容器中充入 和
和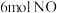 ,发生反应
,发生反应 ,起始压强为
,起始压强为 。
。 末反应达到平衡,此时容器内压强变为起始时的
末反应达到平衡,此时容器内压强变为起始时的 。
。
①判断该反应达到平衡状态的标志是___________ (填标号)。
a.CO、NO、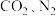 浓度之比为2:2:2:1
浓度之比为2:2:2:1
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.容器内混合气体的平均摩尔质量保持不变
e. 的生成速率和CO的生成速率相等
的生成速率和CO的生成速率相等
②CO的平均反应速率为________  。该反应的压强平衡常数
。该反应的压强平衡常数
________  (用分压代替浓度计算,分压=总压×物质的量分数。用含
(用分压代替浓度计算,分压=总压×物质的量分数。用含 的代数式表示)。
的代数式表示)。
③若在相同时间内测得NO的转化率随温度的变化曲线如图甲所示,NO的转化率在400℃~900℃之间下降由缓到急的原因是___________ 。

(3)有机物的电化学合成是目前研究的热点之一、我国学者利用双膜三室电解法合成了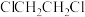 ,该方法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图乙所示。
,该方法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图乙所示。
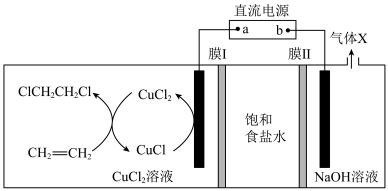
①气体X为___________ ,膜I适合选用___________ (填“阳离子”或“阴离子”)交换膜。
②若制得 ,饱和食盐水质量减小
,饱和食盐水质量减小___________ g。
(1)氢气是一种理想的绿色能源。在
 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出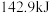 的热量。表示氢气燃烧热的热化学方程式为
的热量。表示氢气燃烧热的热化学方程式为(2)一定温度、催化剂条件下,向容积为2L的恒容密闭容器中充入
 和
和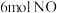 ,发生反应
,发生反应 ,起始压强为
,起始压强为 。
。 末反应达到平衡,此时容器内压强变为起始时的
末反应达到平衡,此时容器内压强变为起始时的 。
。①判断该反应达到平衡状态的标志是
a.CO、NO、
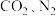 浓度之比为2:2:2:1
浓度之比为2:2:2:1b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.容器内混合气体的平均摩尔质量保持不变
e.
 的生成速率和CO的生成速率相等
的生成速率和CO的生成速率相等②CO的平均反应速率为
 。该反应的压强平衡常数
。该反应的压强平衡常数
 (用分压代替浓度计算,分压=总压×物质的量分数。用含
(用分压代替浓度计算,分压=总压×物质的量分数。用含 的代数式表示)。
的代数式表示)。③若在相同时间内测得NO的转化率随温度的变化曲线如图甲所示,NO的转化率在400℃~900℃之间下降由缓到急的原因是

(3)有机物的电化学合成是目前研究的热点之一、我国学者利用双膜三室电解法合成了
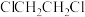 ,该方法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图乙所示。
,该方法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图乙所示。
①气体X为
②若制得
 ,饱和食盐水质量减小
,饱和食盐水质量减小
您最近一年使用:0次
名校
解题方法
9 . 实验室用含锰废料(主要成分是 )制备功能材料
)制备功能材料 的流程如图所示:
的流程如图所示:
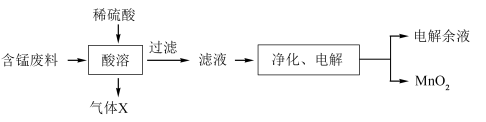
下列说法错误的是
 )制备功能材料
)制备功能材料 的流程如图所示:
的流程如图所示:
下列说法错误的是
A.气体X的中心原子为 杂化 杂化 |
| B.“电解”装置中阳极电势高于阴极电势 |
C.电解时阳极的电极反应式为: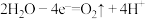 |
| D.电解余液经处理后可返回“酸溶”工序循环利用 |
您最近一年使用:0次
名校
解题方法
10 . 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知: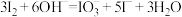 。下列说法不正确的是
。下列说法不正确的是

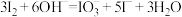 。下列说法不正确的是
。下列说法不正确的是
A.电解结束时,右侧溶液中含有 |
B.左侧发生的电极方程式: |
C.电解槽内发生反应的总化学方程式: |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式会改变 |
您最近一年使用:0次



