名校
1 . 优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
①由B生成对孟烷的反应类型是___________ 。对孟烷的一氯代物有___________ 种。
②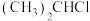 与A生成B的化学方程式是
与A生成B的化学方程式是___________ 。
③A的同系物中相对分子质量最小的物质是___________ 。
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使 的
的 溶液褪色。
溶液褪色。
①F的官能团是___________ 。
②C的结构简式是___________ 。C的属于芳香化合物且具有官能团―OH的同分异构体有___________ 种。
③反应I的化学方程式是___________ 。
(3)下列说法正确的是___________。
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与 反应放出
反应放出 。
。
反应Ⅱ的化学方程式是___________ 。

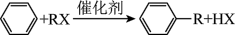 (R为烷基,X为卤原子)
(R为烷基,X为卤原子)
①由B生成对孟烷的反应类型是
②
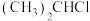 与A生成B的化学方程式是
与A生成B的化学方程式是③A的同系物中相对分子质量最小的物质是
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使
 的
的 溶液褪色。
溶液褪色。①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是___________。
| A.B可使酸性高锰酸钾溶液褪色 | B.C不存在醛类同分异构体 |
| C.D的酸性比E弱 | D.E的沸点高于对孟烷 |
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与
 反应放出
反应放出 。
。反应Ⅱ的化学方程式是
您最近半年使用:0次
解题方法
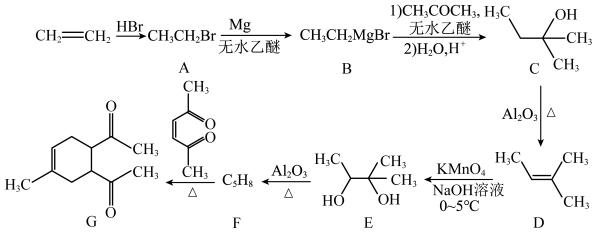
2 . 碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二酮G设计了如下合成路线:
(1)G中官能团的名称为______________ 。
(2)写出实验室制备乙烯的化学方程式:______________ 。
(3)C的化学名称为_______ 。
(4)C→D的反应类型为_______ 。
(5)在核磁共振氢谱中,化合物E有_______ 组吸收峰。
(6)C的同分异构体中,与其具有相同官能团的有_______ 种(不考虑对映异构)。
(7)D与足量酸性 溶液反应生成的有机物为
溶液反应生成的有机物为_______ 、_______ 。
(8)F的结构简式为_______ 。
(9)写出D在一定条件下发生聚合反应的化学方程式:______________ 。
(1)G中官能团的名称为
(2)写出实验室制备乙烯的化学方程式:
(3)C的化学名称为
(4)C→D的反应类型为
(5)在核磁共振氢谱中,化合物E有
(6)C的同分异构体中,与其具有相同官能团的有
(7)D与足量酸性
 溶液反应生成的有机物为
溶液反应生成的有机物为(8)F的结构简式为
(9)写出D在一定条件下发生聚合反应的化学方程式:
您最近半年使用:0次
2024-01-14更新
|
174次组卷
|
2卷引用:天津市南开区2023-2024学年高三上学期期末测试化学试题
名校
3 . Hagrmann酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):

(1)A→B为加成反应,则B的结构简式是_________ ;E→F的反应类型是_______ 。
(2)H中含有的含氧官能团名称是___________ 、___________ ;C的名称(系统命名)是___________ 。
(3)C+F→G的化学方程式是___________ 。
(4)TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基( )。TMOB的结构简式是
)。TMOB的结构简式是___________ 。
(5)下列说法正确的是___________ 。
a.A能和HCl反应得到聚氯乙烯的单体b.D和F中均含有2个 键
键
C.1molG完全燃烧生成7mol d.H能发生加成、取代反应
d.H能发生加成、取代反应

(1)A→B为加成反应,则B的结构简式是
(2)H中含有的含氧官能团名称是
(3)C+F→G的化学方程式是
(4)TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基(
 )。TMOB的结构简式是
)。TMOB的结构简式是(5)下列说法正确的是
a.A能和HCl反应得到聚氯乙烯的单体b.D和F中均含有2个
 键
键C.1molG完全燃烧生成7mol
 d.H能发生加成、取代反应
d.H能发生加成、取代反应
您最近半年使用:0次
2023高三·全国·专题练习
4 . 近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好,以煤为原料在不同条件下可合成下列物质(部分条件未标出),C是一种植物生长调节剂,用它可以催熟果实。
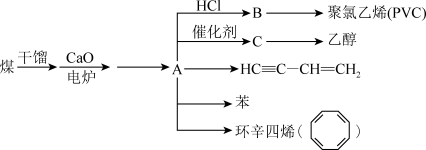
(1)A的电子式为______ ;C的空间结构为平面结构,键角约为______ 。
(2)B中所含官能团的名称是______ 。
(3)分别完全燃烧等质量的HC≡C—CH=CH2和乙炔,所需氧气的量______ (填“前者多”“后者多”或“一样多”)。
(4)苯乙烯(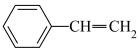 )与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式:
)与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式:______ 。
(5)异丙苯[ ]是苯的同系物。由苯与2-丙醇反应制备异丙苯属于
]是苯的同系物。由苯与2-丙醇反应制备异丙苯属于______ 反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为______ 。
(6)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是______ 。

(1)A的电子式为
(2)B中所含官能团的名称是
(3)分别完全燃烧等质量的HC≡C—CH=CH2和乙炔,所需氧气的量
(4)苯乙烯(
 )与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式:
)与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式:(5)异丙苯[
 ]是苯的同系物。由苯与2-丙醇反应制备异丙苯属于
]是苯的同系物。由苯与2-丙醇反应制备异丙苯属于(6)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是
您最近半年使用:0次
名校
5 . 研究小组以无水正己烷为溶剂,使用特定引发剂在 下,利用异丁烯(
下,利用异丁烯(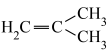 ,沸点为
,沸点为 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以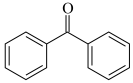 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。

①仪器A的名称为___________ 。
②用钠丝除去正己烷中微量的水,其化学方程式为___________ 。
③若下列两过程开始时,活塞 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为___________ ;当体系的颜色变为___________ 时,开始收集正己烷;收集过程中,应打开的活塞为___________ 。
(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为___________ 。
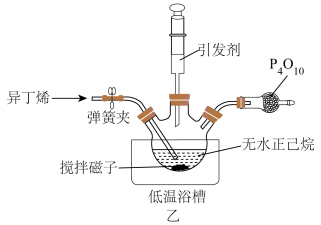
② 的作用为
的作用为___________ 。在低温浴槽中加入的最佳冷却剂为___________ (填序号)。
③将实验操作步骤补充完整:___________→d→___________→a→c→b(填序号)。________
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。
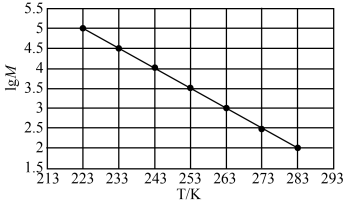
①欲合成平均相对分子质量为105的产品,则需控制反应温度t=___________ ℃。
②若控制反应温度为-30℃,则得到产品的平均聚合度为___________ (保留整数)。
 下,利用异丁烯(
下,利用异丁烯(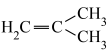 ,沸点为
,沸点为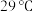 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以
 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。
①仪器A的名称为
②用钠丝除去正己烷中微量的水,其化学方程式为
③若下列两过程开始时,活塞
 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为

②
 的作用为
的作用为| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 冷却剂 | 冰水混合物 | 液氮 | 氯化钙晶体/冰 | 丙酮/干冰 | 液氨 |
| 最低温度/℃ | 0 | -195 | -55 | -78 | -33 |
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。

①欲合成平均相对分子质量为105的产品,则需控制反应温度t=
②若控制反应温度为-30℃,则得到产品的平均聚合度为
您最近半年使用:0次
解题方法
6 . 以糠醛(A)为原料合成医药中间体(J)的路线之一如下:
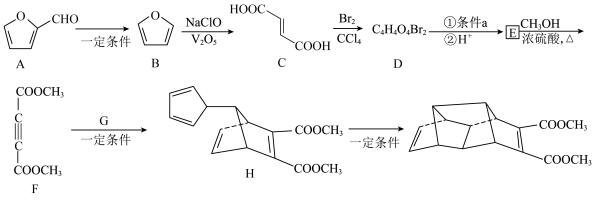
已知:①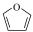 (呋喃)和苯的结构与性质较为相近,如均为平面形分子等。
(呋喃)和苯的结构与性质较为相近,如均为平面形分子等。
②
回答下列问题:
(1)关于有机物A和B,下列推测正确的是___________ (填标号)。
a.A和B互为同系物
b.A和苯甲醛的性质相似
c.B中O原子的价层电子对数为4
d.B与 易发生取代反应,难发生加成反应
易发生取代反应,难发生加成反应
(2)C俗称富马酸,化学名称为反丁烯二酸。
①富马酸分子中,碳原子的杂化轨道类型为___________ 。
②富马酸与马来酸(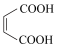 )的部分性质如下表所示:
)的部分性质如下表所示:
富马酸与马来酸熔点差别较大,其原因可能为___________ 。
(3)“条件a”是指___________ 。G的结构简式为___________ 。
(4)芯片制造过程需用到光刻胶。某光刻胶(一种高分子化合物)可由降冰片烯(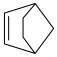 )与马来酸酐(
)与马来酸酐(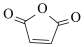 )按物质的量之比1∶1共聚而成,反应的化学方程式为
)按物质的量之比1∶1共聚而成,反应的化学方程式为___________ 。
(5)有机物M是有机物H的同分异构体,M具有以下结构和性质:
i.含有 结构且苯环上有4种不同化学环境的氢原子;
结构且苯环上有4种不同化学环境的氢原子;
ii.苯环上有三个取代基,其中两个是酚羟基;
iii.与饱和 溶液反应产生
溶液反应产生 。
。
则M的可能结构最多有___________ 种(不考虑立体异构)。M的核磁共振氢谱最少有___________ 组峰,其结构简式为___________ (任写一种)。

已知:①
 (呋喃)和苯的结构与性质较为相近,如均为平面形分子等。
(呋喃)和苯的结构与性质较为相近,如均为平面形分子等。②

回答下列问题:
(1)关于有机物A和B,下列推测正确的是
a.A和B互为同系物
b.A和苯甲醛的性质相似
c.B中O原子的价层电子对数为4
d.B与
 易发生取代反应,难发生加成反应
易发生取代反应,难发生加成反应(2)C俗称富马酸,化学名称为反丁烯二酸。
①富马酸分子中,碳原子的杂化轨道类型为
②富马酸与马来酸(
 )的部分性质如下表所示:
)的部分性质如下表所示:| 物质 | 熔点/℃ | 水溶性 |
| 富马酸 | 299 | 溶于水 |
| 马来酸 | 136 | 微溶于水 |
(3)“条件a”是指
(4)芯片制造过程需用到光刻胶。某光刻胶(一种高分子化合物)可由降冰片烯(
 )与马来酸酐(
)与马来酸酐( )按物质的量之比1∶1共聚而成,反应的化学方程式为
)按物质的量之比1∶1共聚而成,反应的化学方程式为(5)有机物M是有机物H的同分异构体,M具有以下结构和性质:
i.含有
 结构且苯环上有4种不同化学环境的氢原子;
结构且苯环上有4种不同化学环境的氢原子;ii.苯环上有三个取代基,其中两个是酚羟基;
iii.与饱和
 溶液反应产生
溶液反应产生 。
。则M的可能结构最多有
您最近半年使用:0次
7 . I.CO2的循环利用是“碳达峰、碳中和”主要措施。
(1)据VSEPR理论可知CO2中心原子价层电子对数为_______
(2)CO2与环氧丙烷 ( )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(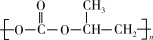 ),写出反应的化学方程式
),写出反应的化学方程式_______
II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
(3)已知298K时,相关物质的能量如图所示,则ΔH1=_______ kJ/mol,(保留三位有效数字),反应①低温_______ 自发进行(填“能”、“不能”)。

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=_______ (列出计算式即可)。(分压=物质的量分数×总压,用平衡分压代替平衡浓度计算的平衡常数即为Kp)。
(5)下列说法中不正确的是_______
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
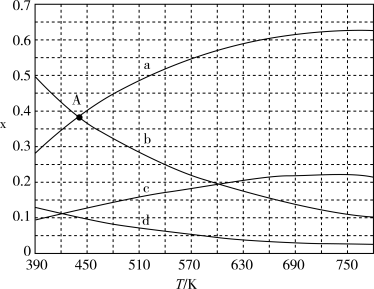
(6)理论计算表明,原料初始组成 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是_______ ,该反应△H _______ 0(填“>”、“<”或“=”)
(1)据VSEPR理论可知CO2中心原子价层电子对数为
(2)CO2与环氧丙烷 (
 )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(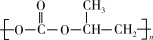 ),写出反应的化学方程式
),写出反应的化学方程式II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2(3)已知298K时,相关物质的能量如图所示,则ΔH1=

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为
 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=(5)下列说法中不正确的是_______
| A.向容器中充入He,使体系压强增大,可增大反应速率 |
| B.向容器中再充入H2可提高CO2转化率 |
C.当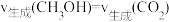 时,说明反应达到了平衡状态 时,说明反应达到了平衡状态 |
| D.选择合适的催化剂,不但可以加快反应速率,还可提高甲醇的平衡产率 |
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)(6)理论计算表明,原料初始组成
 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
您最近半年使用:0次
8 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氯乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)F原子最外层轨道表示式为_______ 。
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是_______ (填标号),判断的根据是_______ ,失去三个电子的变化图是_______ (填标号)。

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是_______ ,其形成的氢化物的沸点_______ H2S的沸点(填>、<或=),理由是_______ 。
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(5)FTFE_______ (填“有”、“没有”)固定熔沸点,其结构简式为:_______ 。
(1)F原子最外层轨道表示式为
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因
(5)FTFE
您最近半年使用:0次
名校
解题方法
9 . A、B、C、D、E、F、G是七种短周期主族元素,它们的原子序数依次增大;A元素的一种同位素原子无中子;B是形成化合物种类最多的元素;D与A同主族,且与F同周期;F元素的最外层电子数是电子总数的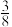 倍;D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
倍;D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
(1)B、F、G最高价氧化物对应水化物酸性强弱顺序为_______ (用化学式表示)。
(2)用电子式表示元素D与F形成的化合物的过程:_______ ,该化合物属于_______ (填“共价”或“离子”)化合物。
(3)A、C、F间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为_______ 。
(4)写出能证明G比F非金属性强的一个化学方程式:_______ 。
(5)向含有amolE的氯化物的溶液中加入含bmolD的最高价氧化物对应水化物的溶液,生成沉淀的物质的量不可能为_______ 。
①amol ②bmol ③ mol ④
mol ④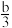 mol ⑤0mol ⑥(4a-b)mol
mol ⑤0mol ⑥(4a-b)mol
(6)有机化合物A仅由上述A、B两种元素组成,其产量可以用来衡量一个国家石油化工发展水平,E具有水果香味,H是高分子化合物。
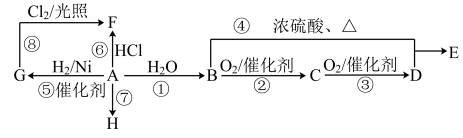
I.物质D所含官能团名称为_______ 。F的结构简式为_______ ;
II.写出②的化学方程式_______ ;其反应类型为_______ ;
III.写出⑦的化学方程式_______ ;其反应类型为_______ 。
 倍;D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
倍;D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。(1)B、F、G最高价氧化物对应水化物酸性强弱顺序为
(2)用电子式表示元素D与F形成的化合物的过程:
(3)A、C、F间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(4)写出能证明G比F非金属性强的一个化学方程式:
(5)向含有amolE的氯化物的溶液中加入含bmolD的最高价氧化物对应水化物的溶液,生成沉淀的物质的量不可能为
①amol ②bmol ③
 mol ④
mol ④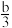 mol ⑤0mol ⑥(4a-b)mol
mol ⑤0mol ⑥(4a-b)mol(6)有机化合物A仅由上述A、B两种元素组成,其产量可以用来衡量一个国家石油化工发展水平,E具有水果香味,H是高分子化合物。

I.物质D所含官能团名称为
II.写出②的化学方程式
III.写出⑦的化学方程式
您最近半年使用:0次
2022-10-29更新
|
188次组卷
|
2卷引用:内蒙古赤峰二中2023届高三上学期10月第二次月考化学试题
10 . 乙烯是重要的化工原料,以乙烯为原料生产部分化工产品的流程如下(部分反应条件已略去):
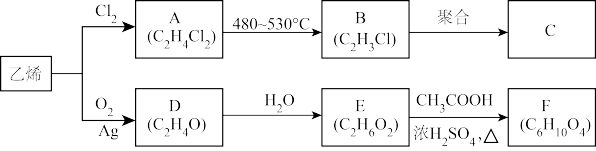
已知:E分子中含有两个羟基,且不连在同一个碳原子上。
请回答下列问题:
(1)写出实验室制乙烯的化学反应方程式_______ 。
(2)由乙烯生成A的反应类型为_______ 。
(3)C是一种常见的塑料,其化学名称为_______ 。
(4)D是环状化合物,其结构简式为_______ 。
(5)写出下列反应的化学方程式:
①A→B:_______ 。
②E→F:_______ 。

已知:E分子中含有两个羟基,且不连在同一个碳原子上。
请回答下列问题:
(1)写出实验室制乙烯的化学反应方程式
(2)由乙烯生成A的反应类型为
(3)C是一种常见的塑料,其化学名称为
(4)D是环状化合物,其结构简式为
(5)写出下列反应的化学方程式:
①A→B:
②E→F:
您最近半年使用:0次



