1 . 实验室制硝基苯的主要步骤如下:
① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。

②通过长颈漏斗上口将已配制好的混酸分多次加入烧瓶中。每加一次,必须振荡烧瓶,当反应物温度不再上升而趋下降时,才可继续加混酸。反应温度应保持在40—50℃,若超过50℃,可用冷水浴冷却烧瓶,加料完毕后,把烧瓶放在水浴上加热,约10分钟内把水浴加热到55-60℃,并保持30分钟,间歇地振荡烧瓶。
③冷却后将反应物倒入分液漏斗,静置分层,分出酸液和粗硝基苯,由于工业浓H2SO4中含有少量汞盐等杂质有催化作用,使反应产物中含有苦味酸(2,4,6-三硝基苯酚)和2,4-二硝基苯酚使粗硝基苯呈浅黄色,此外还含有间二硝基苯。已知:苦味酸与2,4-二硝基苯酚均有酸性,能与碱反应;间二硝基苯性质与硝基苯类似。请回答下列问题
(1)步骤①中长颈漏斗的作用
a_______________________ ,b _______________ 。
(2)步骤 ②中,每加入一次混酸,必须振荡烧瓶的目的_____________________ 。
(3)步骤②中,需严格控制温度的原因___________________________________ 。
(4)步骤③中,静置分层后,粗硝基苯在分液漏斗_____ 层。
(5)要将粗硝基苯中混有少量酸液、苦味酸、2,4一二硝基苯酚以及二硝基苯,除去得到纯净的硝基苯必须进行的五步操作名称为a__________ 、 b _____________ 、c _________ 、 d _____________ 、e_________ 。
① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。

②通过长颈漏斗上口将已配制好的混酸分多次加入烧瓶中。每加一次,必须振荡烧瓶,当反应物温度不再上升而趋下降时,才可继续加混酸。反应温度应保持在40—50℃,若超过50℃,可用冷水浴冷却烧瓶,加料完毕后,把烧瓶放在水浴上加热,约10分钟内把水浴加热到55-60℃,并保持30分钟,间歇地振荡烧瓶。
③冷却后将反应物倒入分液漏斗,静置分层,分出酸液和粗硝基苯,由于工业浓H2SO4中含有少量汞盐等杂质有催化作用,使反应产物中含有苦味酸(2,4,6-三硝基苯酚)和2,4-二硝基苯酚使粗硝基苯呈浅黄色,此外还含有间二硝基苯。已知:苦味酸与2,4-二硝基苯酚均有酸性,能与碱反应;间二硝基苯性质与硝基苯类似。请回答下列问题
(1)步骤①中长颈漏斗的作用
a
(2)步骤 ②中,每加入一次混酸,必须振荡烧瓶的目的
(3)步骤②中,需严格控制温度的原因
(4)步骤③中,静置分层后,粗硝基苯在分液漏斗
(5)要将粗硝基苯中混有少量酸液、苦味酸、2,4一二硝基苯酚以及二硝基苯,除去得到纯净的硝基苯必须进行的五步操作名称为a
您最近一年使用:0次
解题方法
2 . 中学实验室用如图所示装置制取少量溴苯。请填写下列空白。
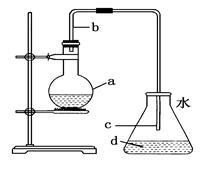
(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起_______ 的作用。
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的________ 遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有________ 生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体。这是溶解了溴的粗溴苯,可选用试剂_________ 除去。
(5)写出烧瓶a中发生反应的化学方程式:____________________________ 。

(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体。这是溶解了溴的粗溴苯,可选用试剂
(5)写出烧瓶a中发生反应的化学方程式:
您最近一年使用:0次
2016-12-09更新
|
535次组卷
|
2卷引用:2015-2016学年河北省冀州市中学高一下期末理科化学A卷
3 . 实验室常用下图所示装置制取少量溴苯,并验证其中的一种产物。

请完成下列问题:
(1)在烧瓶a中装的试剂是________ 、________ 、________ 。
(2)导管c的下口能否浸没于液面下____________ ,理由是____________ 。
(3)反应过程中在导管c的下口附近可以观察到的现象是有_______ 出现,这是由于反应生成的_______ 遇水蒸气而形成的。
(4)反应完毕后,向锥形瓶d中滴加硝酸银溶液有________ 生成,反应的离子方程式是________

请完成下列问题:
(1)在烧瓶a中装的试剂是
(2)导管c的下口能否浸没于液面下
(3)反应过程中在导管c的下口附近可以观察到的现象是有
(4)反应完毕后,向锥形瓶d中滴加硝酸银溶液有
您最近一年使用:0次
名校
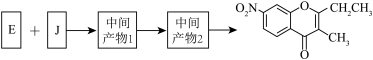
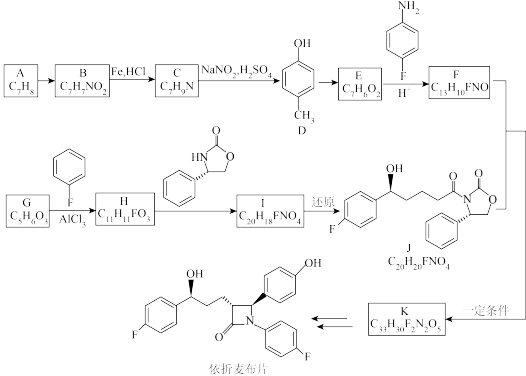
4 . 色酮类化合物K具有抗菌、降血脂等生理活性,其合成路线如下:
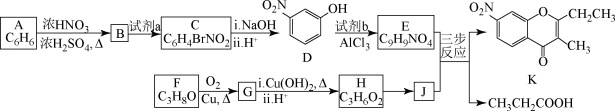
已知:
①
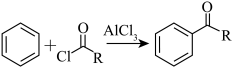 +HCl (R代表烃基)
+HCl (R代表烃基)
②
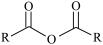 +R
+R OH
OH 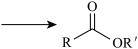 +RCOOH (R、R
+RCOOH (R、R 代表烃基)
代表烃基)
③
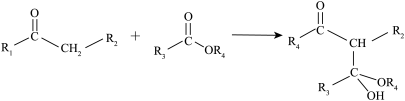
(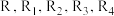 代表烃基)
代表烃基)
(1)A的结构简式是_________ ;根据系统命名法,F的名称是__________ 。
(2)B→C所需试剂a是__________ ;试剂b的结构简式是_________ 。
(3)C与足量的 反应的化学方程式为
反应的化学方程式为__________ 。
(4)G与新制 反应的化学方程式为
反应的化学方程式为__________ 。
(5)已知:①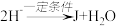 ;②J分子中有两种化学环境不同的氢以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:
;②J分子中有两种化学环境不同的氢以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:__________

已知:
①
 +HCl (R代表烃基)
+HCl (R代表烃基)②
 +R
+R OH
OH  +RCOOH (R、R
+RCOOH (R、R 代表烃基)
代表烃基) ③

(
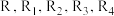 代表烃基)
代表烃基)(1)A的结构简式是
(2)B→C所需试剂a是
(3)C与足量的
 反应的化学方程式为
反应的化学方程式为(4)G与新制
 反应的化学方程式为
反应的化学方程式为(5)已知:①
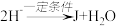 ;②J分子中有两种化学环境不同的氢以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:
;②J分子中有两种化学环境不同的氢以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:
您最近一年使用:0次
名校
解题方法
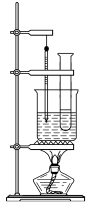
5 . 实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如图所示。回答下列问题:________________ 和____________________ 。
(2)在配制混合酸时应将____________ 加入到____________ 中去。
(3)该反应的化学方程式是__________________________ ;反应类型:________________ 。
(4)由于装置的缺陷,该实验可能会导致的不良后果是_______________________________________ 。
(5)反应完毕后,除去混合酸,所得粗产品用如下操作精制:
①蒸馏 ②水洗 ③用干燥剂干燥 ④用10%NaOH溶液洗 ⑤水洗
正确的操作顺序是______________ 。
(2)在配制混合酸时应将
(3)该反应的化学方程式是
(4)由于装置的缺陷,该实验可能会导致的不良后果是
(5)反应完毕后,除去混合酸,所得粗产品用如下操作精制:
①蒸馏 ②水洗 ③用干燥剂干燥 ④用10%NaOH溶液洗 ⑤水洗
正确的操作顺序是
| A.①②③④⑤ | B.②④⑤③① | C.④②③①⑤ | D.②④①⑤③ |
您最近一年使用:0次
2016-12-09更新
|
768次组卷
|
4卷引用:2014-2015学年广东省揭阳市一中高一下第二次阶段考试化学试卷
2014-2015学年广东省揭阳市一中高一下第二次阶段考试化学试卷(已下线)2018年5月7日 苯的结构与性质——《每日一题》2017-2018学年高一化学人教必修2(已下线)2019年4月29日 《每日一题》必修2-苯的结构与性质四川省绵阳南山中学实验学校2023-2024学年高二下学期期中考试化学试题
名校
6 . 依折麦布片是一种新型高效的调脂药,其合成路线如下,回答以下问题:_______ ,C的结构简式:_______ 。
(2)D反应成E实际需经过多步反应,原因是_______ 。
(3)G到H的化学方程式:_______ ,比H少2个碳原子的同系物L,其同分异构体符合下列要求的有_______ (不考虑立体异构)种。
①F原子直接连苯环,除苯环外无其他环状结构。②与KOH溶液反应,最多消耗5mol KOH。③苯环上只有两个支链。
其中核磁共振氢谱有四组峰,峰面积比2∶2∶1∶1∶1的有机物的结构简式为_______ 。
(4)F和J生成K的反应类型为_______ 。
(5)信息(3)的反应机理如下,有关说法正确的是_______(填字母)。
已知:Ⅰ.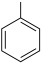

 。
。
Ⅱ.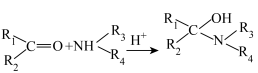

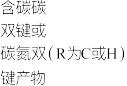 。
。
Ⅲ.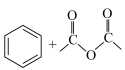
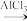
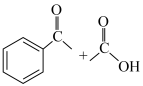 。
。
(2)D反应成E实际需经过多步反应,原因是
(3)G到H的化学方程式:
①F原子直接连苯环,除苯环外无其他环状结构。②与KOH溶液反应,最多消耗5mol KOH。③苯环上只有两个支链。
其中核磁共振氢谱有四组峰,峰面积比2∶2∶1∶1∶1的有机物的结构简式为
(4)F和J生成K的反应类型为
(5)信息(3)的反应机理如下,有关说法正确的是_______(填字母)。

A.反应①中配位键的生成,导致O、Al原子上电子云分布发生变化,有利于②反应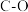 键的异裂 键的异裂 |
| B.整个反应过程碳原子杂化方式有两种 |
C.③反应后分子中存在离域π键 |
| D.最终产物苯乙酮相对于苯更易发生此类反应 |
您最近一年使用:0次
13-14高二下·甘肃张掖·期末
解题方法
7 . 化合物E(HOCH2CH2Cl)和F[HN(CH2CH3)2]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知: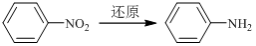 )
)
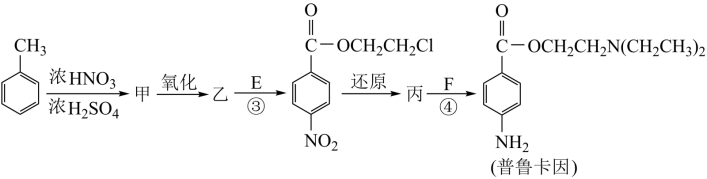
(1)甲的结构简式是_______ 。由甲苯生成甲的反应类型是_______ 。
(2)乙中有两种含氧官能团,反应③的化学方程式是:_______
(3)丙中官能团的名称是_______ 。
(4)普鲁卡因有两种水解产物丁和戊。
①戊与甲互为同分异构体,戊的结构简式是_______ 。
②戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是_______ 。
 )
)
(1)甲的结构简式是
(2)乙中有两种含氧官能团,反应③的化学方程式是:
(3)丙中官能团的名称是
(4)普鲁卡因有两种水解产物丁和戊。
①戊与甲互为同分异构体,戊的结构简式是
②戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是
您最近一年使用:0次
9-10高一下·北京·期末
解题方法
8 . 如图所示,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答下列问题:
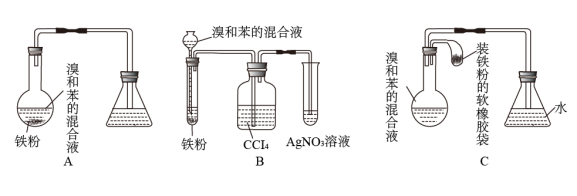
(1)写出三个装置中共同发生反应的化学方程式:___________________
(2)装置A和C均采用了长玻璃导管,其作用是_____________________________
(3)按装置B、C装好仪器及药品后,要使反应开始,应对装置B进行的操作是_________ ,应对装置C进行的操作是 _____________________ 。
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作,装置A中这一问题在实验中造成的后果是________________________ 。
(5)B中采用了洗气瓶吸收装置,反应后洗气瓶中可能出现的现象是_______

(1)写出三个装置中共同发生反应的化学方程式:
(2)装置A和C均采用了长玻璃导管,其作用是
(3)按装置B、C装好仪器及药品后,要使反应开始,应对装置B进行的操作是
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作,装置A中这一问题在实验中造成的后果是
(5)B中采用了洗气瓶吸收装置,反应后洗气瓶中可能出现的现象是
您最近一年使用:0次
13-14高三上·上海奉贤·期末
9 . 化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空。
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是_____ ,_________ ,________ ,______ 。
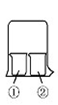
(2)用下图装置:废铜屑制硝酸铜,反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____ (填写化学式)。
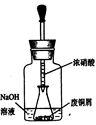
(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题。
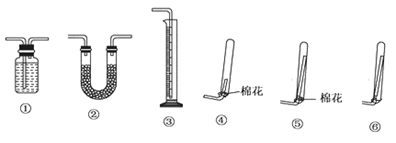
①若要测定生成的NH3的体积,则必须选择的装置是______ (填装置序号),装置中所盛试剂应具有的性质是_______ ,收集干燥的NH3,收集装置应选择(填装置序号)_______ ,理由是__________ 。
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1—10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式_______ 。
(4)下图是苯与溴发生反应并进行产物检验的反应装置:
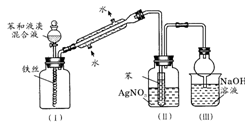
实验装置中的冷凝管“左低右高”的放置目的是____________ ,整套实验装置中能防止倒吸的装置是_____ (填装置序号)。
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫。
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠。
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠。
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎。
②将研钵中的样品露置在空气中两天。
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡。
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少。
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)________ 。
(6)如果要验证③是否成立的实验方法是______________________ 。
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是

| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |

(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题。

①若要测定生成的NH3的体积,则必须选择的装置是
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1—10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式
(4)下图是苯与溴发生反应并进行产物检验的反应装置:

实验装置中的冷凝管“左低右高”的放置目的是
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫。
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠。
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠。
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎。
②将研钵中的样品露置在空气中两天。
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡。
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少。
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)
(6)如果要验证③是否成立的实验方法是
您最近一年使用:0次
名校
解题方法
10 . 实验室制备硝基苯的反应原理和实验装置如下:
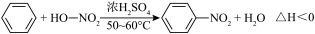
存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯,有关数据如表:
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把17.73 mL(15.6 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60 ℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~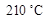 馏分,得到纯硝酸基苯18.45 g。回答下列问题:
馏分,得到纯硝酸基苯18.45 g。回答下列问题:
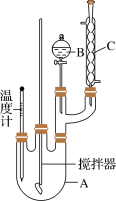
(1)装置B的名称是________ ,装置C的作用是____________________ ;
(2)配制混合液时,________ (填“能”或“不能”)将浓硝酸加入浓硫酸中,说明理由:________________________________________________________________________ ;
(3)为了使反应在50~60 ℃下进行,常用的方法是____________ ;
(4)在洗涤操作中,第二次水洗的作用是______________________________________ ;
(5)本实验所得到的硝基苯产率是_________________ (保留两位有效数字)。

存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯,有关数据如表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/ g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把17.73 mL(15.6 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60 ℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~
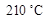 馏分,得到纯硝酸基苯18.45 g。回答下列问题:
馏分,得到纯硝酸基苯18.45 g。回答下列问题:
(1)装置B的名称是
(2)配制混合液时,
(3)为了使反应在50~60 ℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
(5)本实验所得到的硝基苯产率是
您最近一年使用:0次
2016-12-09更新
|
684次组卷
|
2卷引用:2015-2016学年湖北省孝感高中高一下期末化学试卷



