1 . 实验室制乙酸乙酯的主要装置如图中A所示,主要步骤如下:9.实验室制取乙酸正丁酯(沸点:126℃,反应温度115-120℃)的装置如图所示,将冰醋酸(沸点118℃)、正丁醇(沸点118℃)、浓硫酸混合物装入三颈烧瓶中加热,最后将分水器中的酯层与烧瓶中反应物混合后分离提纯得到产品,对该实验的说法错误的是


| A.使用分水器可以提高乙酸正丁酯的产率 |
| B.分离提纯时的洗涤操作在分液漏斗中进行 |
| C.反应开始后发现A装置中没加碎瓷片,应该立即补加以防暴沸 |
| D.用饱和Na2CO3溶液可洗去混合液中的酸性物质 |
您最近半年使用:0次
名校
解题方法
2 . 下列实验操作、现象以及得到的实验结论都正确的是
| 选项 | 操作 | 现象 | 实验结论 |
| A | 将稀盐酸逐滴滴加到盛有饱和 溶液的试管中 溶液的试管中 | 有气泡冒出,溶液出浑浊 |  在酸性条件下不稳定,反应生成 在酸性条件下不稳定,反应生成 和S 和S |
| B | 在淀粉和 的混合溶液中滴加过量氯水 的混合溶液中滴加过量氯水 | 溶液蓝色褪去 | 氯气具有漂白性 |
| C | 向烧瓶中依次加入浓硫酸、乙醇和乙酸,再加入碎瓷片,连接好装置并加热 | 饱和碳酸钠溶液液面上出现无色油状液体,并有水果香味 | 反应生成了乙酸乙酯 |
| D | 将绿豆粒大小的钠投入硫酸铜溶液中 | 钠浮在液面上,快速游动,发出嘶嘶响声,溶液中有红色物质析出 | 钠具有强还原性,可置换出铜 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-07更新
|
481次组卷
|
3卷引用:湖南省长沙市长郡中学2023-2024学年高三上学期月考(四)化学试题
2023高三·全国·专题练习
3 . 制备乙酸乙酯时,向浓H2SO4中缓慢加入乙醇和冰醋酸。(___________)
您最近半年使用:0次
4 . 掌握化学实验技能是进行科学探究的基本保证。下列有关装置选择、操作、原理及现象描述等均正确的是
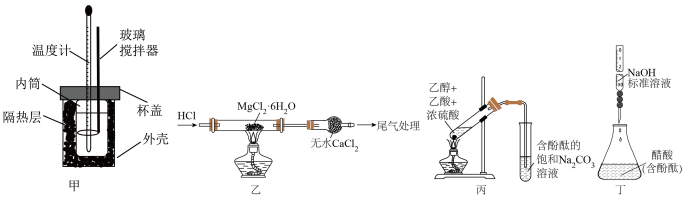

| A.用甲装置进行中和反应反应热的测定实验时,NaOH要缓慢倒入稀硫酸中 |
| B.用乙装置制备无水氯化镁,可以在HCl气流中蒸干,也可以直接在空气中蒸干 |
| C.用丙装置制备乙酸乙酯,右侧试管中出现分层,下层呈红色,上层为无色油状液体 |
| D.用丁装置测定未知醋酸溶液的浓度,锥形瓶应用待测液润洗 |
您最近半年使用:0次
名校
解题方法
5 . 下列说法不正确 的是
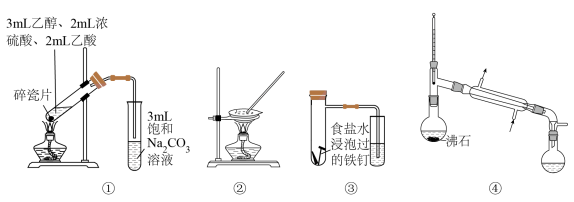

| A.图①装置可用于制备乙酸乙酯 |
B.图②装置可由 制取无水FeCl3固体 制取无水FeCl3固体 |
| C.图③可模拟钢铁的吸氧腐蚀 |
| D.图④可由海水制取蒸馏水 |
您最近半年使用:0次
名校
解题方法
6 . 山西老陈醋素有“天下第一醋”的盛誉,以色、香、醇、浓、酸五大特征著称于世。酿醋过程中的熏醅使醋增色、增香、增脂,其原理是乙醇与乙酸发生了反应。在实验室中用下列装置模拟该反应的原理:
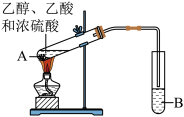
(1)A试管中碎瓷片的作用是___________ ,B试管中盛装的是___________ 。
(2)A试管中发生反应的化学方程式是___________ 。
(3)反应类型是___________ ,该反应中浓硫酸的作用是___________ 。
(4)反应结束后,收集B试管的油状液体,从油状液体中分离出乙酸乙酯、乙酸和乙醇,操作流程如下:

已知试剂a为饱和Na2CO3溶液,分离方法(Ⅰ)是___________ ,分离方法(Ⅱ)是___________ ,试剂b为___________ 。

(1)A试管中碎瓷片的作用是
(2)A试管中发生反应的化学方程式是
(3)反应类型是
(4)反应结束后,收集B试管的油状液体,从油状液体中分离出乙酸乙酯、乙酸和乙醇,操作流程如下:

已知试剂a为饱和Na2CO3溶液,分离方法(Ⅰ)是
您最近半年使用:0次
7 . 有机化合物A是基本的化工原料,在有机化工中具有举足轻重的作用,以A为基本原料制备E的合成路线如图所示。
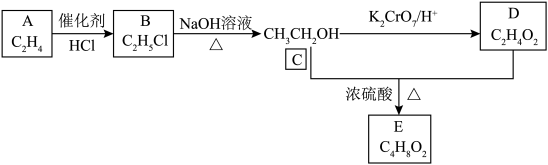
回答下列问题:
(1)A的官能团名称是_______ ,以A为单体合成的高分子化合物的链节是_______ 。
(2)A生成B的反应类型是_______ 。
(3)写出C在催化剂铜和加热条件下生成乙醛的化学方程式:_______ 。
(4)实验室中利用C、D制备E的装置如图所示:
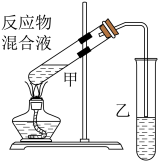
其中试管乙中盛有的试剂为_______ (填字母,下同),为除去生成物E中含有的C、D两种杂质,需采用_______ 对混合物进行洗涤,洗涤后再_______ (填操作名称),从而得到较为纯净的E。
a.饱和食盐水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和NaOH溶液
溶液 d.饱和NaOH溶液
(5)X为A的同系物,且与E含有相同的碳原子数,则X的同分异构体有_______ 种(不考虑立体异构),写出含两个甲基的同分异构体的结构简式:_______ (填一种)。

回答下列问题:
(1)A的官能团名称是
(2)A生成B的反应类型是
(3)写出C在催化剂铜和加热条件下生成乙醛的化学方程式:
(4)实验室中利用C、D制备E的装置如图所示:

其中试管乙中盛有的试剂为
a.饱和食盐水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和NaOH溶液
溶液 d.饱和NaOH溶液(5)X为A的同系物,且与E含有相同的碳原子数,则X的同分异构体有
您最近半年使用:0次
8 . 下列有关物质的制备说法错误的是
| A.“海水提溴”时通Cl2前先将苦卤酸化 |
| B.工业制取漂白粉时应将氯气通入石灰水 |
| C.实验室制备硝基苯时应使用温度计、酒精灯 |
| D.实验室大量制备并纯化乙酸乙酯过程中用饱和CaCl2溶液除乙醇 |
您最近半年使用:0次
名校
9 . 乙酸乙酯是常用的化工原料和有机溶剂,某实验小组在实验室制取乙酸乙酯并进行提纯(已知: 可与乙醇形成
可与乙醇形成 难溶物)。
难溶物)。
(一)制备过程
在A试管中加入 无水乙醇,然后边振荡试管边慢慢加入
无水乙醇,然后边振荡试管边慢慢加入 浓硫酸和
浓硫酸和 冰醋酸,再加入几片碎瓷片。如下图连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和
冰醋酸,再加入几片碎瓷片。如下图连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和 溶液的液面上。
溶液的液面上。
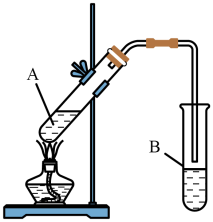
(1)在试管中加入浓硫酸后,应___________ 后再加入冰醋酸。
(2)饱和碳酸钠溶液的主要作用是___________ 、溶解乙醇、___________ 、___________ 。
(3)若预先向饱和 溶液中加入2滴酚酞溶液,实验过程中红色的液面上逐渐出现一层无色液体。实验结束后,振荡B试管,静置,观察到有气泡放出,静置后分层,上下两层均为无色透明液体。分析溶液红色褪去的主要原因,实验小组提出如下假设,并设计实验验证。
溶液中加入2滴酚酞溶液,实验过程中红色的液面上逐渐出现一层无色液体。实验结束后,振荡B试管,静置,观察到有气泡放出,静置后分层,上下两层均为无色透明液体。分析溶液红色褪去的主要原因,实验小组提出如下假设,并设计实验验证。
假设一:碳酸钠与挥发出的乙酸反应。
假设二:酚酞由水层转移到有机层。
由以上现象可以得出结论___________ (填“假设一正确”,“假设二正确”或“假设一、二均正确”)。
(二)提纯过程
将B试管中的混合液转入分液漏斗中,振荡,静置分层后分去水层,有机层依次用 饱和食盐水、
饱和食盐水、 饱和氯化钙溶液和
饱和氯化钙溶液和 蒸馏水洗涤。再将有机层用适量的无水硫酸镁干燥。将干燥后的乙酸乙酯滤入如图所示
蒸馏水洗涤。再将有机层用适量的无水硫酸镁干燥。将干燥后的乙酸乙酯滤入如图所示 蒸馏瓶中,蒸馏,收集
蒸馏瓶中,蒸馏,收集 馏分。
馏分。
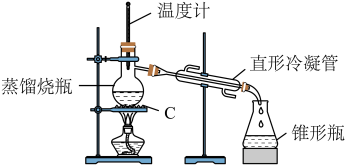
(4)仪器C的名称是___________ 。
(5)饱和氯化钙溶液的作用是___________ ;在用饱和氯化钙溶液洗涤之前,先用饱和氯化钠水溶液洗涤,目的是___________ 。
(6)蒸馏共收集到乙酸乙酯 ,则本实验的产率是
,则本实验的产率是___________ (产率指的是某种生成物的实际产量与理论产量的比值)。
 可与乙醇形成
可与乙醇形成 难溶物)。
难溶物)。(一)制备过程
在A试管中加入
 无水乙醇,然后边振荡试管边慢慢加入
无水乙醇,然后边振荡试管边慢慢加入 浓硫酸和
浓硫酸和 冰醋酸,再加入几片碎瓷片。如下图连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和
冰醋酸,再加入几片碎瓷片。如下图连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和 溶液的液面上。
溶液的液面上。
(1)在试管中加入浓硫酸后,应
(2)饱和碳酸钠溶液的主要作用是
(3)若预先向饱和
 溶液中加入2滴酚酞溶液,实验过程中红色的液面上逐渐出现一层无色液体。实验结束后,振荡B试管,静置,观察到有气泡放出,静置后分层,上下两层均为无色透明液体。分析溶液红色褪去的主要原因,实验小组提出如下假设,并设计实验验证。
溶液中加入2滴酚酞溶液,实验过程中红色的液面上逐渐出现一层无色液体。实验结束后,振荡B试管,静置,观察到有气泡放出,静置后分层,上下两层均为无色透明液体。分析溶液红色褪去的主要原因,实验小组提出如下假设,并设计实验验证。假设一:碳酸钠与挥发出的乙酸反应。
假设二:酚酞由水层转移到有机层。
| 序号 | 实验操作 | 实验现象 |
| 1 | 用胶头滴管吸取少许上层液体于试管中,加入几滴氢氧化钠溶液,振荡 | 溶液变红 |
| 2 | 将吸有酚酞溶液的长胶头滴管穿过有机层向无色的水层中滴加酚酞溶液 | 溶液变红 |
(二)提纯过程
将B试管中的混合液转入分液漏斗中,振荡,静置分层后分去水层,有机层依次用
 饱和食盐水、
饱和食盐水、 饱和氯化钙溶液和
饱和氯化钙溶液和 蒸馏水洗涤。再将有机层用适量的无水硫酸镁干燥。将干燥后的乙酸乙酯滤入如图所示
蒸馏水洗涤。再将有机层用适量的无水硫酸镁干燥。将干燥后的乙酸乙酯滤入如图所示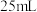 蒸馏瓶中,蒸馏,收集
蒸馏瓶中,蒸馏,收集 馏分。
馏分。
(4)仪器C的名称是
(5)饱和氯化钙溶液的作用是
(6)蒸馏共收集到乙酸乙酯
 ,则本实验的产率是
,则本实验的产率是
您最近半年使用:0次
2023-07-19更新
|
178次组卷
|
2卷引用:辽宁省大连市2022-2023学年高一下学期期末考试化学试题
10 . 学习小组进行实验研究乙醇的化学性质。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(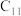 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。
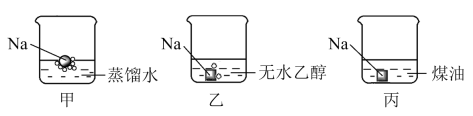
①对比乙、丙的现象,说明 与
与 反应时断裂
反应时断裂___________ (填序号)。
a.C-H键 b.O-H键 c.C-C键
②乙中反应的化学方程式是___________ 。
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。
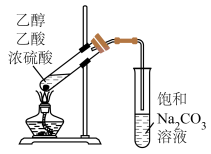
①饱和 溶液的作用是
溶液的作用是___________ 。
②关于该实验的说法正确的是___________ (填序号)。
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
(3)发生化学反应时,物质变化的同时常常伴随有能量变化。将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为___________ 能。
(4)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。
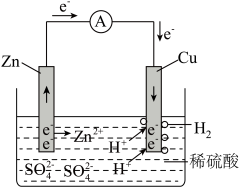
①证实化学能转化为电能的现象是___________ 。
②解释Cu片表面产生气泡的原因:___________ 。
(5)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
当 和
和 化合生成2
化合生成2
 时,放出
时,放出___________  的能量。
的能量。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(
 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。
①对比乙、丙的现象,说明
 与
与 反应时断裂
反应时断裂a.C-H键 b.O-H键 c.C-C键
②乙中反应的化学方程式是
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。

①饱和
 溶液的作用是
溶液的作用是②关于该实验的说法正确的是
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
(3)发生化学反应时,物质变化的同时常常伴随有能量变化。将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(4)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是
②解释Cu片表面产生气泡的原因:
(5)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O-O | H-O |
| 键能/kJ·mol | 436 | 498 | 463 |
 和
和 化合生成2
化合生成2
 时,放出
时,放出 的能量。
的能量。
您最近半年使用:0次



