1 . 餐厨垃圾在酶的作用下可获得乙醇,进一步反应可制备有机物C和高分子材料G,转化关系如下:
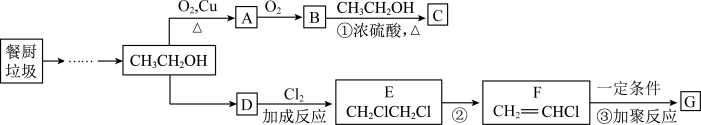
(1)乙醇的官能团的名称是___________ ,写出A的结构简式___________ ,请列举D物质的一种用途___________ ;
(2)反应①的反应类型是___________ ,化学方程式为___________ ;
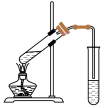
(3)实验室制备C物质的装置如图,试管a中加入三种液体试剂的顺序为___________ ,实验结束时试管 中观察到
中观察到___________ 、滴加酚酞的饱和 溶液红色变浅,并可以闻到香味;
溶液红色变浅,并可以闻到香味;

(4)下列说法中,不正确的是___________ ;
a.D、E、F均属于烃
b.甲烷中含有D物质,不能用酸性高锰酸钾溶液除去
c.CH3CH2OH与CH3OCH3互为同分异构体
d.F、G均能使溴水发生化学反应而褪色
(5)请写出反应③的化学方程式___________ 。

(1)乙醇的官能团的名称是
(2)反应①的反应类型是
(3)实验室制备C物质的装置如图,试管a中加入三种液体试剂的顺序为
 中观察到
中观察到 溶液红色变浅,并可以闻到香味;
溶液红色变浅,并可以闻到香味;
(4)下列说法中,不正确的是
a.D、E、F均属于烃
b.甲烷中含有D物质,不能用酸性高锰酸钾溶液除去
c.CH3CH2OH与CH3OCH3互为同分异构体
d.F、G均能使溴水发生化学反应而褪色
(5)请写出反应③的化学方程式
您最近一年使用:0次
2023-07-17更新
|
126次组卷
|
2卷引用:广西百色市2022-2023学年高一下学期期末考试化学试题
解题方法
2 . A、B、C、D、E、F、G均为有机物,其中A常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如图转化关系。已知醛基在氧气中易氧化成羧基,请回答下列问题:
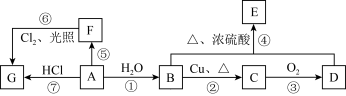
(1)A的结构简式是___________ ,B中官能团的名称为___________ 。
(2)在F的同系物中最简单的有机物的空间构型为___________ 。
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的物质的结构简式___________ 。
(4)写出④反应的化学方程式:___________ 。
(5)实验室由反应④制备E可以采用如图所示装置。烧瓶中依次加入B、浓硫酸、D和碎瓷片,右边试管中加入的是___________ 溶液;装置中通蒸气的导管不能插入溶液中,目的是___________ 。

(1)A的结构简式是
(2)在F的同系物中最简单的有机物的空间构型为
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的物质的结构简式
(4)写出④反应的化学方程式:
(5)实验室由反应④制备E可以采用如图所示装置。烧瓶中依次加入B、浓硫酸、D和碎瓷片,右边试管中加入的是

您最近一年使用:0次
解题方法
3 . 乙酸乙酯是应用最广的脂肪酸酯之一,是一种快干性溶剂,具有优异的溶解能力,是极好的工业溶剂,也可用于柱层析的洗脱剂。请回答相关问题:
Ⅰ.合成:
工业上利用有机化合物A合成乙酸乙酯以生产食用香料,图1为乙酸乙酯的常见合成路线(部分条件略去)。
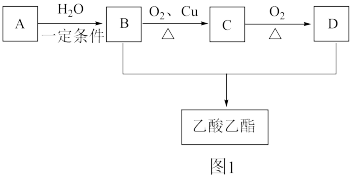
(1)已知A的产量是衡量一个国家石油化工发展水平的重要标志,则A的结构简式为_______ 。
(2)写出B和D生成乙酸乙酯的化学方程式_______ ,C中官能团的名称为_______ 。
Ⅱ.制备:
某兴趣小组以无水乙醇和冰醋酸为原料制备一定量的乙酸乙酯,实验装置如图2。

(3)饱和碳酸钠溶液的作用是_______ 。
(4)b装置还可选择图3中的_______ (填序号)。

(5)实验完毕后,将b装置充分振荡,静置后,溶液分为两层,乙酸乙酯在_______ 层,常用_______ 操作将两层液体分离。
Ⅲ.应用:
已知乙酰乙酸乙酯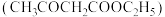 为制备抗癌药“凡诺利品”的中间体(“中间体”是合成某目标产物过程中不可或缺的中间产物,通过“中间体”的多步反应转化最终得到目标产物)。以乙酸乙酯和乙醇钠为原料制备乙酰乙酸乙酯的反应方程式如下:
为制备抗癌药“凡诺利品”的中间体(“中间体”是合成某目标产物过程中不可或缺的中间产物,通过“中间体”的多步反应转化最终得到目标产物)。以乙酸乙酯和乙醇钠为原料制备乙酰乙酸乙酯的反应方程式如下:
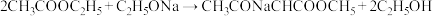

(6)若用丙酸乙酯和乙醇钠为原料制备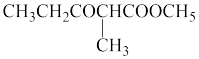 ,则该制备过程中的中间体的结构简式为
,则该制备过程中的中间体的结构简式为_______ 。
Ⅰ.合成:
工业上利用有机化合物A合成乙酸乙酯以生产食用香料,图1为乙酸乙酯的常见合成路线(部分条件略去)。

(1)已知A的产量是衡量一个国家石油化工发展水平的重要标志,则A的结构简式为
(2)写出B和D生成乙酸乙酯的化学方程式
Ⅱ.制备:
某兴趣小组以无水乙醇和冰醋酸为原料制备一定量的乙酸乙酯,实验装置如图2。

(3)饱和碳酸钠溶液的作用是
(4)b装置还可选择图3中的

(5)实验完毕后,将b装置充分振荡,静置后,溶液分为两层,乙酸乙酯在
Ⅲ.应用:
已知乙酰乙酸乙酯
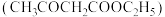 为制备抗癌药“凡诺利品”的中间体(“中间体”是合成某目标产物过程中不可或缺的中间产物,通过“中间体”的多步反应转化最终得到目标产物)。以乙酸乙酯和乙醇钠为原料制备乙酰乙酸乙酯的反应方程式如下:
为制备抗癌药“凡诺利品”的中间体(“中间体”是合成某目标产物过程中不可或缺的中间产物,通过“中间体”的多步反应转化最终得到目标产物)。以乙酸乙酯和乙醇钠为原料制备乙酰乙酸乙酯的反应方程式如下: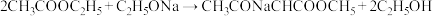

(6)若用丙酸乙酯和乙醇钠为原料制备
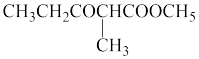 ,则该制备过程中的中间体的结构简式为
,则该制备过程中的中间体的结构简式为
您最近一年使用:0次
解题方法
4 . 阿司匹林是生活中常用的非处方药(OTC),具有解热镇痛作用。一种合成路线“片段”如下:

回答下列问题:
(1)长期服用阿司匹林易引起酸中毒,如果酸中毒可及时服用下列___________溶液(填字母)。
(2)阿司匹林中含有的官能团有___________ (填名称)。
(3)C→D的试剂、条件是___________ 。E制各水杨酸的反应类型是___________ ,副产物的结构简式是___________ 。
(4)写出用水杨酸制备阿司匹林的化学方程式:___________ 。
(5)A→B反应的副产物采用下列装置吸收并制备工业“三酸两碱”中的一种,适宜的装置是___________ (填字母)。

(6)有机物A中苯环上的一溴代物有___________ 种。

回答下列问题:
(1)长期服用阿司匹林易引起酸中毒,如果酸中毒可及时服用下列___________溶液(填字母)。
| A.生理盐水 | B.葡萄糖水 | C.小苏打水 | D.双氧水 |
(3)C→D的试剂、条件是
(4)写出用水杨酸制备阿司匹林的化学方程式:
(5)A→B反应的副产物采用下列装置吸收并制备工业“三酸两碱”中的一种,适宜的装置是

(6)有机物A中苯环上的一溴代物有
您最近一年使用:0次
解题方法
5 . 电化学合成在有机合成领域发挥着重要作用。某实验小组利用电化学方法氧化烯烃制备环氧化物(其中-R基团代表烷烃基),装置如下图所示。下列叙述正确的是


| A.当Pt电极上产生11.2L氢气时,理论上转移1mol电子 |
B.该装置中负极区的化学反应方程式为:Br2+H2O+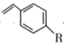  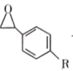 +2Br-+2H+ +2Br-+2H+ |
| C.Pt电极上发生氧化反应 |
D.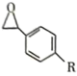 和 和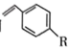 分子中(除-R外)都含有手性碳 分子中(除-R外)都含有手性碳 |
您最近一年使用:0次
6 . 乙烯的年产量是衡量—个国采石油化工发展水平的重要标志之一、以乙烯为原料合成部分化工产品的流程如下(部分反应条件已略去)
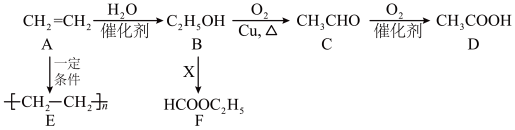
(1)B→F的反应类型为___________ ,C中官能团的名称为___________ 。
(2)物质x的结构简式为___________ 。
(3)D的一种同分异构体属于酯类,写出该同分异构体的结构简式___________ 。
(4)苯乙烯在一定条件下也能发生加聚反应,写出该反应的化学方程式:___________ 。
(5)某兴趣小组制备一定量的乙酸乙酯,装置如下图所示。
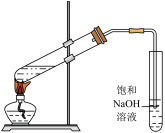
①制备乙酸乙酯的化学方程式为___________ 。
②图中的错误之处有___________ 。

(1)B→F的反应类型为
(2)物质x的结构简式为
(3)D的一种同分异构体属于酯类,写出该同分异构体的结构简式
(4)苯乙烯在一定条件下也能发生加聚反应,写出该反应的化学方程式:
(5)某兴趣小组制备一定量的乙酸乙酯,装置如下图所示。

①制备乙酸乙酯的化学方程式为
②图中的错误之处有
您最近一年使用:0次
7 . 在实验室利用下列装置,可制备某些气体并验证其化学性质。
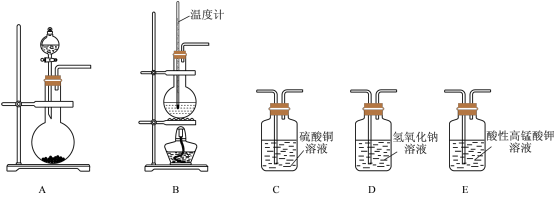
(1)填空,完成下列表格:
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是___________ 。
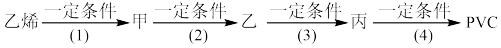
(3)下列说法正确的是___________。
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。___________ 、___________ 。
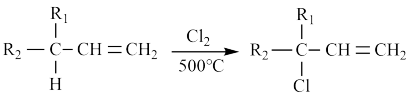


(1)填空,完成下列表格:
| 序号 | 气体 | 装置连接顺(填字母) | 制备反应的化学方程式 |
| ① | 乙烯 | B→D→E | |
| ② | 乙炔 |  |
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是
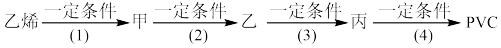
(3)下列说法正确的是___________。
| A.乙烯可以作为植物生长调节剂 | B.PVC不能使酸性高锰酸钾溶液褪色 |
| C.PVC中的官能团是碳碳双键和氯原子 | D.PVC可用作食品包装袋 |
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。
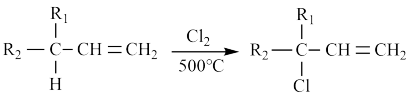

您最近一年使用:0次
名校
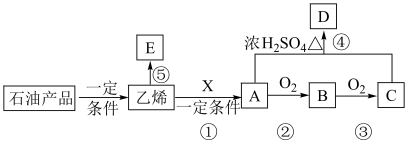
8 . 乙烯工业是石油化工产业的核心,在国民经济中占有重要的地位。生活中,乙烯也是一种常见的水果催熟剂。乙烯能发生如下图所示的化学变化,其中化合物D是一种具有香味的液体,物质E是常见的高分子材料。
(1)乙烯的结构式为___________ ,其中π键与σ键的数目比为___________ 。
(2)在水果箱中放入一些用0.2%的高锰酸钾溶液浸泡过的纸,封严水果箱,能延长水果的保质期,说明其中的化学原理_______ 。
(3)反应①中无机物X为___________ ,反应①的类型为___________ 反应。
(4)反应②的方程式为___________ 。
(5)以下关于物质E的表述,正确的是___________。(复选)
下图是实验室制备D的装置示意图:

(6)从反应后的混合物中分离得到D,应选择的分离方法为___________。
(7)物质D的同分异构体(不包含物质D)中属于酯类的数目有___________种。
(8)为了提高C的转化率,采取的措施有___________ 、___________ (写两条)。

(1)乙烯的结构式为
(2)在水果箱中放入一些用0.2%的高锰酸钾溶液浸泡过的纸,封严水果箱,能延长水果的保质期,说明其中的化学原理
(3)反应①中无机物X为
(4)反应②的方程式为
(5)以下关于物质E的表述,正确的是___________。(复选)
| A.物质E为纯净物 |
| B.物质E不能使溴水褪色 |
| C.物质E中所有碳原子共平面 |
D.反应⑤为熵减过程,却能自发进行,可知该反应的 |
下图是实验室制备D的装置示意图:

(6)从反应后的混合物中分离得到D,应选择的分离方法为___________。
| A.过滤 | B.渗析 | C.分液 | D.蒸馏 |
(7)物质D的同分异构体(不包含物质D)中属于酯类的数目有___________种。
| A.1 | B.2 | C.3 | D.4 |
(8)为了提高C的转化率,采取的措施有
您最近一年使用:0次
名校
解题方法
9 . I.某天然油脂的分子式为C57H106O6 ,1 mol该油脂完全水解可得到1 mol甘油、1 mol脂肪酸X、2 mol脂肪酸Y。经测定X的相对分子质量为284,原子个数比C∶H∶O=9∶18∶1。
(1)下列物质在一定条件下能与X发生反应的有_______ 。
A.氢气 B.乙醇 C.溴水 D.烧碱溶液 E.高锰酸钾酸性溶液
(2)Y的分子式为_______ 。
II.某同学在实验室利用橄榄油与甲醇制备生物柴油(高级脂肪酸甲酯),其原理及实验步骤如下:
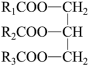 +3CH3OH
+3CH3OH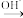
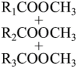 (高级脂肪酸甲酯) +
(高级脂肪酸甲酯) + 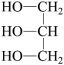
①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶,充分振荡得KOH甲醇溶液
②将40g橄榄油(平均相对分子质量279~286)、40g 正己烷(作溶剂)、配好的KOH甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图,固定装置省略),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;
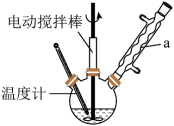
④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
(3)油脂在碱性条件下发生的水解反应称为___ 反应。
(4)装置中仪器a的名称是___ ,保持反应温度在60~64℃左右最好采用的加热方式为___
(5)实验中甲醇过量的主要目的是:___ ; KOH 的用量不宜过多,其原因是:___
(6)步骤④的液体分为两层,上层为生物柴油、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的操作依据是:__
(1)下列物质在一定条件下能与X发生反应的有
A.氢气 B.乙醇 C.溴水 D.烧碱溶液 E.高锰酸钾酸性溶液
(2)Y的分子式为
II.某同学在实验室利用橄榄油与甲醇制备生物柴油(高级脂肪酸甲酯),其原理及实验步骤如下:
 +3CH3OH
+3CH3OH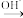
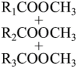 (高级脂肪酸甲酯) +
(高级脂肪酸甲酯) + 
①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶,充分振荡得KOH甲醇溶液
②将40g橄榄油(平均相对分子质量279~286)、40g 正己烷(作溶剂)、配好的KOH甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图,固定装置省略),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;

④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
(3)油脂在碱性条件下发生的水解反应称为
(4)装置中仪器a的名称是
(5)实验中甲醇过量的主要目的是:
(6)步骤④的液体分为两层,上层为生物柴油、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的操作依据是:
您最近一年使用:0次
名校
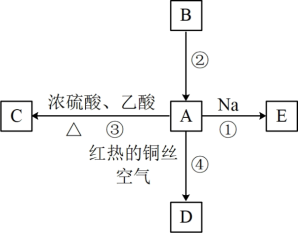
10 . A、B、C、D、E均为有机物,其中A是化学实验中常见的有机物,易溶于水并有特殊香味:B的产量可以用来衡量一个国家石油化学工业的发展水平,有关物质的转化关系如图所示。
Ⅰ.根据图示完成下列问题:
(1)A中官能团的名称为___________ 。
(2)反应②的反应类型是___________ 。
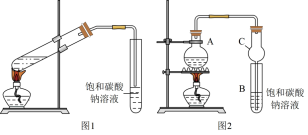
Ⅱ.某校化学探究小组甲、乙两同学分别使用图1、图2装置探究制备反应③的情况。
已知:①无水氯化钙可与乙醇形成难溶于水的 。
。
②相关有机物的沸点:
(3)甲同学向试管中加入3mL乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸。用酒精灯小心均匀地加热试管3-5分钟,产生的蒸汽经导管通到饱和碳酸钠溶液的液面上。关于制备乙酸乙酯的说法错误的是___________ (填标号)。
A.换成水浴加热原料的损失会减少
B.不断蒸出乙酸乙酯,会降低其产率
C.饱和碳酸钠的作用是吸收乙醇,中和乙酸,降低乙酸乙酯溶解度
D.分离乙酸乙酯所需的玻璃仪器是蒸馏烧瓶
E.除去乙酸乙酯中少量的乙醇和水,可先加足量无水氯化钙过滤,再加无水硫酸钠后蒸馏
(4)最终制得纯净的乙酸乙酯2.2g,产率是___________ (计算结果保留3位有效数字)。
(5)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,乙同学利用图2所示装置进行了四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管B,再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是___________ mL和___________ mol/L。
②分析实验___________ (填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。

Ⅰ.根据图示完成下列问题:
(1)A中官能团的名称为
(2)反应②的反应类型是
Ⅱ.某校化学探究小组甲、乙两同学分别使用图1、图2装置探究制备反应③的情况。

已知:①无水氯化钙可与乙醇形成难溶于水的
 。
。②相关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 117.9 | 77 |
密度( ) ) | 0.714 | 0.778 | 1.05 | 0.897 |
A.换成水浴加热原料的损失会减少
B.不断蒸出乙酸乙酯,会降低其产率
C.饱和碳酸钠的作用是吸收乙醇,中和乙酸,降低乙酸乙酯溶解度
D.分离乙酸乙酯所需的玻璃仪器是蒸馏烧瓶
E.除去乙酸乙酯中少量的乙醇和水,可先加足量无水氯化钙过滤,再加无水硫酸钠后蒸馏
(4)最终制得纯净的乙酸乙酯2.2g,产率是
(5)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,乙同学利用图2所示装置进行了四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管B,再测有机层的厚度,实验记录如下:
| 实验编号 | 烧瓶A中的试剂 | 试管B中试剂 | 测得有机层厚度/cm |
| A | 3mL乙醇、2mL乙酸、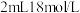 浓硫酸 浓硫酸 | 饱和碳酸钠溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、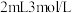 硫酸 硫酸 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
②分析实验
您最近一年使用:0次



