1 . 石油是重要的化工原料,淀粉是天然高分子化合物,对它们进行综合利用具有重要的意义,有关生产流程如下:
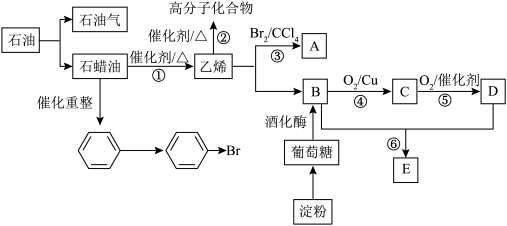
(1)石油气中含有一种碳、氢元素的质量比为5:1的烷烃,它的化学式为_______ ,它有_______ 种同分异构体(不含立体异构);①中获得乙烯的方法称为_______ 。
(2)葡萄糖中含有的官能团名称为_______ ;③的反应类型为_______ 。
(3)④的反应方程式为_______ 。
(4)实验室模拟流程中制取E的装置如图1所示。实验前试管乙中的溶液为饱和 溶液,向其中滴加几滴紫色石蕊试液,溶液呈蓝色,实验结束后向乙中继续滴加紫色石蕊试液,振荡,现象如图2所示。
溶液,向其中滴加几滴紫色石蕊试液,溶液呈蓝色,实验结束后向乙中继续滴加紫色石蕊试液,振荡,现象如图2所示。

①B+D→E的化学方程式为_______ 。
②出现图2所示现象的原因是_______ 。

(1)石油气中含有一种碳、氢元素的质量比为5:1的烷烃,它的化学式为
(2)葡萄糖中含有的官能团名称为
(3)④的反应方程式为
(4)实验室模拟流程中制取E的装置如图1所示。实验前试管乙中的溶液为饱和
 溶液,向其中滴加几滴紫色石蕊试液,溶液呈蓝色,实验结束后向乙中继续滴加紫色石蕊试液,振荡,现象如图2所示。
溶液,向其中滴加几滴紫色石蕊试液,溶液呈蓝色,实验结束后向乙中继续滴加紫色石蕊试液,振荡,现象如图2所示。
①B+D→E的化学方程式为
②出现图2所示现象的原因是
您最近半年使用:0次
2023-07-12更新
|
87次组卷
|
2卷引用:福建省三明市普通高中2022-2023学年高一下学期期末质量检测化学试题
名校
2 . 乳酸乙酯作为香料主要用于配制朗姆酒、牛奶、果酒等型香精。由淀粉为原料合成乳酸乙酯的路线如图:
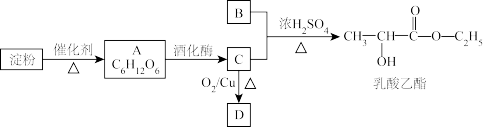
回答下列问题:
(1)A中含有的官能团的名称____ ,C→D的反应类型为____ 。
(2)B的结构简式为____ 。
(3)E是乳酸乙酯的一种同分异构体,两分子E在一定条件下可发生酯化反应生成六元环酯,则E的结构简式可能为____ (写出一种即可)。
(4)除以淀粉为原料制备C,工业上制备C的方法还有____ (用化学方程式表示)。
(5)检验淀粉在酸性条件下发生水解反应的操作:取少量冷却后的水解液于试管中,加NaOH溶液至碱性,再加入少量____ ,加热,若____ (填现象),则证明淀粉已发生水解。

回答下列问题:
(1)A中含有的官能团的名称
(2)B的结构简式为
(3)E是乳酸乙酯的一种同分异构体,两分子E在一定条件下可发生酯化反应生成六元环酯,则E的结构简式可能为
(4)除以淀粉为原料制备C,工业上制备C的方法还有
(5)检验淀粉在酸性条件下发生水解反应的操作:取少量冷却后的水解液于试管中,加NaOH溶液至碱性,再加入少量
您最近半年使用:0次
3 . 现有甲、乙、丙、丁四种有机物,其中甲、乙、丁均属于烃类,丙中只含C、H、O三种元素。甲是一种烷烃且碳原子数是乙的两倍;常温下乙的密度与 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
(1)①若甲的结构中无支链,则甲的结构简式为___________ ,其分子中所有碳原子___________ (填标号)在一条直线上。
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和 的混合气体,装置如图:
的混合气体,装置如图:
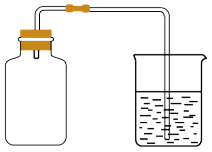
光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有___________ 、___________ (任意写出两条)。
(2)乙的电子式为___________ ;乙与水在一定条件下反应生成丙的化学方程式为___________ 。
(3)将光亮的铜丝放到酒精灯上灼烧后再插入丙中,并重复几次,可观察到的现象为___________ ,在铜作催化剂并加热的条件下,丙与氧气发生反应的化学方程式为___________ 。
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量大小顺序是___________ (用甲、乙、丙、丁表示)。
 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:(1)①若甲的结构中无支链,则甲的结构简式为
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和
 的混合气体,装置如图:
的混合气体,装置如图:
光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有
(2)乙的电子式为
(3)将光亮的铜丝放到酒精灯上灼烧后再插入丙中,并重复几次,可观察到的现象为
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量大小顺序是
您最近半年使用:0次
解题方法
4 . 以淀粉或乙烯为主要原料都可以合成乙酸乙酯,其合成路线如图所示。
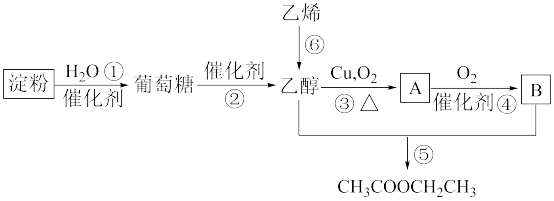
回答下列问题:
(1)淀粉的分子式为___________ ;葡萄糖分子中含有的官能团名称是___________ 。
(2)写出反应⑤的化学方程式___________ ,反应类型为___________ 反应。
(3)下列有关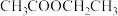 的性质说法正确的是
的性质说法正确的是___________ (填序号)。
a.密度比水小 b.能溶于水 c.能发生加成反应 d.能发生取代反应
(4)比乙烯多一个碳的同系物可以发生加聚反应,其加聚产物的结构简式可表示为___________ 。
(5)物质B与新制氢氧化铜悬浊液混合后现象为________ 。
(6)某学习小组设计乙醇催化氧化转化成A的实验装置如图所示,试回答下列问题。
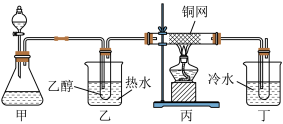
①甲的锥形瓶中盛放的固体药品可能为________ (填字母)。
A. B.KCl C.
B.KCl C. D.
D.
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为________ 。

回答下列问题:
(1)淀粉的分子式为
(2)写出反应⑤的化学方程式
(3)下列有关
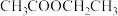 的性质说法正确的是
的性质说法正确的是a.密度比水小 b.能溶于水 c.能发生加成反应 d.能发生取代反应
(4)比乙烯多一个碳的同系物可以发生加聚反应,其加聚产物的结构简式可表示为
(5)物质B与新制氢氧化铜悬浊液混合后现象为
(6)某学习小组设计乙醇催化氧化转化成A的实验装置如图所示,试回答下列问题。

①甲的锥形瓶中盛放的固体药品可能为
A.
 B.KCl C.
B.KCl C. D.
D.
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为
您最近半年使用:0次
5 . 链状烃A( )是基本有机化工原料,由A制备聚合物C和
)是基本有机化工原料,由A制备聚合物C和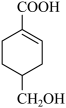 合成路线如图所示(部分条件略去)。
合成路线如图所示(部分条件略去)。

①
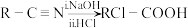
(1)A的名称是
(2)C、D的结构简式分别为
(3)E→F的化学方程式为
(4)B的同分异构体中,满足B中含有一个羧基,并能与溴的四氯化碳溶液发生反应而褪色,且有3种不同化学环境的氢原子,个数比为6∶1∶1的是
(5)等物质的量的
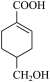 分别与足量NaOH、
分别与足量NaOH、 反应,消耗NaOH、
反应,消耗NaOH、 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
6 . 水杨酸A具有解热镇痛的功效,其可作为医药工业的原料,用水杨酸制备平喘药沙丁胺醇的路线如下(Ac表示-COCH3;Ph表示-C6H5)。
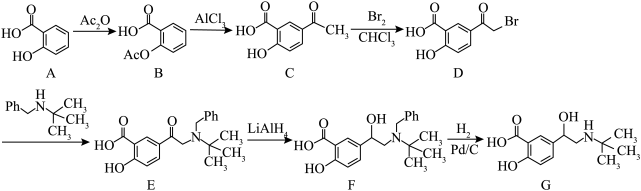
(1)化合物 A的分子式为
 的反应类型为
的反应类型为(2)化合物 D中含有四种官能团,任选两种官能团进行检验。
限选试剂:NaOH溶液、稀硝酸、稀硫酸、新制氢氧化铜悬浊液、饱和溴水、硝酸银、NaHCO3溶液、FeCl3溶液。
官能团名称 | 所选试剂 | 实验现象 |
(3)化合物M(
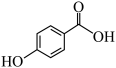 )是化合物A的同分异构体,其沸点M
)是化合物A的同分异构体,其沸点M(4)化合物C有多种同分异构体,写出其中一种能同时满足下列条件的芳香族化合物的结构简式
①能发生水解反应且最多能与4倍物质的量的NaOH反应
②核磁共振氢谱有四组峰,峰面积之比为 3:2:2:1
(5)以水杨酸
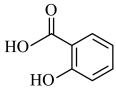 、乙二醇以及甲基丙烯酸(
、乙二醇以及甲基丙烯酸(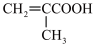 )为原料,利用
)为原料,利用 的原理及所学知识,合成
的原理及所学知识,合成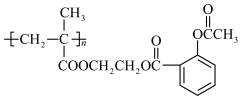
基于你设计的路线,回答下列问题。
①从水杨酸出发,第一步反应的化学方程式为
②最后一步反应中,反应物为
您最近半年使用:0次
7 . 以乙炔为主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡胶,有关合成路线如图所示。
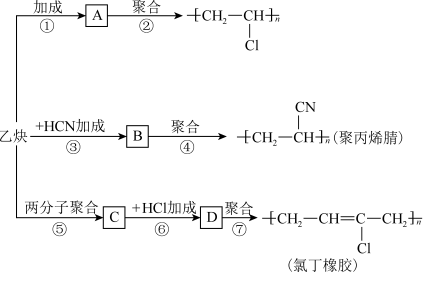
已知反应:nCH2=CH-CH=CH2

请完成下列各题:
(1)写出物质的结构简式:A_____ ,D_____ 。
(2)写出反应③的化学方程式:_____ 。
(3)某化学兴趣小组选用下列装置和药品制取乙炔并进行有关乙炔性质的探究。试回答下列问题:
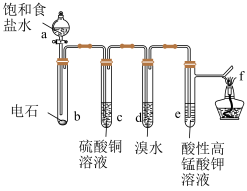
①b中制取乙炔的化学方程式为_____ 。
②制乙炔时,a中装饱和食盐水的目的是_____ 。
③d、e中的反应现象都是溶液褪色,d中反应类型是_____ ;e中反应类型是_____ 。
④若足量溴水吸收乙炔,完全反应生成C2H2Br4,已知称取电石m克,理想状况下,测得d中增重n克,则电石纯度(写出计算过程)_____ 。

已知反应:nCH2=CH-CH=CH2


请完成下列各题:
(1)写出物质的结构简式:A
(2)写出反应③的化学方程式:
(3)某化学兴趣小组选用下列装置和药品制取乙炔并进行有关乙炔性质的探究。试回答下列问题:

①b中制取乙炔的化学方程式为
②制乙炔时,a中装饱和食盐水的目的是
③d、e中的反应现象都是溶液褪色,d中反应类型是
④若足量溴水吸收乙炔,完全反应生成C2H2Br4,已知称取电石m克,理想状况下,测得d中增重n克,则电石纯度(写出计算过程)
您最近半年使用:0次
解题方法
8 . 现有甲、乙、丙、丁四种有机物,其中甲、乙、丁均属于烃类,丙中只含C、H、O三种元素。甲是一种烷烃且碳原子数是乙的两倍;常温下乙的密度与 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12∶1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12∶1,回答下列问题:
(1)①若甲的结构中无支链,则甲的结构简式为_______ ,其分子中所有碳原子_______ (填标号)同一平面上。
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和 的混合气体,装置如图:
的混合气体,装置如图:

光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有_______ 、_______ (任意写出两条)。
(2)乙的电子式为_______ ;乙与水反应生成丙的化学方程式为_______ 。
(3)丙中含有的官能团的名称为_______ ;将光亮的铜丝放到酒精灯上灼烧后再插入丙中,并重复几次,可观察到的现象为_______ ,在铜作催化剂并加热的条件下,丙与氧气发生反应的化学方程式为_______ 。
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量的大小关系为_______ (填分子式)。
 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12∶1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12∶1,回答下列问题:(1)①若甲的结构中无支链,则甲的结构简式为
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和
 的混合气体,装置如图:
的混合气体,装置如图:
光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有
(2)乙的电子式为
(3)丙中含有的官能团的名称为
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量的大小关系为
您最近半年使用:0次
9 . 如表是A、B、C三种烃的有关信息
根据表中信息回答下列问题:
(1)写出烃A与水反应的化学方程式:_______ ,A发生加聚反应的产物名称_______ 。
(2)烃B与浓硝酸反应的化学方程式:_______ 。
(3)如图1是烃B与液溴制取溴苯的装置,试回答:
(a)装置A中发生有机反应的化学方程式:_______ 。
(b)装置C中的现象_______ 。
(c)装置B的作用_______ 。
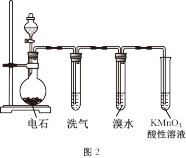
(4)如图2是制取烃C的装置,试回答:
(a)为了控制生成C的速率,分液漏斗中盛放的液体是_______ 。
(b)滴下液体后烧瓶中发生反应生成C,写出此反应的化学方程式:_______ 。
(c)电石中含有硫化钙和水反应会产生杂质气体混在C中,为了不对C性质检验产生干扰,应该除杂,一般选用_______ 洗气。
| A | B | C |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为: 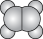 | ①平面型结构; ②球棍模型为:  | ①能使溴的四氯化碳溶液褪色; ②1 mol C能与1 mol H2在一定条件下反应生成A; ③比例模型为:  |
 |  |
(1)写出烃A与水反应的化学方程式:
(2)烃B与浓硝酸反应的化学方程式:
(3)如图1是烃B与液溴制取溴苯的装置,试回答:
(a)装置A中发生有机反应的化学方程式:
(b)装置C中的现象
(c)装置B的作用
(4)如图2是制取烃C的装置,试回答:
(a)为了控制生成C的速率,分液漏斗中盛放的液体是
(b)滴下液体后烧瓶中发生反应生成C,写出此反应的化学方程式:
(c)电石中含有硫化钙和水反应会产生杂质气体混在C中,为了不对C性质检验产生干扰,应该除杂,一般选用
您最近半年使用:0次
2022-05-18更新
|
187次组卷
|
3卷引用:安徽省青阳县第一中学2021-2022学年高二下学期5月月考化学试题
2023高三·全国·专题练习
10 . 设计实验,对有机物中官能团进行检验和探究。
(1)某同学设计如下实验,证明溴乙烷中含有溴元素
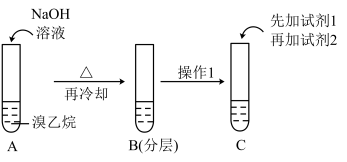
①简述操作1:_______ 。
②C中所加入试剂1为_______ (填化学式)。
(2)资料显示: 可被
可被 氧化,使溴水褪色
氧化,使溴水褪色
① 中加入
中加入 反应的化学方程式:
反应的化学方程式:_______ 。
②用化学试剂检验 中含有的官能团,只取一次待检验溶液,首先检验的官能团是
中含有的官能团,只取一次待检验溶液,首先检验的官能团是_______ (填名称,下同),最后检验的官能团是_______ 。
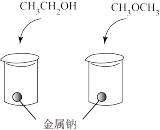
(3)按如图装置对官能团的性质进行进一步探究
实验现象:左侧烧杯内有无色气泡产生,右侧烧杯内无明显现象,由此可知 与金属钠反应时
与金属钠反应时_______ 断裂,判断的依据是_______ 。
(1)某同学设计如下实验,证明溴乙烷中含有溴元素

①简述操作1:
②C中所加入试剂1为
(2)资料显示:
 可被
可被 氧化,使溴水褪色
氧化,使溴水褪色①
 中加入
中加入 反应的化学方程式:
反应的化学方程式:②用化学试剂检验
 中含有的官能团,只取一次待检验溶液,首先检验的官能团是
中含有的官能团,只取一次待检验溶液,首先检验的官能团是(3)按如图装置对官能团的性质进行进一步探究
实验现象:左侧烧杯内有无色气泡产生,右侧烧杯内无明显现象,由此可知
 与金属钠反应时
与金属钠反应时
您最近半年使用:0次



