1 . (2018·全国I卷)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ 。
A. B.
B.
C. D.
D.
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
2023-04-25更新
|
621次组卷
|
6卷引用:专题2 原子结构与元素性质 ★第一单元综合拔高练
专题2 原子结构与元素性质 ★第一单元综合拔高练(人教版2019)选择性必修2 第一章 原子结构与性质 第一节 原子结构(已下线)第五章 物质结构与性质 元素周期律 第26讲 原子结构核 外电子排布原理(已下线)01 常考题空1 电子排布、电离能与电负性 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)第1讲 原子结构 核外电子排布上海市育才中学2023-2024学年高三上学期10月第一次质量调研(等级考)化学试题
2 . 元素第一电离能变化规律

(1)每个周期的第一种元素的第一电离能_______ ,最后一种元素的第一电离能_______ ,即一般来说,随着核电荷数的递增,元素的第一电离能呈_______ 趋势。
(2)同一族,从上到下第一电离能逐渐_______ 。

(1)每个周期的第一种元素的第一电离能
(2)同一族,从上到下第一电离能逐渐
您最近一年使用:0次
3 . 泡利原理:在一个原子轨道里,最多只能容纳_______ 个电子,它们的自旋_______ ,常用上下箭头(↑和↓)表示自旋相反的_______ 。
您最近一年使用:0次
4 . 能层
(1)含义:根据核外电子的_______ 不同,将核外电子分为不同的能层(电子层)。
(2)序号及符号:能层序号一、二、三、四、五、六、七……分别用K、L、M、N、O、P、Q……表示,其中每层所容纳的电子数最多为_______ 个。
(3)能量关系:能层越高,电子的能量越高,能量的高低顺序为_______ <E(L)<_______ <E(N)<E(O)<E(P) _______ 。
(1)含义:根据核外电子的
(2)序号及符号:能层序号一、二、三、四、五、六、七……分别用K、L、M、N、O、P、Q……表示,其中每层所容纳的电子数最多为
(3)能量关系:能层越高,电子的能量越高,能量的高低顺序为
您最近一年使用:0次
5 . 概率密度
1913年,_______ 提出氢原子模型,电子在_______ 上绕核运行。量子力学指出,一定空间运动状态的电子在核外空间各处都可能出现,但出现的_______ 不同,可用概率密度(ρ)表示,即ρ=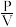 (P表示电子在某处出现的
(P表示电子在某处出现的_______ ;V表示该处的体积)。
1913年,
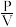 (P表示电子在某处出现的
(P表示电子在某处出现的
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
6 . 熟记第四周期未成对电子数规律
| 未成对电子数及其占据的原子轨道 | 元素符号及价电子排布 | |
| 1 | 4s | K:4s1,Cu: |
| 3d | Sc:3d14s2 | |
| 4p | Ga:4s24p1,Br: | |
| 2 | 3d | Ti:3d24s2,Ni: |
| 4p | Ge:4s24p2,Se:4s24p4 | |
| 3 | 3d | V:3d34s2,Co: |
| 4p | As:4s24p3 | |
| 4 | 3d | Fe: |
| 5 | 3d | Mn:3d54s2 |
| 6 | 3d和4s | Cr:3d54s1 |
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
7 . 原子轨道
(1)概念:量子力学把电子在原子核外的一个_______ 称为一个原子轨道。
(2)形状
①s电子的原子轨道呈_______ 形,能层序数越_______ ,原子轨道的半径越_______ 。
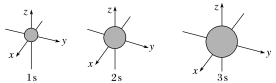
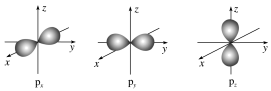
②p电子的原子轨道呈_______ 形,能层序数越_______ ,原子轨道的半径越_______ 。
(1)概念:量子力学把电子在原子核外的一个
(2)形状
①s电子的原子轨道呈

②p电子的原子轨道呈

您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
8 . 电子排布式
将_______ 上所容纳的电子数标在该能级符号_______ ,并按照能层从左到右的顺序排列的式子。
如氮原子的电子排布式为:

例:根据构造原理,写出下列基态原子的核外电子排布式
①2He:_______ ;
②8O:_______ ;
③10Ne:_______ ;
④14Si:_______ ;
⑤18Ar:_______ ;
⑥19K:_______ ;
⑦21Sc:_______ ;
⑧26Fe:_______ 。
将
如氮原子的电子排布式为:

例:根据构造原理,写出下列基态原子的核外电子排布式
①2He:
②8O:
③10Ne:
④14Si:
⑤18Ar:
⑥19K:
⑦21Sc:
⑧26Fe:
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
9 . 解题技巧:粒子半径比较的一般思路
(1)“一层”:先看能层数,能层数越_______ ,一般微粒半径越_______ 。
(2)“二核”:若能层数相同,则看核电荷数,核电荷数越_______ ,微粒半径越_______ 。
(3)“三电子”:若能层数、核电荷数均相同,则看核外电子数,电子数_______ 的半径_______ 。
(1)“一层”:先看能层数,能层数越
(2)“二核”:若能层数相同,则看核电荷数,核电荷数越
(3)“三电子”:若能层数、核电荷数均相同,则看核外电子数,电子数
您最近一年使用:0次
10 . 注意:电离能的影响因素及特例
(1)电离能数值的大小主要取决于原子的_______ 、原子半径及原子的电子构型。
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值_______ ,如稀有气体的电离能在同周期元素中_______ ,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。一般情况,第一电离能:ⅡA_______ ⅢA,ⅤA_______ ⅥA。
(1)电离能数值的大小主要取决于原子的
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值
您最近一年使用:0次



