1 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W的原子核外只有6个电子,X+和Y3+的电子层结构相同,Z-的电子数比Y3+多8个,下列叙述正确的是
| A.W在自然界只有一种核素 | B.半径大小:X+>Y3+>Z- |
| C.Y与Z形成的化合物的水溶液呈弱酸性 | D.X的最高价氧化物对应的水化物为弱碱 |
您最近一年使用:0次
2017-05-25更新
|
1002次组卷
|
4卷引用:福建省宁德市2017届高三毕业班第三次质量检查化学试题
名校
2 . X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确 的是
| Y | Z | M | ||
| W |
| A.原子半径:W>Y>Z>M>X |
| B.N的一种氧化物可用作油漆和涂料 |
| C.氢化物的沸点:Z小于M |
| D.工业上制备W单质的方法为电解熔融的W的氧化物 |
您最近一年使用:0次
2017-05-25更新
|
1560次组卷
|
4卷引用:辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题
辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题
名校
3 . 中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
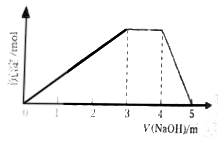
| A.简单的离子半径:M>Y>Z |
| B.气态氢化物的热稳定性:Y>X |
| C.由R、X、Y、M四种元素只组成一种盐 |
| D.最高价氧化物对应水化物的酸性:M>Z |
您最近一年使用:0次
2017-05-25更新
|
607次组卷
|
3卷引用:广东省汕头市2017届高三第三次模拟考试理科综合化学试题
名校
4 . 2017年1月26日,美国《科学》杂志刊发论文称发现了一种新材料——金属氢,证实了一百多年前提出的存在金属氢的假说。下列事实不能说明氢可能具有金属性的是
| A.可以把H写入金属活动性顺序表 | B.H与Na、K等碱金属元素同属于第IA族 |
| C.H存在H- | D.H与非金属反应,产物中H通常显正价 |
您最近一年使用:0次
2017-05-24更新
|
626次组卷
|
2卷引用:河北省石家庄市第二中学2017届高三5月联考理科综合化学试题
5 . 短周期主族元素X、Y、Z、W、M的原子序数依次增大,其中X与其它元素均不位于同一主族,Y和W的原子序数相差8,Y、Z、W三种原子的最外层电子数之和为16,X、Z的最高正价和最低负价的代数和均为0。下列说法正确的是
| A.M的氢化物的水溶液能与W的钠盐溶液,反应得到W的氢化物,说明非金属性M>W |
| B.X和Y形成的原子个数比为1∶1的分子中极性键和非极性键个数之比为2∶1 |
| C.Z元素在自然界中存在游离态 |
| D.原子半径的大小顺序:r(W)>r(Z)>r(Y) |
您最近一年使用:0次
名校
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大。X、W在同一主族,Z+与Y3-具有相同的电子层结构,X原子的最外层电子数是其内层电子数的2倍。下列说法正确的是
| A.粒子半径的大小顺序:r(W)>r(X)> r(Z+)> r(Y3-) |
| B.X的最高价氧化物对应水化物的酸性比Y的强 |
| C.W的气态简单氢化物的热稳定性比X的强 |
| D.工业上可用X的单质与W的氧化物反应制备W的单质 |
您最近一年使用:0次
解题方法
7 . 原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界存在多种A的化合物,B原子核外电子由6种不同的运动状态,B与C可形成正四面体形分子,D的M能层没有空轨道且只有2个未成对电子。请回答下列问题:
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为________ 。
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有________ 个六元环;图2位在元素周期表中与B相邻的元素位置关系,B、G形成的晶胞结构如图3所示(其中“●”为B元素原子,“〇”为G元素原子),图中“●”点构成的堆积方式与图4中_____ (填序号)所表示的堆积方式相同;图3的结构中,设晶胞边长为a cm,B原子直径为bcm,G原子直径为c cm,则该晶胞的空间利用率为_______ (用含a、b、c的式子表示)。

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式_____ (用化学式表示)。
(4)元素C的含氧酸中,酸性最强的是_________ (写化学式),该酸根离子的立体构型为________ 。
(5)基态D原子的核外电子排布式为[Ar]_______ ;D形成的配合物D(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______ ;由D一铝合金为原料可制得一种历史悠久、应用广泛的催化剂,其催化的i实例为: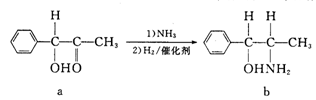 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有__________ (填元素符号)。
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式
(4)元素C的含氧酸中,酸性最强的是
(5)基态D原子的核外电子排布式为[Ar]
 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有
您最近一年使用:0次
名校
8 . 短周期元素X、Y、Z、W、Q的原子序数依次增大,X与Q同主族,X的最外层电子数是次外层电子数的2倍,W的最外层电子数等于其电子层数,Y与Z的核外电子数之和等于X与Q的核外电子数之和,下列说法正确的是
| A.Z、W、Q、X、Y原子半径依次减小 |
| B.W最高价氧化物对应水化物一定能溶于Z最高价氧化物对应水化物的溶液中 |
| C.Y与Q形成化合物在常温下一定为气态 |
| D.Z、Q元素的单质都可以将X元素的单质从其氧化物中置换出来 |
您最近一年使用:0次
2017-05-07更新
|
1270次组卷
|
5卷引用:黑龙江省哈尔滨师范大学附属中学2017届高三第三次模拟考试化学试题
名校
9 . X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期。下列说法正确的是
| A.简单离子半径R>W>Y>Z |
| B.气态氢化物稳定性:HmW<HnR |
C.Z2Y2电子式可表示为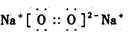 |
| D.RY2和W2均有漂白性,将两者等物质的量混合溶于水,漂白性增强 |
您最近一年使用:0次
2017-05-07更新
|
1141次组卷
|
2卷引用:江西省南昌市2017届高三二模测试卷理综化学试题
10 . 下列说法不正确 的是
| A.某外围电子排布为4f75d16s2基态原子,该元素位于周期表中第六周期第ⅢB族 |
| B.在元素周期表中,s区,d区和ds区的元素都是金属元素 |
C.当碳原子的核外电子排布由 转变为 转变为 时,释放能量,由激发态转化成基态 时,释放能量,由激发态转化成基态 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8 |
您最近一年使用:0次
2017-05-05更新
|
2903次组卷
|
10卷引用:山东省德州一中2021届高三10月月考化学试题
山东省德州一中2021届高三10月月考化学试题(已下线)第30讲 原子结构与性质(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题新疆维吾尔自治区伊犁哈萨克自治州奎屯市第一高级中学2019-2020学年高二期末考试试题湖北省石首市第一中学2019-2020学年高二下学期摸底考试化学试题(已下线)第一章 原子结构与性质【过关测试提高卷】-2020-2021学年高二化学单元复习(新教材人教版选择性必修2)广东省东莞市东华高级中学2021-2022学年高二下学期月考化学试题第一章 原子结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)



