1 . 下表是元素周期表的一部分,针对元素①~⑥回答下列问题。
(1)④元素在周期表中的位置为_______ 。
(2)金属性最强的元素为_______ (填元素符号),其最高价氧化物对应的水化物中含有的化学键为_______ 。
(3)①③⑤三种元素对应的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)元素的非金属性⑥_______ Br(填“>”“<”或“=”),写出能证明该结论的离子方程式_______ 。
| ④ | ⑤ | ||||||
| ① | ③ | ⑥ | |||||
| ② | |||||||
(2)金属性最强的元素为
(3)①③⑤三种元素对应的简单离子半径由大到小的顺序为
(4)元素的非金属性⑥
您最近一年使用:0次
名校
解题方法
2 . 下图是元素周期表的一部分。
(1)①-⑩元素中最稳定的原子是_______ (填元素符号);形成的气态氢化物稳定性最强的是_______ (填氢化物的化学式)。
(2)②的最高价氧化物的电子式为_______ ;用电子式表示⑤和⑥形成化合物的过程:_______ 。
(3)①和⑦金属性相似,①的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为_______ 。
(4)某同学设计了如下实验证明非金属性③>②>⑧。已知 是不溶于水的白色胶状沉淀,
是不溶于水的白色胶状沉淀, 易挥发。
易挥发。
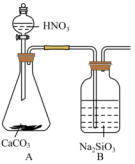
该同学打开分液漏斗活塞,观察到A中产生气泡,B中出现白色胶状沉淀即认为非金属性③>②>⑧。请问该同学的结论合理吗_______ (答“合理”或“不合理”),原因是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)①-⑩元素中最稳定的原子是
(2)②的最高价氧化物的电子式为
(3)①和⑦金属性相似,①的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为
(4)某同学设计了如下实验证明非金属性③>②>⑧。已知
 是不溶于水的白色胶状沉淀,
是不溶于水的白色胶状沉淀, 易挥发。
易挥发。
该同学打开分液漏斗活塞,观察到A中产生气泡,B中出现白色胶状沉淀即认为非金属性③>②>⑧。请问该同学的结论合理吗
您最近一年使用:0次
名校
3 . 几种主族元素在周期表中的位置如下
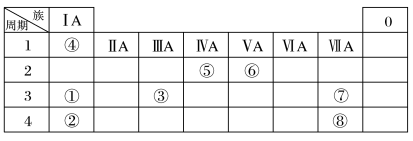
根据上表回答下列问题:
(1)⑦元素的氢化物的电子式是___________ 。
(2)①③⑦三种元素原子半径由大到小的顺序是___________ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是___________ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是___________(填字母)。
(6)①和④形成的化合物是___________ (填“离子”或“共价”)化合物。

根据上表回答下列问题:
(1)⑦元素的氢化物的电子式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是___________(填字母)。
| A.⑦的氢化物比⑧的氢化物稳定 |
| B.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性 |
| C.⑦的单质能将⑧从其钠盐溶液中置换出来 |
| D.⑦的氢化物酸性比⑧的氢化物酸性弱 |
您最近一年使用:0次
2022-09-30更新
|
558次组卷
|
2卷引用:广东省潮州市湘桥区磷溪中学2021-2022学年高一上学期期末考试化学试题
名校
解题方法
4 . 我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为: S+2KNO3+3C=K2S+3CO2↑+N2↑。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,
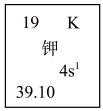
数据“39.10”表示的是___________ ;钾元素在周期表中的位置为___________ 。
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是___________ 。
(3)上述反应生成物中,属于非电解质的是___________ (写结构式);生成物中含有离子键的物质电子式是___________ 。
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为___________ ,它们的非金属性由强到弱的顺序为___________ ;列举一条能证明S和O非金属性强弱的实验事实___________ 。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,

数据“39.10”表示的是
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为
您最近一年使用:0次
5 . 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
请回答下列问题。
(1)元素a中,含有1个质子和1个中子的核素的原子符号为_______ 。e的离子结构示意图为_______ ,元素 g在周期表中的位置为_______ 。
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为_______ 。
(3)非金属性,f_______ g(填“>”或“<”),能证明该结论的依据为_______ (列举一条)。
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:_______ (用相应的化学式表示)。
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
h |
(1)元素a中,含有1个质子和1个中子的核素的原子符号为
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为
(3)非金属性,f
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式
您最近一年使用:0次
名校
6 . 如图是元素周期表的一部分。回答下列问题:

溴被称为海洋元素。
(1)溴在元素周期表中位于第___________ 周期___________ 族。
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
(3)能够证明溴的非金属性强于碘的方法是___________ (写出一种即可)。

溴被称为海洋元素。
(1)溴在元素周期表中位于第
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
(3)能够证明溴的非金属性强于碘的方法是
您最近一年使用:0次
名校
7 . 下表为元素周期表的一部分,请回答下列有关问题:
(1)元素②的一种核素可测定文物年代,这种核素的符号为___________ ,已知元素⑩的一种核素,其中子数为45,这种核素的符号为___________ 。
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为___________ 。
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是___________ (用化学式回答),写出该水化物与⑥的最高价氧化物的水化物反应的离子方程式___________ 。
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:___________ 与盐酸反应最剧烈,___________ 与盐酸反应的速度最慢;___________ 与盐酸反应产生的气体最多。(用元素符号回答)
(5)元素的非金属性⑧___________ ⑩(填“>”或“<”);下列事实不能证明上述结论的是___________ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)元素②的一种核素可测定文物年代,这种核素的符号为
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
您最近一年使用:0次
名校
8 . 下表是周期表中的一部分,根据①—⑧在周期表中的位置,用元素符号或化学式回答问题
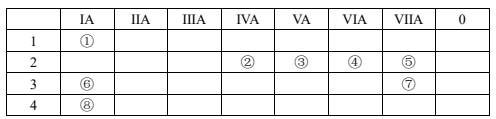
(1)画出表中元素中,非金属性最强的元素的离子结构示意图_______ ;
(2)这些元素的最高价氧化物对应水化物中酸性最强的是______ ,碱性最强的是______ ;
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程_______ ;
(4)表中⑤⑦两种元素氢化物的稳定性更强的是_______ ;
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是_______ ,简述判断理由_______ ;
(6)用一个化学方程式证明②③两种元素非金属性的强弱_______ 。

(1)画出表中元素中,非金属性最强的元素的离子结构示意图
(2)这些元素的最高价氧化物对应水化物中酸性最强的是
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程
(4)表中⑤⑦两种元素氢化物的稳定性更强的是
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是
(6)用一个化学方程式证明②③两种元素非金属性的强弱
您最近一年使用:0次
名校
9 . 下表是元素周期表的一部分,回答下列关问题:
(1)下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是_______ (填元素符号),简单离子半径最小的是_______ (填化学式)。
(3)④与⑧可以形成_______ (填离子或共价)化合物,请用电子式表示其形成过程:_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是
(3)④与⑧可以形成
您最近一年使用:0次
名校
10 . 下表列出了13种元素在元素周期表中的位置:
(1)画出这13钟元素中,非金属性最强的元素的原子结构示意图:_______
(2)元素④⑤⑩分别和①形成的气体化合物中,最稳定的是(填化学式,下同)_______ ;⑦⑫⑬形成的简单离子半径由大到小的顺序是_______ 。
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ ,呈两性的氢氧化物是_______ 。写出三者之间两两反应的化学方程式:_______ 。
(4)可以用来证明⑦和⑧两种元素金属性强弱的实验是_______(填字母)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ||
| 四 | ⑫ | ⑬ |
(1)画出这13钟元素中,非金属性最强的元素的原子结构示意图:
(2)元素④⑤⑩分别和①形成的气体化合物中,最稳定的是(填化学式,下同)
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是
(4)可以用来证明⑦和⑧两种元素金属性强弱的实验是_______(填字母)
| A.将在空气中放置已久的两种元素的块状单质分别放入水中 |
| B.将形状、大小相同的无氧化膜的两种元素的单质分别和同浓度同体积的盐酸反应 |
| C.将形状、大小相同的无氧化膜的两种元素的单质分别和温度相同的热水作用,并滴入酚酞 |
| D.比较两种元素氢化物的热稳定性 |
您最近一年使用:0次



