名校
1 . 氮化铝(AlN)是一种新型材料,硬度大、耐高温、耐腐蚀。
(1)Al在周期表中的位置是___ 。与Al同周期,金属性最强的是___ ,它的最高价氧化物对应水化物与Al的化学反应方程式为___ 。
(2)比较原子半径大小:r(N)___ r(F)(填>、<或=),写出F原子的结构示意图:___ ,写出N原子的电子式:___ 。
(3)请写出一条能证明F的非金属性比N强的事实:___ 。
(1)Al在周期表中的位置是
(2)比较原子半径大小:r(N)
(3)请写出一条能证明F的非金属性比N强的事实:
您最近一年使用:0次
名校
2 . 下表是元素周期表的一部分,针对表中的①~⑩中10种元素回答以下问题:
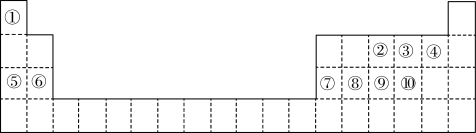
(1)写出⑧元素在周期表的位置______________________ ;
(2)实验室制取②氢化物的化学方程式_______________________________________ ;
②的氢化物与其最高价氧化物水化物反应生成的物质是________________ (填名称)
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是________ (填“共价化合物”或“离子化合物”),可以证明你判断正确的实验依据为:________________________ 。
(4)用电子式表示④、⑥两元素结合成化合物的形成过程____________________________ 。

(1)写出⑧元素在周期表的位置
(2)实验室制取②氢化物的化学方程式
②的氢化物与其最高价氧化物水化物反应生成的物质是
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是
(4)用电子式表示④、⑥两元素结合成化合物的形成过程
您最近一年使用:0次
名校
3 . 如表列出了①~⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是________ (填写化学式)。
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为_____________ (用元素符号表示)。
(3)元素①的气态氢化物的电子式是_________ ,写出实验室里制取该气体的化学方程式为 ____________________ 。
(4)元素③的原子结构示意图是_____ 。元素⑤的单质的导电性介于导体和绝缘体之间.因此是一种良好的____ 材料。
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为_______________________ 。
(6)用离子方程式证明⑦⑧两素非金属性的强弱______________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑦ | |||
| 4 | ⑥ | ⑧ |
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为
(3)元素①的气态氢化物的电子式是
(4)元素③的原子结构示意图是
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(6)用离子方程式证明⑦⑧两素非金属性的强弱
您最近一年使用:0次
2020-08-08更新
|
508次组卷
|
2卷引用:吉林省吉林市吉化第一高级中学校2019-2020学年高一下学期期末考试化学试题
解题方法
4 . 根据元素周期表中短周期的下列内容回答问题:
(1)元素①~⑨形成的单质中,化学性质最稳定的是_____ (填化学式)。④在元素周期表中的位置是________ ,⑥的简单离子的结构示意图为________________
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为________________ ,⑤、⑧按原子个数比2:1形成的化合物的电子式为________________
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:________________
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为________________
| H | ① | ||||||
| ② | ③ | O | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素①~⑨形成的单质中,化学性质最稳定的是
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为
您最近一年使用:0次
5 . A、B、C、D四种元素在元素周期表中的位置如图所示。

请回答下列问题:
(1)A的元素名称是___ ,它在元素周期表第___ 周期,第___ 族。
(2)A、B、C相比,其原子半径由大到小的顺序是___ (用元素符号表示,下同)。
(3)C与D相比,非金属性较强的是___ ,能证明这一结论的事实是___ (用化学方程式表示)。

请回答下列问题:
(1)A的元素名称是
(2)A、B、C相比,其原子半径由大到小的顺序是
(3)C与D相比,非金属性较强的是
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分。
回答下列问题:
(1)元素①的名称是____ ,元素⑧的符号是____ 。
(2)在这些元素中,___ (用元素符号或化学式填写,下同)是最活泼的非金属元素,____ 是最不活泼的元素。
(3)这些元素的最高价氧化物对应的水化物中,____ 酸性最强,____ 碱性最强,具有两性的氢氧化物是____ 。
(4)比较⑤与⑥的化学性质,____ 更活泼,试用实验证明此结论(简述操作、现象和结论):________________________ 。
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是______________________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)元素①的名称是
(2)在这些元素中,
(3)这些元素的最高价氧化物对应的水化物中,
(4)比较⑤与⑥的化学性质,
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
7 . 下表是元素周期表的一部分,请参照元素①—⑥的位置回答下列问题:

(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是__ 。
(2)⑤的原子结构示意图是__ 。
(3)上述元素中,原子半径最大的是__ (写元素符号)。
(4)仅由①、⑥组成的化合物的电子式为__ ,该化合物的分子中含有__ (填“极性”或“非极性”)共价键。
(5)金属性:③__ ④(填“>”或“<”),列举一条能证明该结论的实验事实:__ 。
(6)下列说法正确的是__ (填序号)。
a.②、③组成的化合物只有一种
b.②的气态氢化物稳定性高于⑤
c.⑥在化合物中呈现的最高化合价为+7价

(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是
(2)⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)仅由①、⑥组成的化合物的电子式为
(5)金属性:③
(6)下列说法正确的是
a.②、③组成的化合物只有一种
b.②的气态氢化物稳定性高于⑤
c.⑥在化合物中呈现的最高化合价为+7价
您最近一年使用:0次
2020-04-03更新
|
239次组卷
|
2卷引用:北京市东城区2019-2020学年高一上学期期末教学统一检测化学试题
解题方法
8 . 根据下表回答下列有关问题.
(1)写出下列元素符号:①______ ,⑥______ ,⑦______ ,⑪______ .
(2)这些元素中最活泼的金属元素是______ (填元素符号,下同),最活泼的非金属元素是______ ,最不活泼的元素是______ .
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是______ (填化学式,下同),碱性最强的是______ ,呈两性的氢氧化物是______ ,写出三者之间两两反应的化学方程式:______ ;______ ;______ .
(4)这些元素(除0族元素外)中原子半径最小的是______ (填元素符号,下同),原子半径最大的是______ .
(5)在③与④中,单质的化学性质较活泼的是______ (填元素符号),怎样用化学实验证明?______ 在⑧与⑫中,单质的化学性质较活泼的是____________ (填元素符号),怎样用化学实验证明?_____________________ .
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)这些元素中最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是
(4)这些元素(除0族元素外)中原子半径最小的是
(5)在③与④中,单质的化学性质较活泼的是
您最近一年使用:0次
2020-03-02更新
|
381次组卷
|
2卷引用:第2节 课时1原子核外电子的排布元素周期律
名校
9 . (1)现有下列10种物质:①O2;②H2;③NH4NO3;④Na2O2;⑤Ba(OH)2;⑥CH4;⑦CO2;⑧NaF;⑨NH3;⑩I2。其中既含离子键又含非极性键的是________ (填序号,下同);既含离子键又含极性键的是________ ;。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为______________________________________________ ;若XY2为共价化合物,则其结构式为_________________________________________ 。
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是______________ (填“共价化合物”或“离子化合物”),可以证明该判断正确的实验依据是_______________________________________ 。
(4)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
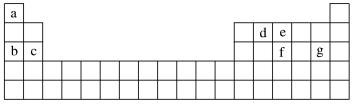
元素的原子间最容易形成离子键的是____ (填字母,下同),容易形成共价键的是____ 。
A.c和f B.b和g C.d和g D.b和e
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是
(4)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:

元素的原子间最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和e
您最近一年使用:0次
10 . 为纪念元素周期表诞生150周年,IUPAC等从世界范围征集优秀青年化学家提名,形成一张“青年化学家元素周期表”,向世界介绍118位优秀青年化学家,有8位中国青年化学家成为“N、Hg、U”等元素的代言人。回答下列问题:
(1)N在周期表中的位置是__ 。
(2)下列有关性质的比较,能用元素周期律解释的是__ 。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(3)非金属性:Cl>Br,用原子结构解释原因__ ,用一个离子方程式证明__ 。
(4)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为__ 。②X的氢化物的电子式__ 。
(1)N在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(3)非金属性:Cl>Br,用原子结构解释原因
(4)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为
您最近一年使用:0次



