解题方法
1 . 下图是元素周期表的一部分。按要求填写下列空白:
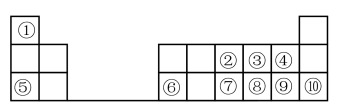
(1)元素⑦在周期表中的位置可表示为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物的电子式为_______ ;⑧的氢化物的结构式为_______
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置可表示为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物的电子式为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2022-12-21更新
|
348次组卷
|
2卷引用:海南省北京师范大学海口附属学校2020-2021学年高一下学期月考化学试题
2 . 下图是元素周期表的一部分。按要求填写下列空白:

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为_______ ;
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式);
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是_______ ;(用化学式表示);
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式_______ ;
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是________ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
3 . 2019年是门捷列夫提出元素周期表150周年,根据元素周期表和周期律,回答问题。
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
(1)①在周期表中所处的位置为__________ 。
(2)与②同族的第四周期元素的原子结构示意图为__________ 。
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式__________ 。
(4)④的单质与水反应的离子方程式为__________ 。
(5)工业制取⑤的单质的化学方程式为__________ 。
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。
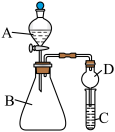
(6)干燥管D的作用是__________ 。
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为__________ 。
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液__________ 的现象,该实验设计的原理是利用最高价氧化物对应水化物的酸性强弱来比较元素非金属性的强弱。
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是__________ 。
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
① | ② | ③ | ||||
④ | ⑤ | ⑥ |
(2)与②同族的第四周期元素的原子结构示意图为
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式
(4)④的单质与水反应的离子方程式为
(5)工业制取⑤的单质的化学方程式为
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。

(6)干燥管D的作用是
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
您最近一年使用:0次
2019-08-04更新
|
195次组卷
|
2卷引用:山东省聊城市莘县第一中学2018-2019学年高一下学期期末考试化学试题
名校
4 . 短周期元素 a~g 在表中的位置如右表,请回答下列问题:
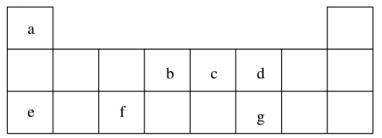
(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)__________ ;b、c两元素非金属性较强的是(写元素符号)_________ ,写出能证明这一结论的一个化学方程式_____________ 。
(2)下列有关说法正确的是( )
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)_______ (填“=”、 “>”或“<”)0.1 mol·L-1盐S中c(ca4+)。
②R常用作净水剂,其原理为(用离子方程式表示)______________ 。
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是_____________ 。
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:_____________ 。

(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)
(2)下列有关说法正确的是
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)
②R常用作净水剂,其原理为(用离子方程式表示)
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:
您最近一年使用:0次
2017-10-21更新
|
707次组卷
|
3卷引用:四川省成都市第七中学2017-2018学年高二上学期第一次月考化学试题
名校
解题方法
5 . 1869年俄国化学家门捷列夫制出第一张元素周期表元素,下图是元素周期表的一部分。回答下列问题:
(1)Ga的原子结构示意图为________ 。
(2)Ge位于金属元素和非金属元素的分界处,可以做________ 材料,其最高正价为________ 。
(3)Cl元素的最高价氧化物对应的水化物为________ (填化学式),设计实验方案证明Cl的得电子能力强于S。
(4)Bi的最高价氧化物为________ (填化学式), ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的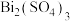 ,该反应的离子方程式为
,该反应的离子方程式为________ 。
(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为________ (填名称),该物质的电子式为________ 。
②氢化物的还原性:
________  (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。
③ 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为________ 。
④ 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为________ (用离子符号表示)。
B | C | N | O | F |
Al | Si | P | S | Cl |
Ga | Ge | As | Se | Br |
In | Sn | Sb | Te | I |
Tl | Pb | Bi | Po | At |
(2)Ge位于金属元素和非金属元素的分界处,可以做
(3)Cl元素的最高价氧化物对应的水化物为
(4)Bi的最高价氧化物为
 ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的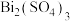 ,该反应的离子方程式为
,该反应的离子方程式为(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为
②氢化物的还原性:

 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。③
 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为④
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为
您最近一年使用:0次
6 . 元素在周期表中的位置反映了元素的原子结构和元素的性质。针对下表中的①~⑩种元素,回答以下问题:

(1)第三周期金属元素中原子半径最小的元素为________ (写序号);表中的X元素在第________ 周期第________ 族。
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为________ 、________ ;
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:________________ ;
(4)用电子式表示②与⑦形成化合物的过程:________________ ;
(5)由①②⑤元素组成的化合物的化学键类型为________ 、________ ;
(6)写出能证明②的金属性强于③的化学事实________ (任写一条)。

(1)第三周期金属元素中原子半径最小的元素为
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:
(4)用电子式表示②与⑦形成化合物的过程:
(5)由①②⑤元素组成的化合物的化学键类型为
(6)写出能证明②的金属性强于③的化学事实
您最近一年使用:0次
解题方法
7 . 几种元素在周期表中的位置如图所示,用化学用语(特殊标记的除外)回答下列问题:
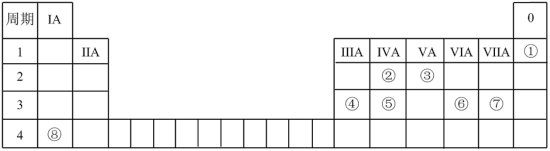
(1)表中所列元素中,①的元素符号是_______ ;金属性最强的是_______ ,该元素在周期表中的位置是_______ 。
(2)②有多种同素异形体,例如足球烯和_______ (填名称)
(3)元素③单质的化学式为_______ ;④的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
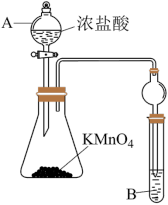
(4)已知 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为_______ ,仪器B中盛放淀粉-碘化钾溶液,所发生的离子反应方程式为_______ ,当观察到_______ 现象时,即可证明非金属性: 。
。

(1)表中所列元素中,①的元素符号是
(2)②有多种同素异形体,例如足球烯和

(3)元素③单质的化学式为
 溶液反应的化学方程式为
溶液反应的化学方程式为(4)已知
 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为 。
。
您最近一年使用:0次
解题方法
8 . 下表列出了9种元素在元素周期表中的位置示意图。
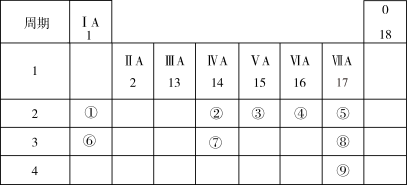
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______________ 。
(2)画出元素⑧形成的简单离子的结构示意图_______________ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______________ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______________ 。
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是______________ (填化学式),写出元素⑤的单质与水反应的化学方程式_______________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______________ 。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
名校
解题方法
9 . 填空题
(一)某同学欲验证 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:
依据上述实验设计,回答下列问题:
(1)铝元素在周期表中的位置为第______ 周期______ 族;
(2)上述实验试管 中的实验现象为
中的实验现象为_________________________ ;
(3)写出试管 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式______________________ ;
(4)上述实验现象证明碱性:
______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(二)某同学欲验证 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:
Ⅰ.向盛有 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;
Ⅱ.向盛有淀粉 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;
(5) 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为____________
(6)试管 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是______________________________
(7)写出试管 中发生的离子反应
中发生的离子反应______________________________
(一)某同学欲验证
 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:实验操作 | 实验现象 | 反应或结论 |
Ⅰ.向试管 | ① |
|
Ⅱ.向试管 | 试管中先出现白色沉淀,后白色沉淀溶解 | ② |
(1)铝元素在周期表中的位置为第
(2)上述实验试管
 中的实验现象为
中的实验现象为(3)写出试管
 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式(4)上述实验现象证明碱性:

 (填“>”“<”或“=”)
(填“>”“<”或“=”) (二)某同学欲验证
 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:Ⅰ.向盛有
 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;Ⅱ.向盛有淀粉
 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;(5)
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(6)试管
 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是(7)写出试管
 中发生的离子反应
中发生的离子反应
您最近一年使用:0次
名校
10 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素②、③、⑥的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)②和④组成的物质中含有___________ 键,可以证明该化合物含有此类型化学键的实验事实为___________ 。
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质___________ (填“能”或“不能”)与A反应,说明推测的理由___________ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②和④组成的物质中含有
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质
您最近一年使用:0次

 溶液,再逐滴滴入
溶液,再逐滴滴入 溶液,再逐滴滴入
溶液,再逐滴滴入

