名校
1 . 据南方日报报道,广东省珠江第二大水系北江流域因当地矿业的开发,造成附近河底沉积物中铊含量严重超标,致使当地人“靠江不饮北江水”。铊(Tl)是某超导体材料的组成元素之一,Tl3+与Ag在酸性介质中发生反应Tl3++2Ag=Tl++2Ag+。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第____ 周期第______ 族。
(2)铊与下列某种元素位于同一主族,该元素是________ 。
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是______ (填序号)。
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是________ 。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第
(2)铊与下列某种元素位于同一主族,该元素是
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是
您最近一年使用:0次
2 . 钠、铝、铁三种金属元素中,_____ 是地壳中含量最高的金属元素,其在周期表中位于第____ 周期____ 族。
您最近一年使用:0次
2019高三·浙江·专题练习
3 . 如表所示是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
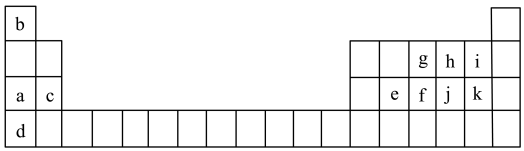
请你根据表中所给元素,回答下列问题:
(1)在所给短周期元素中____ 的原子半径与_____ 的原子半径之比最小 (填元素符号)。
(2)表中金属性最强的元素与氧气反应生成化合物的化学式是________ (填两种即可),i和j氢化物比较,稳定性强的是________ (填写氢化物化学式)。
(3)海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,其单质能做消毒杀菌剂的原因是____________________________________ (用化学方程式表示)。
(4)写出均由a、b、h、j四种元素所形成的两种化合物的水溶液相互反应的离子方程式:_____________ 。
(5)常温下某液态化合物只含上述元素的两种,分子中原子个数比1∶1,请你仅用一个化学方程式表示该液态化合物既有氧化性又有还原性:____________________________ 。

请你根据表中所给元素,回答下列问题:
(1)在所给短周期元素中
(2)表中金属性最强的元素与氧气反应生成化合物的化学式是
(3)海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,其单质能做消毒杀菌剂的原因是
(4)写出均由a、b、h、j四种元素所形成的两种化合物的水溶液相互反应的离子方程式:
(5)常温下某液态化合物只含上述元素的两种,分子中原子个数比1∶1,请你仅用一个化学方程式表示该液态化合物既有氧化性又有还原性:
您最近一年使用:0次
名校
4 . 填写下列空白:
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为_________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)周期表中最活泼的非金属元素位于第_____________ 纵行。
(4)所含元素为18种的周期是第____________ 周期。
(5)4g D2和20g 18O的单质化合时最多能生成_______ g D2O,这些D2O分子中含___ mol中子。
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为______________ 。
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为
(2)周期表中位于第8纵行的铁元素属于第
(3)周期表中最活泼的非金属元素位于第
(4)所含元素为18种的周期是第
(5)4g D2和20g 18O的单质化合时最多能生成
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为
您最近一年使用:0次
名校
5 . 人体含氧65%、碳18%、氢10%、氮3%、钙1.5%、磷1%、钾0.35%、硫0.25%、钠0.15%、氯0.15%、镁0.05%,它们被称为人体常量元素。
(1)人体的构成元素中,从周期表来看,元素数目最多的为________ 族。属于第三周期的非金属元素的原子半径由大到小的顺序________ 。
(2)上述元素中有两种在第ⅥA族,它们的活动性相比较_______ >_______ (用元素符号表示)。
(3)含量前3位的元素形成的一种有机物名称是__________ (写出一种即可)。
(1)人体的构成元素中,从周期表来看,元素数目最多的为
(2)上述元素中有两种在第ⅥA族,它们的活动性相比较
(3)含量前3位的元素形成的一种有机物名称是
您最近一年使用:0次
真题
解题方法
6 . 金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数) 。
。
(1) 元素在周期表中位置是
元素在周期表中位置是_______ ,其原子结构示意图_______ ;
(2) 与最活跃的非金属元素A形成化合物D,D的电子式为
与最活跃的非金属元素A形成化合物D,D的电子式为_______ ;
(3)配平用钙线氧脱磷的化学方程式:
___ P +___ FeO +____ CaO
____ Ca3(PO4)2+____ Fe;
(4)将钙线试样溶于稀盐酸,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测Mn+的方法是_______ (用离子方程式表达);
(5)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3_______ g。
 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数) 。
。(1)
 元素在周期表中位置是
元素在周期表中位置是(2)
 与最活跃的非金属元素A形成化合物D,D的电子式为
与最活跃的非金属元素A形成化合物D,D的电子式为(3)配平用钙线氧脱磷的化学方程式:

(4)将钙线试样溶于稀盐酸,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测Mn+的方法是
(5)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3
您最近一年使用:0次
2016-12-09更新
|
89次组卷
|
3卷引用:2010年普通高等学校招生全国统一考试理综化学部分(重庆卷)
7 . 元素周期表是学习和研究化学的重要工具。下列是元素周期表的部分信息:
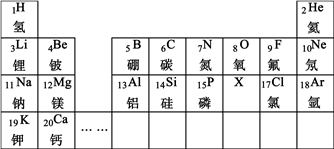
(1)地壳中含量最多的金属元素的原子序数是____________ 。
(2)分析上表规律,可推知,表中X的元素符号为____________ 。
(3)Ca在元素周期表中的位置为____________ 。
(4)写出一种由原子序数1、7、17三种元素组成化合物的化学式:__________ 。

(1)地壳中含量最多的金属元素的原子序数是
(2)分析上表规律,可推知,表中X的元素符号为
(3)Ca在元素周期表中的位置为
(4)写出一种由原子序数1、7、17三种元素组成化合物的化学式:
您最近一年使用:0次
8 . 下图是元素周期表的一部分,表中的①~⑨中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为___________ 。
(2)地壳中含量最多的金属元素是_____________________________ 。
(3)②与④形成的化合物的电子式______________________________ 。
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是___________ ,碱性最强的是____________ ,呈两性的氢氧化物是__________________ 。
 族 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)地壳中含量最多的金属元素是
(3)②与④形成的化合物的电子式
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
2017-12-01更新
|
200次组卷
|
2卷引用:河北省唐山市滦县二中2017-2018学年高二期中考试化学(文)试卷
9 . 下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次
10 . 针对下面10种元素,完成以下各小题
(1)地壳中含量最多的元素是___________ (填名称)。
(2)化学性质最不活泼的元素是___________ (填元素符号)。
(3)Al的原子结构示意图为___________________ 。
(4)C与N相比,原子半径较小的是___________ 。
(5)最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________ 。
(7)S和Cl相比,元素非金属性较强的是___________ 。
(1)地壳中含量最多的元素是
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Al | Si | S | Cl | Ne |
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
您最近一年使用:0次



