13-14高一·全国·课时练习
名校
1 . (1)1807年,英国化学家戴维在研究中发现:电解条件下可把水分解成H2和O2。他设想用电解的方法从KOH、NaOH中分离出K和Na。最初,戴维用饱和KOH溶液进行电解,不料还是得到H2和O2。这时,他考虑在无水条件下继续这项实验,但是,实验中产生的金属液珠一接触空气就立即燃烧起来;这时,他又考虑在________ 条件下电解熔融的KOH继续实验,最后他终于成功地得到了银白色的金属钾。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第________ 周期________ 族。
Ⅱ.关于铷的下列说法中正确的是________ (填序号,下同)。
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳 ③Rb2O2与水能剧烈反应并释放出O2④它是极强的还原剂 ⑤RbOH的碱性比同浓度的NaOH弱
Ⅲ.现有铷和另一种碱金属形成的合金5g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱金属可能是________ (填元素符号)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第
Ⅱ.关于铷的下列说法中正确的是
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳 ③Rb2O2与水能剧烈反应并释放出O2④它是极强的还原剂 ⑤RbOH的碱性比同浓度的NaOH弱
Ⅲ.现有铷和另一种碱金属形成的合金5g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱金属可能是
您最近一年使用:0次
11-12高一下·甘肃武威·阶段练习
名校
2 . 下表标出的是元素周期表的一部分元素,回答下列问题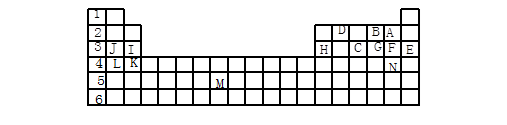
(1) 表中用字母标出的15种元素中,化学性质最不活泼的是__________ (用元素符号表示,下同),金属性最强的是_________ ,非金属性最强的是_________ ,常温下单质为液态的非金属元素是________ ,属于两性元素的是_______ 属于过渡元素的是_______ (该空用字母表示)。
(2) B、F、C气态氢化物的化学式分别为____ 、_____ 、_____ ,其中以_______ 最不稳定。
(3) 第三周期中原子半径最小的是________ (用元素符号表示)。
(4) 写出B、F、J所形成的化合物的电子式_________ 。

(1) 表中用字母标出的15种元素中,化学性质最不活泼的是
(2) B、F、C气态氢化物的化学式分别为
(3) 第三周期中原子半径最小的是
(4) 写出B、F、J所形成的化合物的电子式
您最近一年使用:0次
9-10高二下·吉林·期中
3 . A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: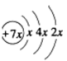 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A_________ B__________ C __________ D __________
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是__________ ,碱性最强的是_________ 。
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是__________ ,电负性最大的元素是__________ 。
(4)D的氢化物比C的氢化物的沸点__________ (填"高"或"低"),原因_____________
(5)E元素原子的核电荷数是__________ ,E元素在周期表的第_______ 周期,第________ 族,已知元素周期表可按电子排布分为s区、p区等,则E元素在_______ 区。
(6)A、B、C最高价氧化物的晶体类型是分别是______ 晶体、______ 晶体、_____ 晶体。
(7)画出D的核外电子排布图_____________________ ,这样排布遵循了_______ 规则。
(8)用电子式表示B的硫化物的形成过程:______________________________________
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
(8)用电子式表示B的硫化物的形成过程:
您最近一年使用:0次
11-12高三上·福建三明·阶段练习
4 . 下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,用化学用语回答下列问题:
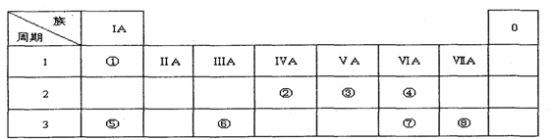
I.(1)请画出元素⑧的离子结构示意图_______________ 。
(2)元素⑦中质子数和中子数相等的同位素符号是_____________ 。
(3)④、⑤、⑦的原子半径由大到小的顺序为_________________ 。(用半径符号表示)
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为_____________ >___________ 。
II.由表中①~⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:
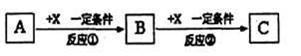
(1)若X是强氧化性单质,则A不可能是___________ (填序号)。
a.S b.N2 c.C d.Al
(2)若A是饮食中的有机物,B与C分子量相差16,则写出A与C反应的方程式,并指出反应类型_____________________________________________________
(3)若A、B、C为含有同一非金属元素的非电解质,写出符合上述关系A转化为B的化学方程式:_______________________________________

I.(1)请画出元素⑧的离子结构示意图
(2)元素⑦中质子数和中子数相等的同位素符号是
(3)④、⑤、⑦的原子半径由大到小的顺序为
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为
II.由表中①~⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:

(1)若X是强氧化性单质,则A不可能是
a.S b.N2 c.C d.Al
(2)若A是饮食中的有机物,B与C分子量相差16,则写出A与C反应的方程式,并指出反应类型
(3)若A、B、C为含有同一非金属元素的非电解质,写出符合上述关系A转化为B的化学方程式:
您最近一年使用:0次
11-12高三上·湖北武汉·阶段练习
5 . 下表为元素周期表的一部分,请参照元素①一⑩在周期表中的位置,用元素符号或化学式回答下列问题。
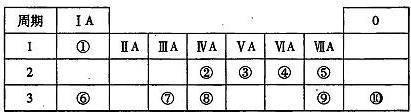
(1)⑤、⑥、⑦的原子半径由大到小的顺序___________ 。
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是_____________ 。
(3)①、④、⑥、⑨中的某些元素可以形成既含有离子键又含有共价键的化合物,写出其中两种不同类别物质的化学式_________ 、___________ 。
(4)上表中所列出的部分元素能形成多种带有18个电子的分子,请写出其中三种的化学式
_____________ 。

(1)⑤、⑥、⑦的原子半径由大到小的顺序
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑥、⑨中的某些元素可以形成既含有离子键又含有共价键的化合物,写出其中两种不同类别物质的化学式
(4)上表中所列出的部分元素能形成多种带有18个电子的分子,请写出其中三种的化学式
您最近一年使用:0次
10-11高一下·海南·期末
6 . 四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题:
(1)元素Z位于周期表中第_______ 周期,_______ 族;
(2)这些元素的氢化物中,水溶液碱性最强的是_____________ (写化学式);
(3)XW2的电子式为________________________ ;
(4)Y的最高价氧化物的化学式为_________________ 。
| X | Y | |
| Z | W |
请回答下列问题:
(1)元素Z位于周期表中第
(2)这些元素的氢化物中,水溶液碱性最强的是
(3)XW2的电子式为
(4)Y的最高价氧化物的化学式为
您最近一年使用:0次
2011-07-27更新
|
956次组卷
|
5卷引用:2014-2015河南省南阳方城一中高一下学期学期第一次月考化学试卷
2014-2015河南省南阳方城一中高一下学期学期第一次月考化学试卷(已下线)2010—2011学年海南中学高一第二学期期末考试(2-20班)化学试卷(已下线)2013-2014学年海南省海南中学第二学期高一期末考试化学试卷(已下线)2015届陕西省宝鸡市岐山县高三上学期期中考试化学试卷甘肃省玉门一中2018-2019学年高一下学期期末考试化学试题
10-11高一下·江西吉安·期中
7 . (1)X元素的原子核外有2个电子层,其中L层有5个电子,该元素在周期表中的位置是_________________________ ,最高价氧化物的化学式为___________ ,该元素的氢化物和最高价氧化物对应的水化物反应的化学方程式为_____________________________ 。
(2)Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO3,则此时Y元素的化合价为____________ ,Y原子的最外层电子数为_________ ,其气态氢化物的化学式为____________ 。
(2)Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO3,则此时Y元素的化合价为
您最近一年使用:0次
2011-05-09更新
|
1123次组卷
|
5卷引用:2016-2017学年吉林省汪清县第六中学高一3月月考化学试卷
2016-2017学年吉林省汪清县第六中学高一3月月考化学试卷(已下线)2010-2011学年江西省安福中学高一下学期期中考试化学试卷(已下线)同步君 必修2 第1章 第2节 元素周期表和元素周期律的应用高中化学人教版 必修2 第一章 物质结构 元素周期律 第二节 元素周期律 元素周期表和元素周期律的应用(已下线)4.2.2 元素周期表和元素周期律的应用练习(1)——《高中新教材同步备课》(人教版 必修第一册)
10-11高一下·北京房山·阶段练习
8 . 指出下列元素在周期表中的位置:
①Ne:___ 周期______ 族; ②C:____ 周期_______ 族;
③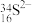 微粒中的质子数是
微粒中的质子数是_______ ,中子数是_______ ,核外电子数是_______ 。
①Ne:
③
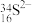 微粒中的质子数是
微粒中的质子数是
您最近一年使用:0次
10-11高二下·河南郑州·阶段练习
9 . (1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第_______ 周期____ 族;最高价氧化物的化学式为__________ ,砷酸钠的化学式是__________ 。
(2)已知下列元素在周期表中的位置,写出它们价电子排布式和元素符号:
①第4周期ⅣB族_____________________________________ ;
②第5周期ⅦA族___________________________________ 。
(2)已知下列元素在周期表中的位置,写出它们价电子排布式和元素符号:
①第4周期ⅣB族
②第5周期ⅦA族
您最近一年使用:0次
10-11高三·河北衡水·阶段练习
10 . 下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语作答:
(1)④、⑤、⑦的原子半径由大到小的顺序为____________ 。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_________________ 。
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
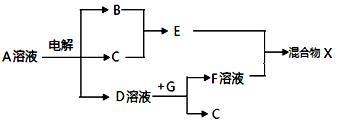
①写出电解A溶液的化学方程式______________________________________ 。
②若上图中各步反应均为完全转化,则混合物X中含有的物质有____________ 。
(4)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为___________ ,②其氢化物的化学式为____________ 。
③Y由②⑤⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为___________________ 。
I A | 0 | ||||||
① | II A | III A | IV A | V A | VI A | VII A | |
② | ④ | ||||||
⑤ | ③ | ⑧ | ⑥ | ⑦ |
(1)④、⑤、⑦的原子半径由大到小的顺序为
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出电解A溶液的化学方程式
②若上图中各步反应均为完全转化,则混合物X中含有的物质有
(4)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为
③Y由②⑤⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
您最近一年使用:0次



