解题方法
1 . 下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
您最近一年使用:0次
名校
2 . 氮元素及其化合物的转化关系如图所示。___________ 。
(2)氮元素在元素周期表中的位置是___________ 。
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是___________ 。
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。___________ 。
②催化转化过程中,理论上每生成1mol 时,转移的电子为
时,转移的电子为___________ mol。
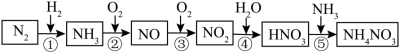
(2)氮元素在元素周期表中的位置是
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。
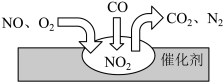
②催化转化过程中,理论上每生成1mol
 时,转移的电子为
时,转移的电子为
您最近一年使用:0次
2024-05-06更新
|
59次组卷
|
2卷引用:江苏省扬州市邗江中学2023-2024学年高一下学期三月检测化学试题
名校
3 . 下表为元素周期表的一部分,用化学用语回答下列问题:___________ 。
(2)⑥、⑦、⑧、③的简单离子的半径由大到小顺序为___________ 。(写离子符号)
(3)元素③、⑤、⑧组成的化合物是84消毒液的主要成分,可以在碱性条件下处理CN-,将CN-氧化成CO 和N2,写出反应的离子方程式
和N2,写出反应的离子方程式___________ 。
(4)将⑤和⑥单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积___________ L。最终获得溶液的物质的量浓度为___________ mol/L。
(2)⑥、⑦、⑧、③的简单离子的半径由大到小顺序为
(3)元素③、⑤、⑧组成的化合物是84消毒液的主要成分,可以在碱性条件下处理CN-,将CN-氧化成CO
 和N2,写出反应的离子方程式
和N2,写出反应的离子方程式(4)将⑤和⑥单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
名校
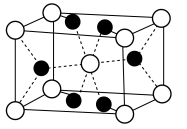
4 . 氢化镁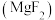 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。
I.氟化镁晶胞是长方体,其结构如图所示:_______ 区(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(2) 晶胞示意图中:离子半径:
晶胞示意图中:离子半径: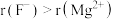 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:_____ 。
II.一种由 制备
制备 的工艺流程如图
的工艺流程如图
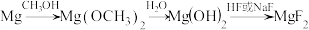
已知:ⅰ. 易溶于甲醇;
易溶于甲醇;
ⅱ.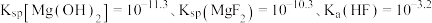
(3)上述流程中,可循环利用的物质是_______ 。
(4)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
 小组同学预测化学反应速率:①
小组同学预测化学反应速率:① ②,理由是甲基为
②,理由是甲基为_______ 基团,导致 键极性:
键极性: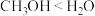 。
。
 实验表明化学反应速率:①
实验表明化学反应速率:① ②,分析其原因可能是
②,分析其原因可能是_______ 。
(5)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: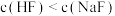 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:_______ 。
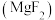 晶体广泛应用在光学、冶金、国防、医疗等领域。
晶体广泛应用在光学、冶金、国防、医疗等领域。I.氟化镁晶胞是长方体,其结构如图所示:
 ”“
”“ ”或“
”或“ ”)。
”)。(2)
 晶胞示意图中:离子半径:
晶胞示意图中:离子半径: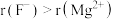 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:II.一种由
 制备
制备 的工艺流程如图
的工艺流程如图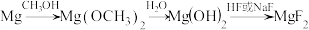
已知:ⅰ.
 易溶于甲醇;
易溶于甲醇;ⅱ.
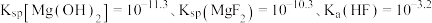
(3)上述流程中,可循环利用的物质是
(4)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。 小组同学预测化学反应速率:①
小组同学预测化学反应速率:① ②,理由是甲基为
②,理由是甲基为 键极性:
键极性: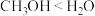 。
。 实验表明化学反应速率:①
实验表明化学反应速率:① ②,分析其原因可能是
②,分析其原因可能是(5)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: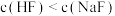 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次
名校
解题方法
5 . 元素周期律反映了元素性质的周期性变化规律。
(1)氮氧化铝(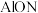 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是___________ 。
(2)在元素周期表中, ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:___________ 。
(3)锡为主族元素,其原子结构示意图: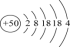 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是___________ , 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:___________ 。
(4)硒 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式:___________ 。理论上该反应每转移 电子,可得到的
电子,可得到的 的质量为
的质量为___________ g。
(1)氮氧化铝(
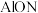 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是(2)在元素周期表中,
 ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:(3)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:(4)硒
 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式: 电子,可得到的
电子,可得到的 的质量为
的质量为
您最近一年使用:0次
名校
6 . 按下列要求填空
(1)基态某原子的最外层电子排布式是 ,推断该元素位于第
,推断该元素位于第_____ 周期第____ 族,在元素周期表中属于____ 区。
(2)基态某原子的价层电子排布式为 ,在元素周期表中属于
,在元素周期表中属于_______ 区。
(3) 杂化类型为
杂化类型为_______ ,VSEPR模型为_______ ,离子空间构型为_______ 。
(1)基态某原子的最外层电子排布式是
 ,推断该元素位于第
,推断该元素位于第(2)基态某原子的价层电子排布式为
 ,在元素周期表中属于
,在元素周期表中属于(3)
 杂化类型为
杂化类型为
您最近一年使用:0次
7 . 回答下列问题
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是________ ,基态Mo原子核外有________ 种不同运动状态的电子,其中核外电子占据最高电子层的符号是________ 。
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知: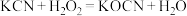 ,回答下列问题:
,回答下列问题:
 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为________ (用元素符号表示,下同),电负性从大到小的顺序为________ ,基态氮原子外围电子排布式为________ 。
(1)金属钼(Mo)常用于工业、军事等领域,已被多个国家列为战略金属,我国的钼储量居世界第二。已知钼在元素周期表中呈现的信息如下,回答下列问题:
钼在元素周期表中的位置是
(2)氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知:
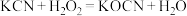 ,回答下列问题:
,回答下列问题: 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为
您最近一年使用:0次
名校
解题方法
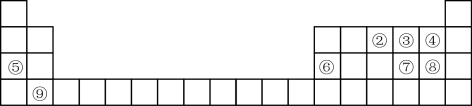
8 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_______ 。
(3)非金属性e强于g,用原子结构解释原因:_______ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_______ (填序号)。
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | |||||||
| 3 | b | c | d | e | ||||
| 4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因:
(4)下列对f及其化合物的推断中,正确的是
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
您最近一年使用:0次
9 . 结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
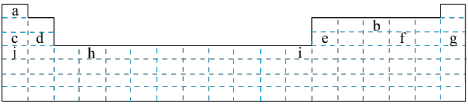
(2)f元素位于第
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
| A.比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e |
| B.比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j<c<d<e |
| C.比较四种元素形成的单质分别与非氧化性酸反应置换氢气的剧烈程度:c>j>d>e |
| D.将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e |
您最近一年使用:0次
名校
解题方法
10 . 1869年俄国化学家门捷列夫制出第一张元素周期表元素,下图是元素周期表的一部分。回答下列问题:
(1)Ga的原子结构示意图为________ 。
(2)Ge位于金属元素和非金属元素的分界处,可以做________ 材料,其最高正价为________ 。
(3)Cl元素的最高价氧化物对应的水化物为________ (填化学式),设计实验方案证明Cl的得电子能力强于S。
(4)Bi的最高价氧化物为________ (填化学式), ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的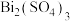 ,该反应的离子方程式为
,该反应的离子方程式为________ 。
(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为________ (填名称),该物质的电子式为________ 。
②氢化物的还原性:
________  (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。
③ 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为________ 。
④ 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为________ (用离子符号表示)。
B | C | N | O | F |
Al | Si | P | S | Cl |
Ga | Ge | As | Se | Br |
In | Sn | Sb | Te | I |
Tl | Pb | Bi | Po | At |
(2)Ge位于金属元素和非金属元素的分界处,可以做
(3)Cl元素的最高价氧化物对应的水化物为
(4)Bi的最高价氧化物为
 ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的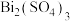 ,该反应的离子方程式为
,该反应的离子方程式为(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为
②氢化物的还原性:

 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。③
 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为④
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为
您最近一年使用:0次



