名校
1 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是_______ 。
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是_______ (填化学式;用“>”连接)。
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断_______ (填“正确”或“错误”);根据元素周期律,自然界中最强的碱是_______ (填化学式)。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ |
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断
您最近一年使用:0次
2023-01-16更新
|
426次组卷
|
4卷引用:安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题
安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题山东省莘县多校2022-2023学年高一上学期期末线上联考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷
名校
解题方法
2 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图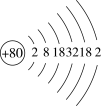 汞在第
汞在第___________ 周期。
(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷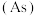 也是氮族元素。
也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是___________ (填序号)。
a、含有离子键和共价键
b、能与 溶液反应
溶液反应
c、与 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样
③砷酸 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)据汞的原子结构示意图
 汞在第
汞在第(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷
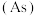 也是氮族元素。
也是氮族元素。①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是a、含有离子键和共价键
b、能与
 溶液反应
溶液反应c、与
 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样③砷酸
 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:
您最近一年使用:0次
2022-12-28更新
|
141次组卷
|
2卷引用:河南省顶级名校2022-2023学年高三上学期12月摸底考试化学试题
解题方法
3 . 下图是元素周期表的一部分。按要求填写下列空白:
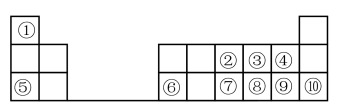
(1)元素⑦在周期表中的位置可表示为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物的电子式为_______ ;⑧的氢化物的结构式为_______
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置可表示为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物的电子式为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2022-12-21更新
|
351次组卷
|
2卷引用:海南省北京师范大学海口附属学校2020-2021学年高一下学期月考化学试题
解题方法
4 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第_______ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(4)Na的最高价氧化物对应的水化物的化学式为_______ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物对应的水化物的化学式为
您最近一年使用:0次
解题方法
5 . 按要求完成下列填空
(1)写出KOH电子式_______ ;写出CO2的结构式_______
(2)短周期主族元素中周期序数和族序数相等的元素有_______ (填元素符号)
(3)用电子式表示下列化合物的形成过程H2S:_______ ;MgF2:_______ 。
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为_______ 。
(1)写出KOH电子式
(2)短周期主族元素中周期序数和族序数相等的元素有
(3)用电子式表示下列化合物的形成过程H2S:
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为
您最近一年使用:0次
名校
解题方法
6 . 元素①-⑥在元素周期表中的位置如下,按要求填空
回答下列问题:
(1)元素①的名称和符号为:_______ 。
(2)元素②的一种中子数为8的核素可用作分析古代人类食物结构,写出其原子符号_______ 。
(3)元素③-⑥中,原子半径最小的是_______ (填元素符号)。
(4)元素的非金属性:⑤_______ ⑥(填“>”、“<”或“=”),若通过实验事实证明上述结论,利用适当的文字与化学用语进行概述:_______ (写出2条)
(5)常温下,元素④的最高价氧化物的水化物可溶于③的最高价氧化物对应的水化物浓溶液中,其对应的化学方程式为_______ 。
| IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ① | ② | ||||||
| 第3周期 | ③ | ④ | ⑤ | 6 | ||||
| 第4周期 | ⑦ |
回答下列问题:
(1)元素①的名称和符号为:
(2)元素②的一种中子数为8的核素可用作分析古代人类食物结构,写出其原子符号
(3)元素③-⑥中,原子半径最小的是
(4)元素的非金属性:⑤
(5)常温下,元素④的最高价氧化物的水化物可溶于③的最高价氧化物对应的水化物浓溶液中,其对应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 填空或写出下列反应的离子方程式:
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和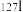 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为_________ 。碘元素在元素中位于第__________ 周期第__________ 族。
(2)向明矾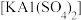 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:________________ 。
(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)______ 。
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是________________ 。
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是________________ 。
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为
 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和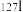 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为(2)向明矾
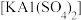 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是
您最近一年使用:0次
名校
解题方法
8 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p的原子结构示意图为___________________ 。
(2)o、p两元素的部分电离能数据如下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_________________________________________________________ 。
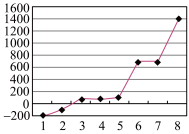
(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是___________________ (填图1中的序号)。
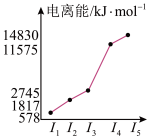
(4)表中所列的某主族元素的电离能情况如图所示,则该元素是___________________ (填元素符号)。
(5)基态钒原子的价电子排布图为___________________ 。
(6)写出单电子数最多的原子的电子排布式:__________________________________________ 。
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
(1)元素p的原子结构示意图为
(2)o、p两元素的部分电离能数据如下表:
元素 元素电离能/  | o | p |
| 717 | 759 |
| 1509 | 1561 |
| 3248 | 2957 |
比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图所示,则该元素是

(5)基态钒原子的价电子排布图为
(6)写出单电子数最多的原子的电子排布式:
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
A.[Ne]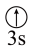 | B.[Ne]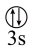 | C.[Ne]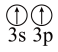 | D.[Ne]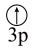 |
您最近一年使用:0次
9 . 根据以下9种元素在元素周期表中的位置,回答下列问题:
(1)①的原子轨道形状是_______ ;②③④的第一电离能由大到小的顺序是_______ (填编号)。
(2)下列可以判断⑤和⑥金属性强弱的是_______ (填序号)。
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式_______ ,它的熔点高,硬度大,电绝缘性好,化学性质稳定。它的晶体类型是_______ ,试推测其可能有哪些用途_______ (填序号)。
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式
您最近一年使用:0次
解题方法
10 . 写出元素周期表中前20号元素的符号______
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
您最近一年使用:0次




