1 . 下表列出了A~R九种元素在元素周期表中的位置:
(1)A的最高价氧化物对应水化物的电子式___________ ,核内有10个中子的F的核素表示为___________ ;H的最高价氧化物对应水化物的化学式___________ ,以上元素其中化学性质最不活泼的是___________ (填元素符号)。
(2)A、B、C三种元素按原子半径由大到小的顺序排列为___________ (用元素符号表示)。
(3)E、F元素最简单氢化物中稳定性最强的化学式是___________ ,该氢化物在常温下跟A发生反应的化学方程式是___________ 。
(4)D、B两种元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(5)关于元素周期表、周期律,下列说法正确的是___________(填字号)
| 周期 | IA | IIA | IIIA | IV A | VA | VIA | VIIA | 0 | |
| 族 | |||||||||
| 2 | E | F | |||||||
| 3 | A | C | D | G | H | R | |||
| 4 | B |
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
(3)E、F元素最简单氢化物中稳定性最强的化学式是
(4)D、B两种元素的最高价氧化物对应的水化物发生反应的离子方程式是
(5)关于元素周期表、周期律,下列说法正确的是___________(填字号)
| A.在金属和非金属分界处可以找到半导体材料 |
| B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素 |
| C.通常农药所含有的元素位于元素周期表左下方区域 |
| D.稀有气体原子都满足8电子稳定结构 |
您最近一年使用:0次
解题方法
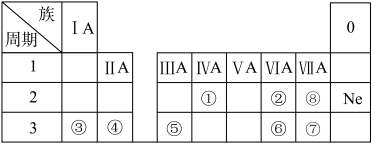
2 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
①___________ ;⑤___________ ;⑦___________ ;⑧___________ 。
(2)②和③元素所组成的化合物中可做供氧剂的是___________ (写化学式)。
(3)⑥元素的原子结构示意图为___________ 。②元素的原子结构示意图为___________ 。
(4)①元素的氧化物中是酸性氧化物的是___________ (写化学式)。
①
(2)②和③元素所组成的化合物中可做供氧剂的是
(3)⑥元素的原子结构示意图为
(4)①元素的氧化物中是酸性氧化物的是
您最近一年使用:0次
名校
3 . 结合下图所示元素周期表,回答下列问题:

(1)表中所列元素,属于短周期元素的有___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:___________ 、___________ 、___________ 。

(1)表中所列元素,属于短周期元素的有
(2)f元素位于第
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:
您最近一年使用:0次
名校
4 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:
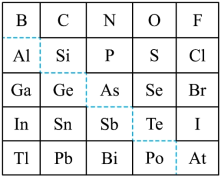
(1)元素Ga在元素周期表中的位置为:______ ;
(2)Sn的最高正价为______ ,C1的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是______ (写化学式),其电子式为______ 。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4______ H2SeO4(填“>”、<”、“=”或“无法比较”);
③氢化物的还原性:H2O______ H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N______ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
名校
5 . 据报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知Rb的原子序数为37。回答下列有关问题:
(1)Rb的原子结构示意图中共有______ 个电子层,最外层电子数为______ 。
(2)Rb在元素周期表中的位置是______ 。
(3)取少量铷单质加入水中,可观察到其剧烈反应,涉及反应的离子方程式为____________ 。
(1)Rb的原子结构示意图中共有
(2)Rb在元素周期表中的位置是
(3)取少量铷单质加入水中,可观察到其剧烈反应,涉及反应的离子方程式为
您最近一年使用:0次
名校
6 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的元素周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构。性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
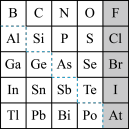
(1) 的结构示意图是
的结构示意图是___________ 。
(2)元素In在元素周期表中的位置是___________ 。
(3)P的最高价氧化物的化学式为___________ ,Al元素的最高价氧化物对应的水化物与S元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(4) 的中子数与电子数的差值是
的中子数与电子数的差值是___________ ;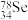 和
和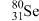 的物理性质
的物理性质___________ (填“相同”或“不同”),化学性质___________ (填“相同”或“不同”)。
(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是___________ 。
A.
B.
C.
②氢化物的还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)
 的结构示意图是
的结构示意图是(2)元素In在元素周期表中的位置是
(3)P的最高价氧化物的化学式为
(4)
 的中子数与电子数的差值是
的中子数与电子数的差值是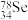 和
和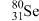 的物理性质
的物理性质(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是
A.

B.

C.

②氢化物的还原性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
7 . 人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
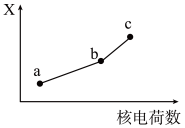
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2023-12-05更新
|
258次组卷
|
3卷引用:四川省眉山北外附属东坡外国语学校2023-2024学年高一下学期开学化学试题
名校
8 . 如图是元素周期表的一部分,A~J代表对应的元素,回答下列问题:
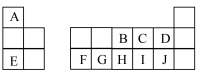
(1)F的元素符号为___________ ,元素C在周期表中的位置为___________ 。
(2)A、D和E三种元素的离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(4)A、B和J三种元素形成常见化合物所含化学键的类型是___________ 。
(5)下列说法错误的是___________ (填标号)。
a.单质的熔点:
b.简单氢化物的沸点:
c.氧化物对应水化物的酸性:
(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为___________ 。

(1)F的元素符号为
(2)A、D和E三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、B和J三种元素形成常见化合物所含化学键的类型是
(5)下列说法错误的是
a.单质的熔点:

b.简单氢化物的沸点:

c.氧化物对应水化物的酸性:

(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
2023-09-12更新
|
443次组卷
|
2卷引用:安徽省皖江名校联考2023-2024学年高二上学期开学化学试题
9 . 联合国将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,下表代表元素周期表前四周期,回答下列问题:

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中_____ 。
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为_____ 。
(3)下列有关性质的比较正确,且能用元素周期律解释的是___________ 。
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式___________ ;___________ 。
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为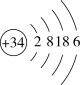 。
。
①Se在元素周期表中的位置是___________ 。
②Se的简单气态氢化物的化学式为___________ 。
③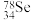 和
和 互称为
互称为___________ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为
(3)下列有关性质的比较正确,且能用元素周期律解释的是
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为
 。
。①Se在元素周期表中的位置是
②Se的简单气态氢化物的化学式为
③
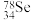 和
和 互称为
互称为
您最近一年使用:0次
名校
解题方法
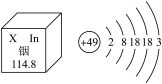
10 . 中国科学院院士___________ 主持测定了铟、铱、铕等种元素相对原子质量的新值。如图是铟元素在元素周期表中的信息和原子结构示意图,
___________ ,铟元素位于元素周期表的第___________ 周期。


您最近一年使用:0次



