解题方法
1 . 完成下列问题
(1)写出Ni的元素名称_______ , 该元素在周期表的位置为第_______ 周期,第_______ 族。
(2)基态Si原子的电子排布式为_______ ,基态S原子的电子排布式为_______ 。
(3)写出基态Fe原子的价层电子排布式:_______ 。
(1)写出Ni的元素名称
(2)基态Si原子的电子排布式为
(3)写出基态Fe原子的价层电子排布式:
您最近一年使用:0次
名校
解题方法
2 . 为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:
(1)①~⑦对应元素中,非金属性最强的元素名称是_______ ;⑤在周期表中的位置为_______ 。
(2)②与③形成化合物的电子式为_______ ;①的最高价氧化物的结构式为_______ 。
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (用化学式来回答)。
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是_______ (填对应的序号)。
| ① | ② | |||||||
| ③ | ④ | ⑤ | ||||||
| ⑥ | …… | ⑦ | ||||||
(2)②与③形成化合物的电子式为
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是
您最近一年使用:0次
2022-09-08更新
|
115次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期开学考试化学试题
名校
3 . 近年来,我国航空航天事业成果显著,“北斗三号”导航卫星搭载了精密计时的铷(Rb)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图1)。回答下列问题:

(1)下列说法错误的是_______(填字母)。
(2)Rb原子第一电子层上电子的能量比最外层上电子的能量_______ (填“低”或“高”)。
(3)如图2中 所示粒子共表示
所示粒子共表示_______ 种元素,铷元素原子的化学性质与如图中_______ (填字母)的化学性质相似。


(1)下列说法错误的是_______(填字母)。
A.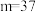 , ,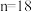 | B.铷是金属元素 |
| C.铷的相对原子质量是85.47 | D.铷原子有5个电子层,最外层有1个电子 |
(3)如图2中
 所示粒子共表示
所示粒子共表示
您最近一年使用:0次
2022-09-07更新
|
378次组卷
|
3卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题
4 . 回答下列问题:
(1)硼酸(H3BO3)为一元弱酸,电离方程式H3BO3+H2O H++B(OH)
H++B(OH) 。已知:H3BO3的电离常数Ka=5.8×10−10,H2CO3的电离常数Ka1=4.4×10−7、Ka2=4.7×10−11,向饱和硼酸溶液中滴加少量Na2CO3溶液,写出发生反应的离子方程式
。已知:H3BO3的电离常数Ka=5.8×10−10,H2CO3的电离常数Ka1=4.4×10−7、Ka2=4.7×10−11,向饱和硼酸溶液中滴加少量Na2CO3溶液,写出发生反应的离子方程式_______ 。
(2)已知戊烷(C5H12)的3种同分异构体的沸点数据如下表:
请从物质结构角度分析,正戊烷、异戊烷、新戊烷沸点依次降低的原因是_______ 。
(3)某第四周期元素位于元素周期表中的第六纵行,则该元素位于元素周期表中_______ 区(按电子排布分区),其基态原子的价电子轨道表达式为_______ 。
(1)硼酸(H3BO3)为一元弱酸,电离方程式H3BO3+H2O
 H++B(OH)
H++B(OH) 。已知:H3BO3的电离常数Ka=5.8×10−10,H2CO3的电离常数Ka1=4.4×10−7、Ka2=4.7×10−11,向饱和硼酸溶液中滴加少量Na2CO3溶液,写出发生反应的离子方程式
。已知:H3BO3的电离常数Ka=5.8×10−10,H2CO3的电离常数Ka1=4.4×10−7、Ka2=4.7×10−11,向饱和硼酸溶液中滴加少量Na2CO3溶液,写出发生反应的离子方程式(2)已知戊烷(C5H12)的3种同分异构体的沸点数据如下表:
| 正戊烷 | 异戊烷 | 新戊烷 | |
| 沸点/℃ | 36.1 | 27.9 | 9.5 |
(3)某第四周期元素位于元素周期表中的第六纵行,则该元素位于元素周期表中
您最近一年使用:0次
名校
5 . 下表是元素周期表的一部分,回答下列关问题:
(1)下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是_______ (填元素符号),简单离子半径最小的是_______ (填化学式)。
(3)④与⑧可以形成_______ (填离子或共价)化合物,请用电子式表示其形成过程:_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是
(3)④与⑧可以形成
您最近一年使用:0次
名校
解题方法
6 . 下表为元素周期表中的一部分,列出10种元素在周期表中的位置,用化学符号回答下列各题。
(1)10种元素中,化学性质最不活泼的是___________ 。
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物的化学式为___________ 。
(5)①和⑨两元素形成化合物的电子式为___________ :该化合物焰色试验为___________ 色。
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为___________ 。
| 主族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨两元素形成化合物的电子式为
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为
您最近一年使用:0次
2022-03-08更新
|
172次组卷
|
2卷引用:新疆乌苏市第一中学2021-2022学年高一下学期开学考试化学(A)试题
解题方法
7 . 下表是元素周期表的一部分,表中的每个编号代表一种短周期元素,回答下列问题:
(1)①和③两种元素形成化合物的电子式为___________ 。
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为___________ (用化学式表示)。
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为___________ 。
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为___________ 。
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和③两种元素形成化合物的电子式为
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式
您最近一年使用:0次
名校
8 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)金属性最强的是___________ (填元素名称)。
(2)⑨的离子结构示意图为___________ 。
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是___________ (填化学式)。
(4)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是___________ (填化学式)
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程___________ 。
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)⑨的离子结构示意图为
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是
(4)④、⑤、⑥的简单离子半径由大到小的顺序为
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为
您最近一年使用:0次
2022-01-22更新
|
527次组卷
|
3卷引用:湖北省麻城市实验高级中学2021-2022学年高一下学期2月迎春考化学试题
名校
9 . 下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
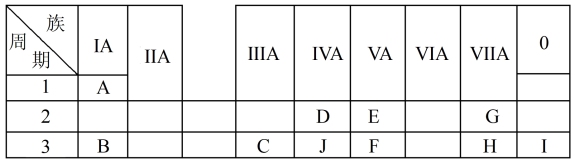
(1)表中元素,化学性质最不活泼的是_______ (填化学名称),只有负价而无正价的元素是_______ (填元素符号)。
(2)34号元素在元素周期表中的位置是_______ 。
(3)H最高价氧化物的化学式为_______ ,G和H氢化物中沸点更高的是_______ ,原因为:_______ 。
(4)A分别与E、G、H形成的化合物中,最稳定的是_______ 。
(5)在B、C、E、F中,原子半径最大的是_______ (填元素符号)。
(6)B、H两种元素所形成的化合物所含的化学键类型为_______ 。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:_______ 。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:_______ 。

(1)表中元素,化学性质最不活泼的是
(2)34号元素在元素周期表中的位置是
(3)H最高价氧化物的化学式为
(4)A分别与E、G、H形成的化合物中,最稳定的是
(5)在B、C、E、F中,原子半径最大的是
(6)B、H两种元素所形成的化合物所含的化学键类型为
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
2021高一·全国·专题练习
名校
10 . 下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
您最近一年使用:0次
2021-12-06更新
|
1082次组卷
|
4卷引用:浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题
浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题(已下线)专题4.2.1 元素性质的周期性变化规律(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题



