解题方法
1 . 如图1是一些微粒的结构示意图和硒元素的相关信息,回答下列问题:
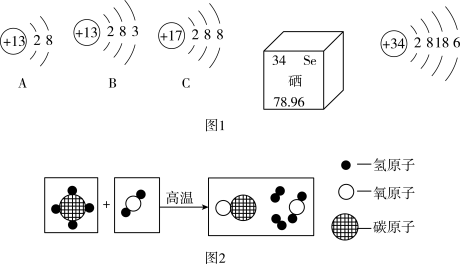
(1)A、B、C 中属于阳离子的是___ ,其离子符号为___ 。
(2)硒元素属于___ (填“金属”或“非金属”)元素,硒元素和钠元素组成化合物的化学式为____ 。
(3)如图2是某个反应的微观示意图:
①请将图示后两个方框中的微观粒子示意图补画完全,使反应成立___________ 。
②请用化学方程式表示该反应_______________________ 。

(1)A、B、C 中属于阳离子的是
(2)硒元素属于
(3)如图2是某个反应的微观示意图:
①请将图示后两个方框中的微观粒子示意图补画完全,使反应成立
②请用化学方程式表示该反应
您最近一年使用:0次
解题方法
2 . 元素周期表是学习化学的重要工具,下表是元素周期表的一部分,请回答下列问题:
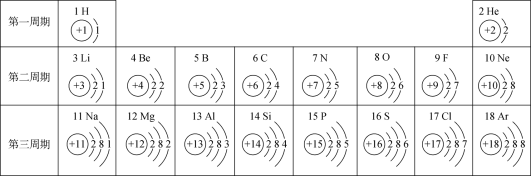
(1)不同元素之间的最本质区别是_________ 不同;
(2)表中与氧元素化学性质相似的是_______ 元素;
(3)12号元素的原子在化学反应中比较容易_____ (填“得到”或“失去”)电子;
(4)11﹣18号元素在表中处于同一周期的原因是它们原子结构中的_____ 相同。

(1)不同元素之间的最本质区别是
(2)表中与氧元素化学性质相似的是
(3)12号元素的原子在化学反应中比较容易
(4)11﹣18号元素在表中处于同一周期的原因是它们原子结构中的
您最近一年使用:0次
2020-08-06更新
|
45次组卷
|
2卷引用:开学考试化学试卷04——2020年秋季高一新生入学分班考试化学试卷(全国通用)
3 . 化学的学科特征是在原子、分子水平上研究物质和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al原子结构图Na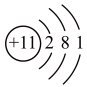 、Al
、Al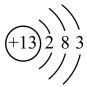 可推知,金属Na、Al的化学性质不同的原因是
可推知,金属Na、Al的化学性质不同的原因是_____________________________ 。
②CO和CO2化学性质不同的原因是_____________ 。
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是___________________________ 。
(2)如图是氢气在氧气中燃烧的微观示意图(图中“o”代表氢原子。“●”代表氧原子)。
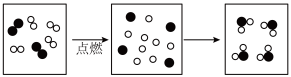
①参加该化学反应的最小粒子是_____________ (填微粒符号)。
②写出该反应的化学方程式____________________________ 。
(1)物质的结构决定性质。
①根据Na、Al原子结构图Na
 、Al
、Al 可推知,金属Na、Al的化学性质不同的原因是
可推知,金属Na、Al的化学性质不同的原因是②CO和CO2化学性质不同的原因是
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是
(2)如图是氢气在氧气中燃烧的微观示意图(图中“o”代表氢原子。“●”代表氧原子)。

①参加该化学反应的最小粒子是
②写出该反应的化学方程式
您最近一年使用:0次
2020-08-06更新
|
110次组卷
|
2卷引用:开学考试化学试卷03——2020年秋季高一新生入学分班考试化学试卷(全国通用)
名校
4 . 下表是元素周期表的一部分,回答有关问题。

(1)写出元素符号:①___ ,⑥___ 。
(2)在这些元素中,最活泼的金属元素的原子结构示意图为___ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为___ 。
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为___ (填离子符号)。
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有___ 。
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:___ 。

(1)写出元素符号:①
(2)在这些元素中,最活泼的金属元素的原子结构示意图为
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
2020-07-12更新
|
259次组卷
|
5卷引用:北京临川育人学校2021-2022学年高二上学期开学考试化学试题
解题方法
5 . 下表为元素周期表的一部分,用化学用语回答下列问题:
(1)⑧的原子结构示意图为________________ 。
(2)④和⑧在周期表中的位置分别是________________ ;________________ 。
(3)②和③气态氢化物稳定性的大小顺序:________________ (填化学式)。
(4)③⑧⑩的最高价含氧酸的酸性最强的是________________ (填化学式)。
(5)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是__ (填化学式),属于___ (填“共价化合物”或“离子化合物”)。
(6)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为_____ 。
(7)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是_____ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性
| 主族 周期 | I | II | III | IV | V | VI | VII |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)④和⑧在周期表中的位置分别是
(3)②和③气态氢化物稳定性的大小顺序:
(4)③⑧⑩的最高价含氧酸的酸性最强的是
(5)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是
(6)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为
(7)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性
您最近一年使用:0次
解题方法
6 . “题图”是部分元素的离子结构示意图和元素周期表的一部分。 请回答:
(1)图①、②中属于阴离子的是______ (填序号),该元素的质子数为______ ;13号元素原子的最外层电子数为_________ 。
① ②
②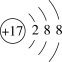
(2)由表中原子序数为1、8、13的元素组成物质的化学式为_____________ 。
(1)图①、②中属于阴离子的是
①
 ②
②
 | ||||||
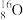 | ||||||
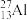 |  | |||||
您最近一年使用:0次
名校
7 . 下表是元素周期表的一部分,用化学用语回答下列问题:
(1)③的元素符号为___ ,元素④与⑦形成化合物的电子式为___ 。
(2)比较元素①和⑥的原子半径大小:①___ (填“>”或“<”)⑥
(3)元素⑥的离子结构示意图为___ 。
(4)元素①和⑧形成的化合物中含有的化学键为___ 。
(5)元素②、⑤的最高价氧化物对应的水化物之间反应的离子方程式为___ 。
(6)工业上冶炼元素⑥的单质的化学方程式为___ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③的元素符号为
(2)比较元素①和⑥的原子半径大小:①
(3)元素⑥的离子结构示意图为
(4)元素①和⑧形成的化合物中含有的化学键为
(5)元素②、⑤的最高价氧化物对应的水化物之间反应的离子方程式为
(6)工业上冶炼元素⑥的单质的化学方程式为
您最近一年使用:0次
名校
8 . 下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
名校
解题方法
9 . 下表中阿拉伯数字(1、2…)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)B、C两元素中非金属性较强的是____ (写出元素名称),I元素在周期表中的位置是_____ 。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式_______ 。
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式_____ ,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M,用电子式表示M的形成过程:____ 。
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式_______ 。
| 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)B、C两元素中非金属性较强的是
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式
您最近一年使用:0次
10 . 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑧的原子结构示意图为_________ ;
(2)②的气态氢化物分子的结构式为___________ ,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____ (填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________ (填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________ (填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____ 。
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为
(2)②的气态氢化物分子的结构式为
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是
(4)⑤、⑥元素的金属性强弱依次为
(5)④、⑤、⑥的形成的简单离子半径依次
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:
您最近一年使用:0次
2020-05-18更新
|
517次组卷
|
2卷引用:江西省上饶市横峰中学2019-2020学年高一(自招班)下学期入学考试化学试题



