13-14高一·全国·课后作业
名校
1 . A、B两种元素,A的原子序数为x,A和B所在周期所含的元素种类分别是a和b。
(1)如果A和B同在ⅠA族,当A在B的上一周期时,B的原子序数为___________ ,当A在B的下一周期时,B的原子序数为___________ 。
(2)如果A和B同在ⅦA族,当A在B的上一周期时,B的原子序数为____________ ,当A在B的下一周期时,B的原子序数为____________ 。
(1)如果A和B同在ⅠA族,当A在B的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当A在B的上一周期时,B的原子序数为
您最近一年使用:0次
2020-05-14更新
|
244次组卷
|
8卷引用:吉林省长春市德惠市实验中学2018-2019学年高一下学期期初检测化学试题
吉林省长春市德惠市实验中学2018-2019学年高一下学期期初检测化学试题(已下线)2014年高一化学人教版必修二 1-1-1元素周期表练习卷安徽省阜阳三中2017-2018学年高一上学期第二次调研考试化学试题人教版高中化学必修二第一章《物质结构 元素周期律》测试卷苏教版高一化学必修2专题1《微观结构与物质的多样性》测试卷湖北省孝感市云梦县2019-2020高一下学期普通高中联考协作体线上考试化学试题(已下线)4.1.1 原子结构 元素周期表 核素练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)【精品卷】4.1.2 元素周期表课堂例题-人教版2023-2024学年必修第一册
名校
解题方法
2 . 下表是周期表中的一部分,根据①--⑩在周期表中的位置,用元素符号 或化学式 回答下列问题:
(1)表中元素,化学性质最不活泼的是______ ,还原性最强的单质是______ ,可用于制半导体材料的元素是______ ;
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是______ ;
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是______ ;
(4)铍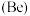 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______ (填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑦ | ⑧ | ⑩ | ||||
| 3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是
(4)铍
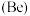 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
您最近一年使用:0次
名校
解题方法
3 . 下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。回答问题:

(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。并注明金属非金属的分界线___ 。
(2)有人认为在元素周期表中,有一种元素也可以放在第ⅦA族,你认为该元素为___ (填元素符号)。
(3)实验室制ca3的化学反应方程式为___ 。
(4)g的氧化物与e的最高价氧化物对应水化物反应的离子方程式为___ 。
(5)设计实验验证b、c非金属性的强弱,用离子方程式表示为___ 。
(6)i在周期表中的位置为___ 。i对应的单质与水反应的化学方程式为___ 。
(7)a2d2的电子式为___ ;用电子式表示fCl2的形成过程___ 。
(8)分别由a、d、e、h四种元素形成的两种盐反应的离子方程式为___ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。并注明金属非金属的分界线
(2)有人认为在元素周期表中,有一种元素也可以放在第ⅦA族,你认为该元素为
(3)实验室制ca3的化学反应方程式为
(4)g的氧化物与e的最高价氧化物对应水化物反应的离子方程式为
(5)设计实验验证b、c非金属性的强弱,用离子方程式表示为
(6)i在周期表中的位置为
(7)a2d2的电子式为
(8)分别由a、d、e、h四种元素形成的两种盐反应的离子方程式为
您最近一年使用:0次
2020-04-23更新
|
63次组卷
|
2卷引用:四川省仁寿第一中学校南校区2019-2020学年高一下学期开学考试化学试题
名校
解题方法
4 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:__ (填元素符号),
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子__ ,碱性最强的化合物的电子式是:__ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:__ 。
(4)表示①与⑦的化合物的电子式__ ,该化合物是由__ (填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_ (用化学式表示)。
(6)元素③的简单氢化物的结构式__ ,在常温下和元素⑦的单质反应的离子方程式__ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式
您最近一年使用:0次
2020-04-22更新
|
297次组卷
|
2卷引用:湖南省双峰县第一中学2019-2020学年高一下学期入学考试化学试题
5 . 黑火药是中国古代四大发明之一,它的爆炸反应为:
2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
(1)生成物A的电子式为:__________________ ,属于______________ 晶体。
(2)黑火药中位于短周期的元素有_________ 种。其中有一种元素的单质可制药,其氧化物可做防腐剂,该元素在周期表中的位置是_________ ,该元素的原子核外有_______ 种不同运动状态的电子。
(3)黑火药所含元素中原子半径从大到小的顺序是______________ (用元素符号表示);
(4)下列能说明黑火药中碳与硫两元素非金属性相对强弱的有___________________ 。
A.相同条件下水溶液的pH:Na2CO3>Na2SO4 B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价 D.加热分解温度:CH4>H2S
2KNO3+3C+S
 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)(1)生成物A的电子式为:
(2)黑火药中位于短周期的元素有
(3)黑火药所含元素中原子半径从大到小的顺序是
(4)下列能说明黑火药中碳与硫两元素非金属性相对强弱的有
A.相同条件下水溶液的pH:Na2CO3>Na2SO4 B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价 D.加热分解温度:CH4>H2S
您最近一年使用:0次
名校
解题方法
6 . 氟及其化合物在生产生活中被广泛使用,造福人类。
(1)氟在元素周期表中的位置是___________ 。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式____________ 。已知25℃时,氢氟酸的电离平衡常数Ka=3.6×10-4,若将0.01 mol·L-1的HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度由大到小的顺序为_____ 。
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为_______ 。
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是________ NA。N2F4气体可用Fe3+氧化二氟胺(HNF2)制得,写出该反应的离子方程式______________ 。
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是_____________ 。
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:________ 。
(1)氟在元素周期表中的位置是
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:
您最近一年使用:0次
2020-01-23更新
|
243次组卷
|
4卷引用:河南省郑州市第一中学2021届高三上学期开学测试化学试题
河南省郑州市第一中学2021届高三上学期开学测试化学试题福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题(已下线)2020届高三《新题速递·化学》2月第01期(考点01-06)(已下线)考点05 元素周期表和元素周期律-2020年高考化学命题预测与模拟试题分类精编
7 . 下表是元素周期表的一部分,请回答:
(1)周期表中第三周期第ⅡA族的元素是_____ 。
(2)P、S、Cl三种元素中,非金属性最强的是____ (填元素符号)。
(3)钠元素最高价氧化物对应水化物的化学式是____ ,常温下该水化物溶液的pH____ (填“>”“<”或“=”)7。
(4)如图为木炭在氧气中燃烧的能量变化图,此反应为____ (填“放热”或“吸热”)反应。

| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | H | ||||||
| 2 | C | ||||||
| 3 | Na | Mg | P | S | Cl |
(1)周期表中第三周期第ⅡA族的元素是
(2)P、S、Cl三种元素中,非金属性最强的是
(3)钠元素最高价氧化物对应水化物的化学式是
(4)如图为木炭在氧气中燃烧的能量变化图,此反应为

您最近一年使用:0次
2020-01-11更新
|
111次组卷
|
3卷引用:广东省2020年普通高中学业水平考试化学合格性考试模拟试题(四)
名校
8 . 如表是元素周期表的一部分,其中每个数字编号代表一种短周期元素。

请按要求回答下列问题:
(1)元素②的元素名称是____ 。
(2)元素⑤处于周期表中第____ 周期第___ 族。
(3)①⑦七种元素中原子半径最大的是___ (填元素符号)。②③④三种元素的最简单氢化物中最稳定的是____ (填化学式)。
(4)元素③和元素⑦的氢化物均极易溶于水,且二者能反应产生大量白烟,写出该白色物质发生分解的化学方程式______ 。
(5)元素⑥的最高价氧化物对应的水化物是一种____ 性氢氧化物,该物质与元素⑦的最高价氧化物对应水化物反应的离子方程式为_____ 。

请按要求回答下列问题:
(1)元素②的元素名称是
(2)元素⑤处于周期表中第
(3)①⑦七种元素中原子半径最大的是
(4)元素③和元素⑦的氢化物均极易溶于水,且二者能反应产生大量白烟,写出该白色物质发生分解的化学方程式
(5)元素⑥的最高价氧化物对应的水化物是一种
您最近一年使用:0次
名校
9 . 下表是元素周期表的一部分,根据A~H在元素周期表中的位置,用元素符号或化学式回答下列问题:
(1)上表中,元素金属性最强的是________ (填元素符号)。
(2)写出D的原子结构示意图:__________
(3)B与C的原子半径比较:B________ C (填“>”或“<”)。G与H的非金属性比较:G ________ H(填“>”或“<”)。
(4)A与H形成化合物的电子式:_______
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | F | H |
(1)上表中,元素金属性最强的是
(2)写出D的原子结构示意图:
(3)B与C的原子半径比较:B
(4)A与H形成化合物的电子式:
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:
您最近一年使用:0次
2019-09-21更新
|
286次组卷
|
4卷引用:四川省成都实验中学2020-2021学年度高2022届高二上学期开学考试化学试题
四川省成都实验中学2020-2021学年度高2022届高二上学期开学考试化学试题湖南省张家界市2018-2019学年高一下学期期末考试化学试题湖北省沙市中学2019-2020学年高二上学期期中考试化学(学考)试题(已下线)专题09 元素周期律(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学
10 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是_______ 。
(2)③④⑤⑥元素的离子半径从大到小顺序是___________________ (填离子符号),表中十种元素最高价氧化物对应水化物中具有两性的是____________ (填写化学式)。
(3)⑤⑥⑦单质的活泼性顺序为________________________ (从大到小排列,填元素符号),判断的实验依据是________________________________________________ (写出一种)。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)③④⑤⑥元素的离子半径从大到小顺序是
(3)⑤⑥⑦单质的活泼性顺序为
您最近一年使用:0次



