解题方法
1 . 如图为钡在元素周期表中的相关信息及原子结构示意图。请回答下列问题:
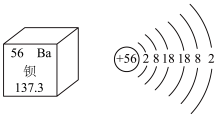
(1)钡是___________ 元素(填“金属”或“非金属”);钡的相对原子质量为___________ 。
(2)钠、镁、铝三种元素中___________ 元素与钡元素位于同一族(填元素符号)。
(3)钡原子在化学变化中易___________ 电子形成钡离子(填“得”或“失”),钡离子有毒,医疗上用“钡餐”(主要成分为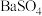 )作
)作 射线透视胃部的内服药,但
射线透视胃部的内服药,但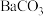 不能用作“钡餐”的原因为
不能用作“钡餐”的原因为___________ (用化学方程式解释)。

(1)钡是
(2)钠、镁、铝三种元素中
(3)钡原子在化学变化中易
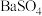 )作
)作 射线透视胃部的内服药,但
射线透视胃部的内服药,但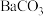 不能用作“钡餐”的原因为
不能用作“钡餐”的原因为
您最近一年使用:0次
解题方法
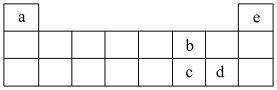
2 . 揭示物质结构的内部特征,有助我们更加准确的理解物质世界。下表是元素周期表的一部分,请回答有关问题。_____ 。
a.门捷列夫 b.道尔顿 c.汤姆生 d.凯库勒
(2)
①a和b化合形成生活中最常见的物质分子式为_____ 。
②上述分子中半径较小的是原子_____ (填元素符号)。
③上述原子结构示意图为_____ 。
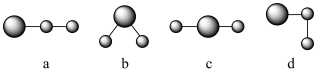
④该分子结构用球棍模型表示正确的是_____ 。
(3)上表中c元素在元素周期表中的位置是_____ ,其简单氢化物的电子式是_____ ,此氢化物的热稳定性比d元素的氢化物热稳定性_____ (填“强”或“弱”)。
a.门捷列夫 b.道尔顿 c.汤姆生 d.凯库勒
(2)

①a和b化合形成生活中最常见的物质分子式为
②上述分子中半径较小的是原子
③上述原子结构示意图为
④该分子结构用球棍模型表示正确的是
(3)上表中c元素在元素周期表中的位置是
您最近一年使用:0次
名校
3 . 金属材料与人类生活息息相关,请回答下列问题。_______ 。
(2)家用台灯通常采用铜质插头,是利用金属铜的_______ 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是_______ 。
(4)将一定质量的Zn片加入 的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是_______ ;若滤液显蓝色,则滤液中溶质一定有_______ 。
(2)家用台灯通常采用铜质插头,是利用金属铜的
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是
(4)将一定质量的Zn片加入
 的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
您最近一年使用:0次
名校
解题方法
4 . 下表为周期表的前四周期,其中的编号代表对应的元素,请用元素符号 回答下列问题
(1)⑦号元素在周期表中的位置是___________ 。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:___________ 。
化学性质最稳定的元素是:___________
(3)根据元素周期律预测:⑾的最高价氧化物的水化物属于___________ (填强酸/弱酸)
(4)①②③④可以形成一种盐,此盐中①②③④原子个数比为5∶1∶1∶3,该盐的化学式是___________ 。
(5)不能 说明⑥的金属性比⑩强的是___________。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
| ⑩ | ⑾ |
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:
化学性质最稳定的元素是:
(3)根据元素周期律预测:⑾的最高价氧化物的水化物属于
(4)①②③④可以形成一种盐,此盐中①②③④原子个数比为5∶1∶1∶3,该盐的化学式是
(5)
| A.⑥与稀盐酸反应比⑩与同条件稀盐酸反应剧烈 |
| B.⑥单质的熔、沸点比⑩的低 |
| C.⑥的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强 |
| D.与非金属单质反应时,⑥原子失电子数目比⑩原子失电子数目少 |
您最近一年使用:0次
5 . 超导体是由 、
、 、
、 三种元素组成,回答下列问题:
三种元素组成,回答下列问题:
(1) 元素属于元素周期表的
元素属于元素周期表的___________ 区元素,其价电子排布式是___________ 。
(2)基态 原子核外电子排布式为
原子核外电子排布式为___________ 。
 、
、 、
、 三种元素组成,回答下列问题:
三种元素组成,回答下列问题:(1)
 元素属于元素周期表的
元素属于元素周期表的(2)基态
 原子核外电子排布式为
原子核外电子排布式为
您最近一年使用:0次
6 . 下图是元素周期表的一部分,表中所列数字①~⑧分别代表某种化学元素。请依据这8种元素回答下列问题。___________ 。(填元素符号 )
(2)下列有关性质的比较,不能用元素周期律解释的是___________。
(3)④的单质在 中燃烧,生成的淡黄色物质的化学式为
中燃烧,生成的淡黄色物质的化学式为___________ ,该化合物的电子式:___________ 。
(4)从原子结构的角度解释非金属性:② ③,
③,___________ 。
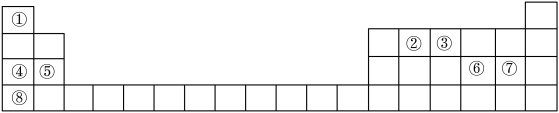
(2)下列有关性质的比较,不能用元素周期律解释的是___________。
A.酸性: | B.金属性: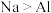 |
C.碱性: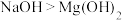 | D.热稳定性: |
(3)④的单质在
 中燃烧,生成的淡黄色物质的化学式为
中燃烧,生成的淡黄色物质的化学式为(4)从原子结构的角度解释非金属性:②
 ③,
③,
您最近一年使用:0次
7 . 工业制硫酸时所用硫铁矿的主要成分为FeS2,硫元素在周期表中的位置第_______ 周期_______ 族;写出第一步反应的化学方程式_______ ,在该反应中被氧化的元素是_______ 。
您最近一年使用:0次
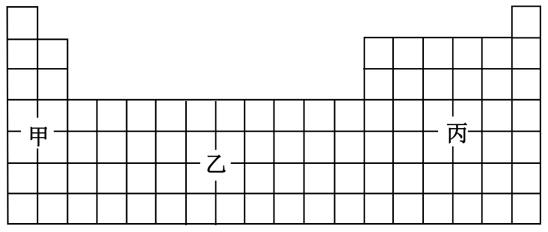
8 . 元素周期表是化学领域的重要工具,在材料、能源、环境和生命科学研究中发挥着重要作用。下面是元素周期表的一部分:_____ 。
2.根据 的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在_____ 族。
2.根据
 的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
您最近一年使用:0次
9 . 钛元素Ti与81号铊元素TI的符号相似而被弄错,铊在元素周期表中的位置是___________ 。
您最近一年使用:0次
解题方法
10 . 下图是元素周期表的一部分,回答下列问题:___________ 。
(2)元素③和⑤能形成多种化合物,其中可作供氧剂的化合物电子式为___________ 。
(3)元素⑤⑥⑧最高价氧化物对应水化物碱性由强到弱顺序为___________ (填化学式)。元素⑥、⑦最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(4)元素⑩的原子序数为35,该元素简单离子的结构示意图为___________ 。
(5)下列可用于判断元素④⑦非金属性强弱的是___________。
(6)从形成化学键类型角度分析,元素①与③易形成多种元素组成的___________ 化合物,一种绿色氧化剂可用于除甲醛(分子式为 )气体,生成两种无毒的氧化物,写出该反应的化学方程式为
)气体,生成两种无毒的氧化物,写出该反应的化学方程式为___________ 。

(2)元素③和⑤能形成多种化合物,其中可作供氧剂的化合物电子式为
(3)元素⑤⑥⑧最高价氧化物对应水化物碱性由强到弱顺序为
(4)元素⑩的原子序数为35,该元素简单离子的结构示意图为
(5)下列可用于判断元素④⑦非金属性强弱的是___________。
| A.氢化物水溶液的酸性强弱:⑦>④ | B.与氢气反应的剧烈程度:④>⑦ |
| C.简单阴离子的还原性:⑦>④ | D.用④的单质与⑦的钠盐溶液反应 |
(6)从形成化学键类型角度分析,元素①与③易形成多种元素组成的
 )气体,生成两种无毒的氧化物,写出该反应的化学方程式为
)气体,生成两种无毒的氧化物,写出该反应的化学方程式为
您最近一年使用:0次



