解题方法
1 . I. 下面是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:
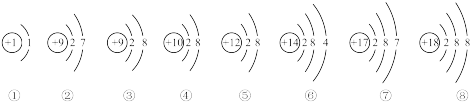
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是_______ ;在化学反应中容易得到电子的是_______ ;属于阳离子的是_______ ;表示F-离子的是_______ ;属于同一种元素的是_______ ;属于非金属元素的是_______ ;电子层数相同,最外层电子数也相同的粒子有_______ ;能与①形成AB4型分子的是_______ 。
II.某微粒的结构示意图可表示为
(2)当x=10+y时,该粒子为_______ (填“原子”、“阳粒子”或“阴离子”),当x<10+y时,该粒子为_______ 。
(3)当y=2时x=_______ 。该元素能形成的离子符号为_______ 。
(4)若该结构示意图表示的粒子是R-,则x=_______ ,y=_______ 。
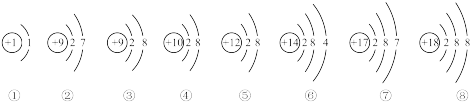
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是
II.某微粒的结构示意图可表示为

(2)当x=10+y时,该粒子为
(3)当y=2时x=
(4)若该结构示意图表示的粒子是R-,则x=
您最近一年使用:0次
2 . 联合国大会将 2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。下表显示了元素周期表中短周期的一部分,①~⑦代表七种短周期元素。
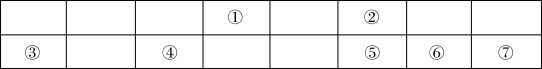
(1)七种元素中化学性质最不活泼的是_______ (填元素符号),形成化合物数目最多的元素是_______ (填元素符号)。
(2)元素②的最低价阴离子的离子结构示意图是_______ 。
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为_______ 。
(6)用电子式表示元素③和元素⑥形成化合物的过程_______ 。

(1)七种元素中化学性质最不活泼的是
(2)元素②的最低价阴离子的离子结构示意图是
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为
(6)用电子式表示元素③和元素⑥形成化合物的过程
您最近一年使用:0次
3 . 铁、铝在生产生活中有广泛的应用。回答下列问题:
(1)铝的原子结构示意图为_______ 。它位于元素周期表的第_______ 周期,第_______ 族。
(2)Na、Al最高价氧化物的水化物之间反应的化学方程式是_______ 。
(3)实验室制备氢氧化铝的常用方法是在氯化铝溶液中滴加氨水,反应的离子方程式为_______ 。
(4)检验某溶液中是否含有 Fe3+的操作方法是_______ 。
(1)铝的原子结构示意图为
(2)Na、Al最高价氧化物的水化物之间反应的化学方程式是
(3)实验室制备氢氧化铝的常用方法是在氯化铝溶液中滴加氨水,反应的离子方程式为
(4)检验某溶液中是否含有 Fe3+的操作方法是
您最近一年使用:0次
22-23高一上·全国·课时练习
4 . 原子结构特点(F→I)
(1)相似性:最外层电子数均为_______ 。
(2)递变性:电子层数逐渐_______ ,原子半径逐渐_______ 。
(1)相似性:最外层电子数均为
(2)递变性:电子层数逐渐
您最近一年使用:0次
22-23高一上·全国·课时练习
5 . 元素周期表和元素周期律的应用
(1)根据同周期、同主族元素性质的递变规律判断元素性质的_______________ 。
(2)应用于_______________ 元素的相互推断。
(3)预测新元素
为新元素的发现及预测它们的_______________ 提供线索。
(4)寻找新物质
①在金属与非金属分界线附近寻找_______________ 。
②研究_______________ 附近元素,制造新农药。
③在_______________ 中寻找催化剂和耐高温、耐腐蚀的合金材料。
(1)根据同周期、同主族元素性质的递变规律判断元素性质的
(2)应用于
(3)预测新元素
为新元素的发现及预测它们的
(4)寻找新物质
①在金属与非金属分界线附近寻找
②研究
③在
您最近一年使用:0次
6 . 数量关系

(1)列序数与族序数的关系
①列序数<8,主族和副族的族序数=__________ ;
②列序数=8或9或10,为第Ⅷ族;
③列序数>10,主族和副族的族序数=_____________ (0族除外)。
(2)三个定量关系
①周期序数=______________ 。
②主族序数=______________ 。
③原子序数=_______________________________________ 。
(3)原子序数的定量关系
①同周期,IIA与IIIA族原子序数差可能为_________________ ;
②同族,相邻周期原子序数差:IA~IIA:_________________ ;
IIIA~0族:_________________ 。如Na与K相差8,Cl与Br相差18。

(1)列序数与族序数的关系
①列序数<8,主族和副族的族序数=
②列序数=8或9或10,为第Ⅷ族;
③列序数>10,主族和副族的族序数=
(2)三个定量关系
①周期序数=
②主族序数=
③原子序数=
(3)原子序数的定量关系
①同周期,IIA与IIIA族原子序数差可能为
②同族,相邻周期原子序数差:IA~IIA:
IIIA~0族:
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
7 . 元素周期表的结构
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—__________ ,VIIA—__________ ,0族—________________ ,IVA、VA、VIA族依次又叫_______________________ 。
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
8 . 原子序数
(1)含义:按照元素在周期表中的_______ 给元素编号。
(2)原子序数与元素的原子结构之间存在的关系:原子序数=__________________ 。
(1)含义:按照元素在周期表中的
(2)原子序数与元素的原子结构之间存在的关系:原子序数=
您最近一年使用:0次
名校
解题方法
9 . 2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相。对月壤中化学元素的分析有助于认识月球表面环境。元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如下:
(1)经分析,月壤中含有大量的h元素,h在周期表中的位置为______________________ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。这两种元素化的金属性强弱顺序为:e_______ f(填“>”或“<”),用电子式表示f与i形成离子化合物的过程________________ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物为_______ ,导致该氢化物熔沸点偏高的原因是________________________________ 。
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。
(5)i是海水中含量丰富的元素,其单质及其化合物在生产、生活领域应用广泛。在图中相应位置写出2种含i元素物质的化学式______ (要求物质类别各不相同;参照c元素形成的NO的定位及写法)。

a | |||||||||||||||||
b | c | d | |||||||||||||||
e | f | g | h | i | |||||||||||||
j |
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。这两种元素化的金属性强弱顺序为:e
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为
(5)i是海水中含量丰富的元素,其单质及其化合物在生产、生活领域应用广泛。在图中相应位置写出2种含i元素物质的化学式

您最近一年使用:0次
10 . 某学习小组探究B及其化合物的性质。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。
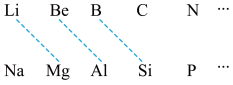
B在元素周期表中的位置是_______ 。其最高价氧化物的化学式为_______ ,与氢氧化钠溶液反应的化学方程式为_______ 。
(2)某科研团队研究发现硼氢化钠( )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
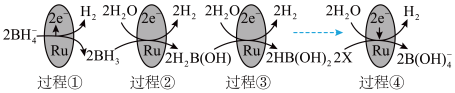
①上图中X的化学式为_______ 。
② 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用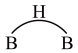 表示,则二聚物结构式为
表示,则二聚物结构式为_______ 。
③图中反应的总化学方程式为_______ 。
④_______ g 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。

B在元素周期表中的位置是
(2)某科研团队研究发现硼氢化钠(
 )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
①上图中X的化学式为
②
 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用 表示,则二聚物结构式为
表示,则二聚物结构式为③图中反应的总化学方程式为
④
 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
您最近一年使用:0次



