名校
解题方法
1 . 我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为: S+2KNO3+3C=K2S+3CO2↑+N2↑。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,
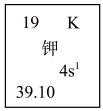
数据“39.10”表示的是___________ ;钾元素在周期表中的位置为___________ 。
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是___________ 。
(3)上述反应生成物中,属于非电解质的是___________ (写结构式);生成物中含有离子键的物质电子式是___________ 。
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为___________ ,它们的非金属性由强到弱的顺序为___________ ;列举一条能证明S和O非金属性强弱的实验事实___________ 。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,

数据“39.10”表示的是
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为
您最近一年使用:0次
名校
2 . 以下元素及物质与人类的生产生活紧密相关。完成下列填空:
(1)氯元素的原子结构示意图_______ ;氯与钠元素组成的化合物的电子式_______ 。
(2)钠、铝、铁三种元素中,_______ 元素是地壳中含量最高的金属元素,其在元素周期表中位于第_______ 周期_______ 族。
(3)以下不是铝、铁的共性的是_______
(4)浓硫酸具有强氧化性,它能与铜反应的化学方程式为_______ 。
(5)列举一个可以说明氯和硫非金属性强弱的事实_______ 。
(1)氯元素的原子结构示意图
(2)钠、铝、铁三种元素中,
(3)以下不是铝、铁的共性的是_______
| A.导电性 | B.导热性 | C.延展性 | D.能与碱溶液反应 |
(5)列举一个可以说明氯和硫非金属性强弱的事实
您最近一年使用:0次
名校
解题方法
3 . 如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)地壳中含量最多的元素是____ 。
(2)氯元素位于元素周期表第____ 周期VIIA族。
(3)单质的化学性质最不活泼的是____ 。
(4)HF和HCl中,热稳定性较强的是____ 。
(5)元素最高价氧化物对应的水化物中,碱性最强的是____ (填化学式)。
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=____ 。
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第
(3)单质的化学性质最不活泼的是
(4)HF和HCl中,热稳定性较强的是
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=
您最近一年使用:0次
4 . 1869年,门捷列夫总结出了元素周期表,还基于此预言了三种当时未被发现的元素,门捷列夫分别称它们为“类硼”、“类铝”与“类硅”。这三种元素在之后的几十年中陆续被发现,从而让人们意识到元素周期表具有重大价值。
(1)基态硼原子的最外层电子数为___________ 。“类硼”是与硼同族的第四周期元素,则“类硼”可能有的性质是___________ (填写下列字母)。
a.最高化合价为 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽
c.该元素单质可与沸水反应置换出 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱
(2)“类硼”最高价氯化物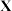 的熔点为
的熔点为 ,则
,则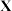 的化学式为
的化学式为___________ ,且该物质属于___________ 晶体。
(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第___________ 周期,其基态原子最外层有___________ 个未成对电子。“类硅”的原子半径___________ (填“>”、“<”或“=”)“类硼”的原子半径,“类硅”的电负性___________ (填“>”、“<”或“=”)“类硼”的电负性。
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表___________ 区中,其基态原子的价电子的电子排布式为___________ 。
(1)基态硼原子的最外层电子数为
a.最高化合价为
 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽c.该元素单质可与沸水反应置换出
 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱(2)“类硼”最高价氯化物
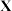 的熔点为
的熔点为 ,则
,则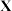 的化学式为
的化学式为(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表
您最近一年使用:0次
2022-06-29更新
|
237次组卷
|
3卷引用:上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题
上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题福建省漳州市第三中学2022-2023学年高二下学期3月质量检测化学试题(已下线)专题03 晶体结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)
5 . 《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄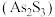 经常用来修改错字。
经常用来修改错字。
(1)S在元素周期表中的位置是第_______ 周期、第ⅥA族。
(2)写出S的最高价氧化物对应的水化物的化学式:_______ 。
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,_______ ,原子半径S小于P,得电子能力S强于P。
(4)在元素周期表中,砷( )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是_______ (填字母)。
a.原子的最外层电子数为5 b.原子半径: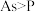 c.稳定性:
c.稳定性: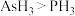
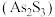 经常用来修改错字。
经常用来修改错字。(1)S在元素周期表中的位置是第
(2)写出S的最高价氧化物对应的水化物的化学式:
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,
(4)在元素周期表中,砷(
 )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是a.原子的最外层电子数为5 b.原子半径:
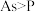 c.稳定性:
c.稳定性: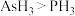
您最近一年使用:0次
名校
6 . Ⅰ.黑火药爆炸的化学方程式为: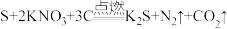 。回答下列问题:
。回答下列问题:
(1)硫元素在周期表的位置是_______ 。氨气的电子式_______ 。
(2)用电子式表示化合物 的形成过程为
的形成过程为_______ 。
(3)上述氧化产物结构式为_______ 。
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
请回答下列问题:
(5)上述元素中,M层电子数最多的是_______ (填元素名称)。
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
(8)元素⑦的最高价氧化物对应的水化物与元素⑨的最简单氢化物的水溶液反应的离子方程式_______ 。
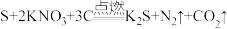 。回答下列问题:
。回答下列问题:(1)硫元素在周期表的位置是
(2)用电子式表示化合物
 的形成过程为
的形成过程为(3)上述氧化产物结构式为
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
A.原子半径: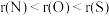 | B.热稳定性: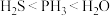 |
C.溶解度: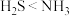 | D.微粒种类:氢硫酸<氨水 |
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
请回答下列问题:
(5)上述元素中,M层电子数最多的是
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将形状、大小相同的这两种元素的单质分别与等体积20℃的水反应 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
解题方法
7 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
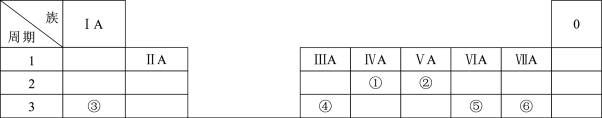
(1)②的原子结构示意图是_______ 。
(2)写出①的最高价氧化物的电子式:_______ 。
(3)⑤和⑥分别形成的最简单氢化物更稳定的是_______ (填化学式)。
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为_______ 。

(1)②的原子结构示意图是
(2)写出①的最高价氧化物的电子式:
(3)⑤和⑥分别形成的最简单氢化物更稳定的是
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为
您最近一年使用:0次
名校
8 . 如图是元素周期表的一部分。回答下列问题:

溴被称为海洋元素。
(1)溴在元素周期表中位于第___________ 周期___________ 族。
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
(3)能够证明溴的非金属性强于碘的方法是___________ (写出一种即可)。

溴被称为海洋元素。
(1)溴在元素周期表中位于第
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
(3)能够证明溴的非金属性强于碘的方法是
您最近一年使用:0次
名校
9 . 随着原子序数的递增,七种短周期元素的原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。请回答下列问题:
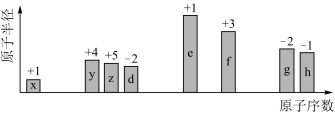
(1)x在元素周期表中的位置是___________ ,如果x的某种原子中含2个中子,则该原子的核素符号为___________ 。
(2)y的最简单氢化物中含有的化学键类型为___________ (填“离子键”“极性共价键”或“非极性共价键”)。
(3)d、e、f的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(4) e的单质在空气中充分燃烧,所得产物的电子式为___________ 。
(5)f的单质和e的最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(6)能说明h的非金属性比g的强的实验事实是___________ (列举一条)。

(1)x在元素周期表中的位置是
(2)y的最简单氢化物中含有的化学键类型为
(3)d、e、f的简单离子半径由大到小的顺序为
(4) e的单质在空气中充分燃烧,所得产物的电子式为
(5)f的单质和e的最高价氧化物对应的水化物相互反应的化学方程式为
(6)能说明h的非金属性比g的强的实验事实是
您最近一年使用:0次
名校
10 . 运用元素周期律和元素周期表,可以系统研究元素的性质。回答下列问题:
(1)碱金属元素中,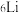 和
和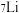 之间的关系是互为
之间的关系是互为_______ 。金属钾的氧化物有多种,其中过氧化钾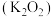 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是_______ ,根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
②硅和锗单质分别与 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是_______ (填“硅”或“锗”)。
(1)碱金属元素中,
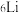 和
和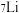 之间的关系是互为
之间的关系是互为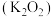 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是
②硅和锗单质分别与
 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是
您最近一年使用:0次



