1 . X、Y、Z、W、M、R、T七种短周期元素,周期表中位置如图:
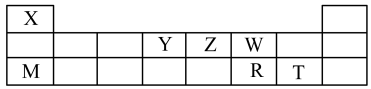
试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是______ (用元素符号表示)。
(2)W的简单氢化物的电子式为_______ 。
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为______ 。
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是______ (用化学式表示)。
(5)M和R最高价氧化物对应水化物反应的离子方程式为______ 。

试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是
(2)W的简单氢化物的电子式为
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是
(5)M和R最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
名校
2 . 我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。
(1)镓的原子结构示意图为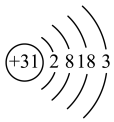 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是___________ 。
(2)GaAs的熔点为1238℃且熔融状态不导电,据此判断它是___________ (填“共价”或“离子”)化合物。
(3)镓与氨气在1100℃下反应生成氮化镓和氢气,该可逆反应每生成1 mol 放出10.3 kJ热量。该反应的热化学方程式是
放出10.3 kJ热量。该反应的热化学方程式是___________ 。(已知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
(4)下列说法错误的是___________ 。
a.氢氧化镓可能具有两性 b.砷化镓具有半导体性质
c.As与 在低温时可剧烈化合为
在低温时可剧烈化合为 d.酸性:
d.酸性:
(1)镓的原子结构示意图为
 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是(2)GaAs的熔点为1238℃且熔融状态不导电,据此判断它是
(3)镓与氨气在1100℃下反应生成氮化镓和氢气,该可逆反应每生成1 mol
 放出10.3 kJ热量。该反应的热化学方程式是
放出10.3 kJ热量。该反应的热化学方程式是(4)下列说法错误的是
a.氢氧化镓可能具有两性 b.砷化镓具有半导体性质
c.As与
 在低温时可剧烈化合为
在低温时可剧烈化合为 d.酸性:
d.酸性:
您最近一年使用:0次
3 . 请仿照表中已有元素的呈现方式补全下表_____ 。
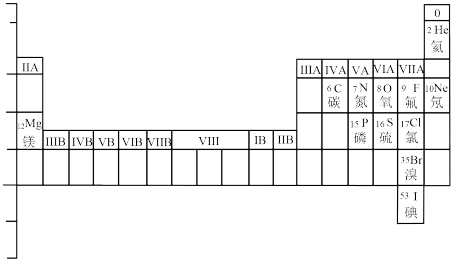

您最近一年使用:0次
4 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)元素②的原子结构示意图是______ 。
(2)比较元素原子半径大小:③______ ④(填“>”或“<”)。
(3)元素③位于元素周期表中第______ 周期VA族。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式______ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为______ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ | ||||||||
(2)比较元素原子半径大小:③
(3)元素③位于元素周期表中第
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近一年使用:0次
解题方法
5 . 下表列出了A~M 13种元素在周期表中的位置:
(1)这些元素中,金属性最强的元素是_______ (填元素符号,下同),非金属性最强的是_______ 。
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式_______ 。
(3) 、
、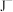 、
、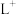 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是_______ ,最小的是_______ 。
(4)A与D形成的化合物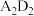 是
是_______ 化合物,其电子式为_______ 。
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式
(3)
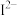 、
、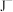 、
、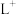 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是(4)A与D形成的化合物
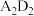 是
是
您最近一年使用:0次
名校
6 . 元素在周期表中的位置,反映了元素的原子结构和性质。如图是元素周期表的一部分,请按照要求回答下列问题:
(1)①的元素符号是______ ,元素②位于周期表中的第______ 周期第______ 族。
(2)②、③两种元素中,非金属性较强的是______ (填元素符号)
(3)①、②、④三种元素中,原子半径最大的是______ (填元素符号)。
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是______ (填化学式)。
(5)常温下,将元素⑥的单质通入 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式______
| 族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | |||||
(2)②、③两种元素中,非金属性较强的是
(3)①、②、④三种元素中,原子半径最大的是
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是
(5)常温下,将元素⑥的单质通入
 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2023-06-08更新
|
164次组卷
|
2卷引用:云南省普通高中2021-2022学年高一下学期期末学业水平考试化学试题
名校
解题方法
7 . 实验室加热液体时常加入沸石,其主要成分为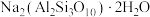 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:
(1)元素Si在周期表中的位置是_______ 。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式);Na与同周期非金属性最强的元素形成的化合物可做调味品,用电子式表示该化合物的形成过程_______ 。
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是_______ (填化学式)。
(4)Na所在周期的主族元素中,简单离子半径最小的是_______ (填离子符号)
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
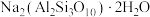 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:(1)元素Si在周期表中的位置是
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是
(4)Na所在周期的主族元素中,简单离子半径最小的是
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
8 . 合成氨是人类科学技术发展史上的一项重大成就,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氮原子中,能量最高的电子的电子云在空间有_______ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为_______ ;第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为_______ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有_______ (填元素符号)
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①Mn在元素周期表中的位置_______ ,基态Mn原子未成对的电子数为_______ 。
②第三电离能
_______ 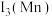 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
(1)基态氮原子中,能量最高的电子的电子云在空间有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①Mn在元素周期表中的位置
②第三电离能

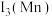 (填“>”或“<”),原因是
(填“>”或“<”),原因是
您最近一年使用:0次
2023-02-14更新
|
662次组卷
|
3卷引用:山东省泰安市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
9 . 请回答下列问题。
(1)在第三周期元素中,化学性质最不活泼的是_______ ,可用于制半导体材料的元素是_______ ,最高价氧化物的水化物碱性最强的是_______ ,酸性最强的是_______ ,具有两性的是_______ (以上均用化学式填空)。
(2)在C、N、O、F中,原子半径最大的是_______ 。
(3)第32号元素在元素周期表中的位置为_______ 。
(4)由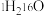 与
与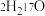 所代表的物质中,共有
所代表的物质中,共有_______ 种元素,_______ 种原子, 、
、 的关系是
的关系是_______ 。
(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:_______ 。
(1)在第三周期元素中,化学性质最不活泼的是
(2)在C、N、O、F中,原子半径最大的是
(3)第32号元素在元素周期表中的位置为
(4)由
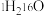 与
与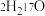 所代表的物质中,共有
所代表的物质中,共有 、
、 的关系是
的关系是(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:
您最近一年使用:0次
名校
10 . I、下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
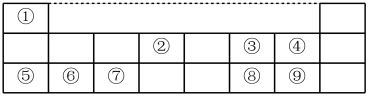
(1)元素⑧在周期表中的位置___________ ;
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与二氧化碳反应的化学方程式___________ 。
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为___________ 。
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式___________ 。
II、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。

(5)若实验室用该浓硫酸配制240mL0.5mol/L的稀硫酸,请计算需要该浓硫___________ mL(精确到小数点后1位)。
(6)配制过程中的正确操作顺序是:b、d___________ 、e(填“字母”)。
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是___________ 。
a、移液过程有H2SO4溶液溅出瓶外
b、移液后未洗涤烧杯和玻璃棒
c、定容时俯视容量瓶刻度线
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶

(1)元素⑧在周期表中的位置
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与二氧化碳反应的化学方程式
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式
II、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。

(5)若实验室用该浓硫酸配制240mL0.5mol/L的稀硫酸,请计算需要该浓硫
(6)配制过程中的正确操作顺序是:b、d
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是
a、移液过程有H2SO4溶液溅出瓶外
b、移液后未洗涤烧杯和玻璃棒
c、定容时俯视容量瓶刻度线
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶
您最近一年使用:0次



