名校
解题方法
1 . 一氯化碘(ICl)是一种卤素互化物,与卤素单质性质相似,可用于制农药等。
(1)Cl在元素周期表中位于第三周期、第_______ 族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为_______ 价。
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,_______ ,得电子能力Cl强于I。
(4)下列推断中,正确的是_______ (填字母)。
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
(1)Cl在元素周期表中位于第三周期、第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,
(4)下列推断中,正确的是
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
您最近一年使用:0次
2023-01-17更新
|
273次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
名校
2 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是_______ 。
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是_______ (填化学式;用“>”连接)。
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断_______ (填“正确”或“错误”);根据元素周期律,自然界中最强的碱是_______ (填化学式)。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ |
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断
您最近一年使用:0次
2023-01-16更新
|
426次组卷
|
4卷引用:山东省莘县多校2022-2023学年高一上学期期末线上联考化学试题
山东省莘县多校2022-2023学年高一上学期期末线上联考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷
名校
解题方法
3 . 下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:

(1)地壳中含量最高的金属元素是___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)用电子式表示J与C形成化合物的过程:___________ 。
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。

(1)地壳中含量最高的金属元素是
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)用电子式表示J与C形成化合物的过程:
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
2023-01-11更新
|
441次组卷
|
4卷引用:河北省保定市部分高中2022-2023学年高一上学期期末考试化学试题
4 . 下表是元素周期表的一部分,请回答:
(1)元素⑦的原子结构示意图为_______ ;元素⑩的名称为_______ 。
(2)在这些元素中,化学性质最活泼的金属元素是_______ (填元素符号,下同),最不活泼的元素是_______ ;原子半径最小的元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同);具有两性的是_______ 。
(4)用电子式表示⑤⑦形成化合物过程:_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)用电子式表示⑤⑦形成化合物过程:
您最近一年使用:0次
5 . 下表列出了①~④四种元素在周期表中的位置.
回答下列问题:
(1)①的元素符号为_____________ 。
(2)②的基态原子电子排布式为__________________________ 。
(3)③和④中原子半径较大的是_____________ (填元素符号)。
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为_____________ 形;每个p能级都有_____________ 个相互垂直的电子云。

| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ||||||
| 4 | ④ |
回答下列问题:
(1)①的元素符号为
(2)②的基态原子电子排布式为
(3)③和④中原子半径较大的是
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为

您最近一年使用:0次
6 . 元素在周期表中的位置反映了元素的原子结构和性质,矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1)Al元素在元素周期表中的位置为_____ ,K2O的电子式为_____ 。
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为_____ 。
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_____ 族。
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是_____ 。
(1)Al元素在元素周期表中的位置为
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是
您最近一年使用:0次
解题方法
7 . 元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
2023-01-04更新
|
734次组卷
|
3卷引用:辽宁省辽南协作体2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图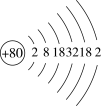 汞在第
汞在第___________ 周期。
(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷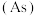 也是氮族元素。
也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是___________ (填序号)。
a、含有离子键和共价键
b、能与 溶液反应
溶液反应
c、与 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样
③砷酸 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)据汞的原子结构示意图
 汞在第
汞在第(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷
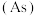 也是氮族元素。
也是氮族元素。①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是a、含有离子键和共价键
b、能与
 溶液反应
溶液反应c、与
 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样③砷酸
 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:
您最近一年使用:0次
2022-12-28更新
|
141次组卷
|
2卷引用:河南省顶级名校2022-2023学年高三上学期12月摸底考试化学试题
21-22高二下·全国·单元测试
解题方法
9 . 元素周期表:_______ 的表格,元素周期系只有一个,元素周期表多种多样。
您最近一年使用:0次
10 . 三张有重要历史意义的周期表
(1)门捷列夫周期表:门捷列夫周期表又称_______ 周期表,重要特征是从第_______ 周期开始每个周期截成_______ 截,第_______ 族分_______ 族,第_______ 族称为过渡元素。
(2)维尔纳周期表
维尔纳周期表是_______ ,每个周期一行,各族元素、过渡金属、稀有气体、镧系和锕系,各有各的位置,同族元素_______ ,它确定了前_______ 个周期的元素种类。
(3)玻尔元素周期表
玻尔元素周期表特别重要之处是把21~28、39~46等元素用_______ 框起,这说明他已经认识到,这些框内元素的原子新增加的_______ 是填入_______ 的,他已经用原子结构解释元素周期系了,玻尔元素周期表确定了第_______ 周期为_______ 种元素。
(1)门捷列夫周期表:门捷列夫周期表又称
(2)维尔纳周期表
维尔纳周期表是
(3)玻尔元素周期表
玻尔元素周期表特别重要之处是把21~28、39~46等元素用
您最近一年使用:0次



