21-22高二下·全国·单元测试
1 . 元素周期表的基本结构
(1)周期元素种数的确定
第一周期从_______ 开始,以_______ 结束,只有两种元素。其余各周期总是从_______ 能级开始,以_______ 结束,从ns能级开始以np结束递增的_______ (或电子数)就等于每个周期里的元素数目。
(2)元素周期表的形成
若以一个方格代表一种元素,每个_______ 排一个横排,并按s、p、d、f分段,左侧对齐,可得到如图元素周期表:
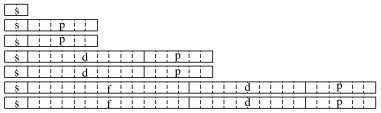
若将p段与p段对齐,d段与d段对齐、f段单独列出,将_______ 与p段末端对齐,则得到书末的元素周期表:
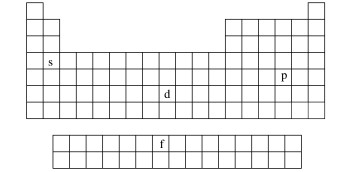
(1)周期元素种数的确定
第一周期从
| 周期 | ns~np | 电子数 | 元素数目 |
| 一 | 1s1~2 | ||
| 二 | 2s1~22p1~6 | ||
| 三 | 3s1~23p1~6 | ||
| 四 | 4s1~23d1~104p1~6 | ||
| 五 | 5s1~24d1~105p1~6 | ||
| 六 | 6s1~24f1~145d1~106p1~6 | ||
| 七 | 7s1~25f1~146d1~107p1~6 |
(2)元素周期表的形成
若以一个方格代表一种元素,每个

若将p段与p段对齐,d段与d段对齐、f段单独列出,将

您最近一年使用:0次
21-22高二下·全国·单元测试
2 . 元素周期表探究
①元素周期表的结构

②元素周期表的分区
i.根据核外电子的排布分区
按电子排布式中最后填入电子的_______ 符号可将元素周期表分为s、p、d、f 4个区,而ⅠB、ⅡB族这2个纵行的元素的核外电子因先填满了_______ 能级而后再填充ns能级而得名_______ 区。5个区的位置关系如图所示。
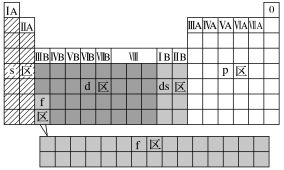
ii.根据元素的金属性和非金属性分区
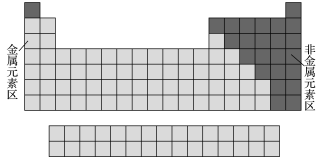
①元素周期表的结构

②元素周期表的分区
i.根据核外电子的排布分区
按电子排布式中最后填入电子的

ii.根据元素的金属性和非金属性分区

您最近一年使用:0次
解题方法
3 . 下表为元素周期表的一部分,请回答有关问题
(1)已知元素⑩的一种核素,其中中子数为45,用原子符号表示该核素为__________
(2)⑥是地壳中含量最高的金属元素,用原子符号表示该元素为__________
(3)由上述④⑤元素构成的淡黄色固体化合物的化学式______ ,该化合物与水反应的化学方程式___________________ 。
(4)元素⑨的焰色试验火焰颜色为__________
(5)元素④在元素周期表中的位置是第______ 周期第_____ 族
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)已知元素⑩的一种核素,其中中子数为45,用原子符号表示该核素为
(2)⑥是地壳中含量最高的金属元素,用原子符号表示该元素为
(3)由上述④⑤元素构成的淡黄色固体化合物的化学式
(4)元素⑨的焰色试验火焰颜色为
(5)元素④在元素周期表中的位置是第
您最近一年使用:0次
名校
解题方法
4 . 元素①-⑥在元素周期表中的位置如下,按要求填空
回答下列问题:
(1)元素①的名称和符号为:_______ 。
(2)元素②的一种中子数为8的核素可用作分析古代人类食物结构,写出其原子符号_______ 。
(3)元素③-⑥中,原子半径最小的是_______ (填元素符号)。
(4)元素的非金属性:⑤_______ ⑥(填“>”、“<”或“=”),若通过实验事实证明上述结论,利用适当的文字与化学用语进行概述:_______ (写出2条)
(5)常温下,元素④的最高价氧化物的水化物可溶于③的最高价氧化物对应的水化物浓溶液中,其对应的化学方程式为_______ 。
| IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ① | ② | ||||||
| 第3周期 | ③ | ④ | ⑤ | 6 | ||||
| 第4周期 | ⑦ |
回答下列问题:
(1)元素①的名称和符号为:
(2)元素②的一种中子数为8的核素可用作分析古代人类食物结构,写出其原子符号
(3)元素③-⑥中,原子半径最小的是
(4)元素的非金属性:⑤
(5)常温下,元素④的最高价氧化物的水化物可溶于③的最高价氧化物对应的水化物浓溶液中,其对应的化学方程式为
您最近一年使用:0次
5 . 根据元素周期表中1~20号元素的性质和递变规律,回答下列问题:
(1)原子序数为8的元素符号是_______ ;
(2)硫化氢的化学式是_______ ;
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是:F_______ Cl(填“>”或“<”);
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(1)原子序数为8的元素符号是
(2)硫化氢的化学式是
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是:F
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
2022-12-16更新
|
385次组卷
|
2卷引用:湖南省部分普通高中2022-2023学年高一上学期学业水平合格性考试化学试题
解题方法
6 . 下表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是_______ (填元素符号,下同);金属性最强的元素是_______ ;单质的化学性质最不活泼的元素是_______ ;气体单质有颜色的元素_______ ;可运输浓硫酸的金属元素是_______ 。
(2)最高价氧化物对应水化物酸性最强的是_______ ,碱性最强的是_______ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是_______ (填化合物化学式);
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:_______ ,氢氧化铝治疗胃酸分泌过多的离子方程式:_______ 。
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
解题方法
7 . 写出1-36号元素的元素符号与名称______ 。
您最近一年使用:0次
名校
解题方法
8 . 填空或写出下列反应的离子方程式:
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和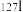 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为_________ 。碘元素在元素中位于第__________ 周期第__________ 族。
(2)向明矾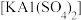 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:________________ 。
(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)______ 。
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是________________ 。
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是________________ 。
(1)碘-131是元素碘(元素周期表中第53号元素)的一种放射性同位素,符号为
 。在核医学中,以
。在核医学中,以 以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。
以NaI溶液的形式直接用于甲状腺功能检查和甲状腺疾病。 和
和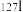 互为同位素,这两种原子的中子数差值为
互为同位素,这两种原子的中子数差值为(2)向明矾
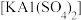 溶液中滴加Ba(OH)2、溶液
溶液中滴加Ba(OH)2、溶液 恰好沉淀,离子方程式是:
恰好沉淀,离子方程式是:(3)实验室常利用氨水制取Al(OH)3,而不用NaOH的溶液的原因是(用离子方程式说明)
(4)实验室用FeCl2溶液和NaOH溶液制取Fe(OH)2时观察到的现象是
(5)将0.2mol钠、镁、铝分别投入10mL1mol/L的盐酸中,在标准状况下产生氢气体积的大小顺序是
您最近一年使用:0次
名校
解题方法
9 . 金属Na、Mg、Al有广泛的应用。
(1)Al在元素周期表中的位置是______ 。
(2)金属镁可以用来生产金属铀(元素符号是U): ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是______ (填化学式,下同),被还原的物质是______ 。
(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
由实验1和实验2得出的结论是:金属性,______ >______ >______ (填元素符号),用原子结构理论解释:同周期元素从左到右,______ 。
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式______ 。
(1)Al在元素周期表中的位置是
(2)金属镁可以用来生产金属铀(元素符号是U):
 ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
| 实验1 | 实验2 |
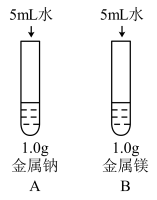 |  |
| 钠与水反应剧烈,镁与水反应缓慢 | 镁与盐酸反应剧烈,铝与盐酸反应缓慢 |
由实验1和实验2得出的结论是:金属性,
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式
您最近一年使用:0次
2022-12-14更新
|
92次组卷
|
2卷引用:新疆伊宁市第八中学2021-2022学年高一上学期期末考试化学试题
名校
解题方法
10 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p的原子结构示意图为___________________ 。
(2)o、p两元素的部分电离能数据如下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_________________________________________________________ 。
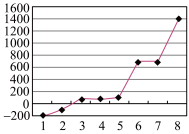
(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是___________________ (填图1中的序号)。
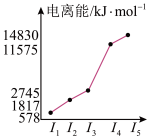
(4)表中所列的某主族元素的电离能情况如图所示,则该元素是___________________ (填元素符号)。
(5)基态钒原子的价电子排布图为___________________ 。
(6)写出单电子数最多的原子的电子排布式:__________________________________________ 。
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
(1)元素p的原子结构示意图为
(2)o、p两元素的部分电离能数据如下表:
元素 元素电离能/  | o | p |
| 717 | 759 |
| 1509 | 1561 |
| 3248 | 2957 |
比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图所示,则该元素是

(5)基态钒原子的价电子排布图为
(6)写出单电子数最多的原子的电子排布式:
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
A.[Ne]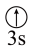 | B.[Ne]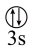 | C.[Ne]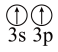 | D.[Ne]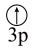 |
您最近一年使用:0次




