名校
解题方法
1 . 已知元素周期表中共有18纵行。如图所示实线表示元周期表的边界,按电子排布,可把元素周期表划分为s区、p区、d区、ds等,除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
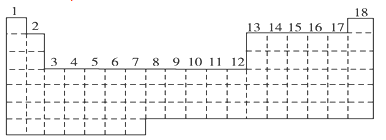
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区_____ 。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)_____ 。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:___________ 。
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布
您最近一年使用:0次
2022-10-20更新
|
158次组卷
|
2卷引用:河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题
解题方法
2 . 如图是元素周期表的一部分,回答下列问题:
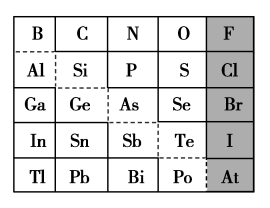
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
3 . 基态 原子的价电子排布式为
原子的价电子排布式为_______ ,在元素周期表中位置为_______ 。
 原子的价电子排布式为
原子的价电子排布式为
您最近一年使用:0次
名校
4 . 新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:_______ 个质子,左图中89.91表示的是_______ ;
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据_______ 个电子层;
(3)钇元素形成氧化物的化学式是_______ 。
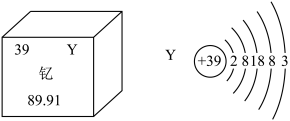
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据
(3)钇元素形成氧化物的化学式是
您最近一年使用:0次
2022-10-08更新
|
327次组卷
|
3卷引用:新疆和田地区第一中学2022-2023学年高一上学期开学考试化学试题
5 . 下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
(1)上述元素属于第三周期,且可以做半导体材料的是_______ (填字母代号)。
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______ 。
②表中Y可能为以上13种元素中的_______ (填写字母)元素。用元素符号表示X和l形成化合物的电子式是_______ 。
(3)以上13种元素中,_______ (填写字母)元素原子失去核外第一个电子需要的能量最多。
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于_______ 区。
| b | |||||||||||||||||||
| h | j | ||||||||||||||||||
| a | c | f | i | l | m | ||||||||||||||
| e | g | ||||||||||||||||||
| d | k | ||||||||||||||||||
(1)上述元素属于第三周期,且可以做半导体材料的是
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量
②表中Y可能为以上13种元素中的
(3)以上13种元素中,
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于
您最近一年使用:0次
6 . 默写元素周期表中的1至20号元素,写出元素符号及名称_______ 。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
| 符号 | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ |
| 名称 | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |
| 符号 | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ |
| 名称 | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ | ____ |
您最近一年使用:0次
解题方法
7 . 镁铝合金与钢在生产生活中有广泛的应用。
(1)地壳中含量最高的金属元素是___________ ,其单质的还原性比Na___________ (填“强”或“弱”)。
(2)镁铝合金比铝___________ (填“硬”或“软”),用足量的氢氧化钠溶液溶解镁铝合金,剩余的金属主要是___________ 。
(3)钢中含有的主要金属元素是___________ ,(填元素符号)该元素的单质粉末(过量)在氯气中加热,发生反应的化学方程式为___________ 。
(1)地壳中含量最高的金属元素是
(2)镁铝合金比铝
(3)钢中含有的主要金属元素是
您最近一年使用:0次
2022-10-07更新
|
135次组卷
|
2卷引用:黑龙江省佳木斯市第八中学2021-2022学年高一上学期期末考试化学试题
解题方法
8 . 完成下列问题
(1)写出Ni的元素名称_______ , 该元素在周期表的位置为第_______ 周期,第_______ 族。
(2)基态Si原子的电子排布式为_______ ,基态S原子的电子排布式为_______ 。
(3)写出基态Fe原子的价层电子排布式:_______ 。
(1)写出Ni的元素名称
(2)基态Si原子的电子排布式为
(3)写出基态Fe原子的价层电子排布式:
您最近一年使用:0次
9 .  、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,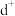 中各层电子数都是
中各层电子数都是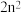 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物_______ 。
 、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,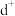 中各层电子数都是
中各层电子数都是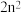 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物
您最近一年使用:0次
解题方法
10 . 请根据构造原理,按要求写出下列电子排布式或原子结构示意图:
(1)16S的电子排布式___________ 。
(2)26Fe的简化电子排布式___________ 。
(3)某元素原子的电子排布式为[Ar]3d104s24p1,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第___________ 周期。
②该元素处于元素周期表的第___________ 族。
③试推测该元素处于元素周期表的___________ 区。
(1)16S的电子排布式
(2)26Fe的简化电子排布式
(3)某元素原子的电子排布式为[Ar]3d104s24p1,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第
②该元素处于元素周期表的第
③试推测该元素处于元素周期表的
您最近一年使用:0次



