解题方法
1 . a、b、c、d为短周期主族元素,a的M层上有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d属于同周期元素,且d的原子半径小于c的原子半径。下列叙述错误的是
| A.四种元素中,元素d的非金属性最强 |
| B.元素a、b、c均能与氧元素形成两种或两种以上的化合物 |
| C.元素a分别与b、d元素形成的化合物均是离子化合物 |
| D.元素c、d分别与氢元素形成的最简单氢化物中的化学键均为非极性共价键 |
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示,下列说法正确的是


| A.金属性:N>Q | B.最高价氧化物对应水化物的酸性:M<Y |
| C.简单离子半径:Q>N>X | D.原子序数:Z>M>X>Y |
您最近一年使用:0次
解题方法
3 . 短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的价层电子排布式为 ,X、Y、Z三种元素组成的一种化合物
,X、Y、Z三种元素组成的一种化合物 的焰色呈黄色,向该化合物中滴加盐酸,产生刺激性气味气体和浅黄色固体,该气体通入品红溶液中,品红溶液褪色。下列叙述错误的是
的焰色呈黄色,向该化合物中滴加盐酸,产生刺激性气味气体和浅黄色固体,该气体通入品红溶液中,品红溶液褪色。下列叙述错误的是
 ,X、Y、Z三种元素组成的一种化合物
,X、Y、Z三种元素组成的一种化合物 的焰色呈黄色,向该化合物中滴加盐酸,产生刺激性气味气体和浅黄色固体,该气体通入品红溶液中,品红溶液褪色。下列叙述错误的是
的焰色呈黄色,向该化合物中滴加盐酸,产生刺激性气味气体和浅黄色固体,该气体通入品红溶液中,品红溶液褪色。下列叙述错误的是| A.基态Y原子最外层电子的电子云轮廓图为球形 |
B.电负性: |
C. 的VSEPR模型为平面三角形 的VSEPR模型为平面三角形 |
D.Z的最简单氢化物的中心原子采取 杂化 杂化 |
您最近一年使用:0次
名校
4 . 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)W在元素周期表中的位置为___________ 。
(2)用电子式表示X与Y组成 的化合物的形成过程:
的化合物的形成过程:___________ 。
(3)M位于第四周期,与W同族。
①根据元素周期律,下列推断正确的是___________ (填序号)。
A.M的最高正化合价为+7价 B.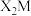 的还原性比
的还原性比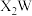 强
强
C.最高价氧化物的水化物的酸性:M>W D.稳定性:
② 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为___________ 。(用含M的化学式表示)
(1)W在元素周期表中的位置为
(2)用电子式表示X与Y组成
 的化合物的形成过程:
的化合物的形成过程:(3)M位于第四周期,与W同族。
①根据元素周期律,下列推断正确的是
A.M的最高正化合价为+7价 B.
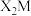 的还原性比
的还原性比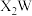 强
强C.最高价氧化物的水化物的酸性:M>W D.稳定性:

②
 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为
您最近一年使用:0次
2024-02-11更新
|
301次组卷
|
3卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题
名校
解题方法
5 . 短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如图所示。Z核外最外层电子数与X核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确的是


| A.原子半径大小:Y>Z>Q |
| B.W、Y、Z三种元素可形成离子化合物 |
| C.该化合物中Y原子不满足8电子稳定结构 |
D.Z与W可形成 ,其空间结构是直线形 ,其空间结构是直线形 |
您最近一年使用:0次
2024-02-10更新
|
374次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题
6 .  为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的简单氢化物能与它的最高价氧化物的水化物反应生成盐,
的简单氢化物能与它的最高价氧化物的水化物反应生成盐, 原子核外
原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,
能级上的电子总数相等, 原子核外没有未成对电子,
原子核外没有未成对电子, 与
与 位于同一主族。下列说法正确的是
位于同一主族。下列说法正确的是
 为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的简单氢化物能与它的最高价氧化物的水化物反应生成盐,
的简单氢化物能与它的最高价氧化物的水化物反应生成盐, 原子核外
原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,
能级上的电子总数相等, 原子核外没有未成对电子,
原子核外没有未成对电子, 与
与 位于同一主族。下列说法正确的是
位于同一主族。下列说法正确的是A.简单离子半径: | B. 的第一电离能比 的第一电离能比 第一电离能小 第一电离能小 |
C.用电解 的氧化物制备 的氧化物制备 单质 单质 | D. 的简单氢化物比 的简单氢化物比 的简单氢化物稳定 的简单氢化物稳定 |
您最近一年使用:0次
名校
7 . X、Y,Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示 的形成过程:
的形成过程:____________________ 。
(2)W在周期表中的位置是____________________ 。
(3)ZYX的电子式为__________ , 中含有的化学键类型为
中含有的化学键类型为__________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是____________________ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是__________ (填字母)。
a.简单阴离子的还原性:Q>R b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R d.Q的单质能从 溶液中置换出R单质
溶液中置换出R单质
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是_______________________________ 。
(7)35号元素溴(Br)和Q位于同一主族,被称为“海洋元素”,高溴酸( )的酸性比
)的酸性比
_______ (填“强”或“弱”),请从位—构—性角度分析原因____________________________ 。
(1)用电子式表示
 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R d.Q的单质能从
 溶液中置换出R单质
溶液中置换出R单质(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(7)35号元素溴(Br)和Q位于同一主族,被称为“海洋元素”,高溴酸(
 )的酸性比
)的酸性比
您最近一年使用:0次
解题方法
8 . 现有几种短周期元素的性质或原子结构如下表,下列判断不正确的是
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成 原子电子层结构 原子电子层结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气中的主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
A.元素的非金属性: | B. 分子的空间结构为直线形 分子的空间结构为直线形 |
C. 的电子式为 的电子式为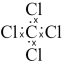 | D.实验室可将未用完的T单质放回原试剂瓶 |
您最近一年使用:0次
解题方法
9 . a、b、c、d、e、f是原子序数依次增大的非0族元素,位于元素周期表的前四周期。a的一种核素无中子,b的s能级电子数与p能级的电子数之比为4:3,c与e同主族,未成对电子数为2,d在同周期元素中的原子半径最大,f在同周期元素中的未成对电子数最多。请回答下列问题:
(1)上述元素中,位于元素周期表p区的元素有________ (填元素符号),其中基态c原子中电子占据的最高能级的原子轨道形状是________ 。
(2)基态e原子的核外电子排布式为_______ ,其核外有____ 种不同空间运动状态的电子。
(3)b、c、d、e简单离子半径由大到小的顺序为_____ (用离子符号表示)。
(4)基态f原子的未成对电子数与成对电子数之比为______ 。
(1)上述元素中,位于元素周期表p区的元素有
(2)基态e原子的核外电子排布式为
(3)b、c、d、e简单离子半径由大到小的顺序为
(4)基态f原子的未成对电子数与成对电子数之比为
您最近一年使用:0次
解题方法
10 . 几种短周期元素的原子半径及其主要化合价见下表,下列说法正确的是
元素符号 |
|
|
|
|
|
原子半径 | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
主要化合价 |
|
|
|
|
|
A.简单阳离子的氧化性: |
B.简单离子半径: |
C.元素最高价氧化物对应的水化物的碱性: |
D.相同条件下,气态氢化物的稳定性: |
您最近一年使用:0次
2024-01-13更新
|
222次组卷
|
2卷引用:云南省昆明市五华区2023-2024学年高一上学期1月期末化学试题