名校
解题方法
1 . 现有H、N、O、Na、S、Cl、Fe、Cu八种常见元素,回答下列问题:
(1)S在周期表中的位置____________ ;
(2)Na+ 离子的结构示意图为__________________ ;
(3)能说明非金属性Cl比S强的事实是_____________ (用化学方程式表示);
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):
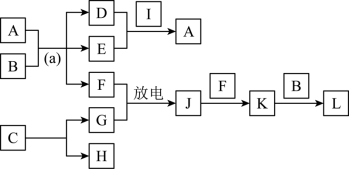
①C的化学式为____________________ ;
②D的电子式为____________________ ;
③L的稀溶液与H反应的离子方程式为___________________________________________ ;
④反应(a)的化学方程式为_________________________________________ 。
(1)S在周期表中的位置
(2)Na+ 离子的结构示意图为
(3)能说明非金属性Cl比S强的事实是
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):

①C的化学式为
②D的电子式为
③L的稀溶液与H反应的离子方程式为
④反应(a)的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、Q、M、R、T、W是原子序数依次增大的前四周期元素其中X元素的原子核外只有一个电子;X与Y原子序数之和等于Z的原子序数;Z元素的气态氢化物极易溶于水,可用作制冷剂;Q基态原子核外s能级电子总数与p能级电子总数相等;M基态原子核外有6个原子轨道排有电子,且只有1个未成对电子;R最高价氧化物的水化物是一种强酸;T为s区元素且基态原子各能层没有未成对电子;W最外层只有1个电子,其内层各能级所有轨道电子均成对。
(1)Y的基态原子最高能层符号为___________ 。
(2)Z基态原子有___________ 种不同运动状态的电子。
(3)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是___________ (用分子式表示)。
(4)Y、T能组成化合物TY2,写出其电子式___________ 。
(5)W在元素周期表中的位置为___________ ,其基态原子价层电子排布图为___________ 。
(6)下列说法不正确的是___________ 。
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
(1)Y的基态原子最高能层符号为
(2)Z基态原子有
(3)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是
(4)Y、T能组成化合物TY2,写出其电子式
(5)W在元素周期表中的位置为
(6)下列说法不正确的是
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
您最近一年使用:0次
名校
解题方法
3 . 一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
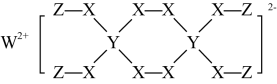

| A.工业上通过电解熔融的WX来制得W |
| B.Z、X两元素形成的某种化合物可做消毒剂 |
| C.Y的最高价氧化物对应水化物为强酸 |
| D.该漂白剂中各元素均满足8电子稳定结构 |
您最近一年使用:0次
2020-06-02更新
|
525次组卷
|
3卷引用:黑龙江省大庆铁人中学2019-2020学年高一下学期期中考试化学试题
黑龙江省大庆铁人中学2019-2020学年高一下学期期中考试化学试题(已下线)第02练 元素周期律-2020年【衔接教材·暑假作业】新高二化学(人教版)新疆乌鲁木齐市第十二中学 2022-2023学年高三下学期2月月考化学试题
名校
4 . X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断正确的是( )
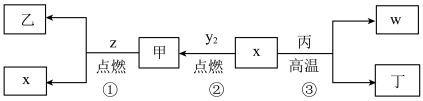

| A.反应①、②属于氧化还原反应,③属于非氧化还原反应 |
| B.Y的离子半径比Z的离子半径小 |
| C.反应③可以证明X的非金属性强于W |
| D.一定条件下,x与甲反应生成丁 |
您最近一年使用:0次
2019-12-19更新
|
835次组卷
|
7卷引用:黑龙江省大庆铁人中学2022-2023学年高一下学期期中考试化学试题
解题方法
5 . Q、R、X、Y、Z、L六种元素的原子序数依次增大,R和L是同主族元素,R的最外层电子数比次外层电子数少1,L的单质常温常压下是紫黑色固体。Q和X形成的离子化合物XQ是碱石灰的主要成分。X、Y、Z位于同一周期,Y的外围电子数是最外层电子数的6倍,Z位于ds区且不能和稀硫酸反应生成H2。请回答下列问题:
(1)Q的价层电子排布式为___________________ ,L的含氧酸HLO3中L的杂化方式为__________ ,酸根LO3-的离子构型为________________ 。
(2)ZR42-的配体是______ ,在ZSO4溶液中加入过量KCN,生成配合物[Z(CN)4]2—,则1mol该配合物中含有的π键的数目是_______ 。与Z同周期的元素中,与Z原子最外层电子数相等的元素还有_________ (填元素符号)
(3)Y的氧化物呈如下图所示的无限链状结构,则该氧化物的化学式为______________ 。
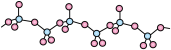
(4)X和Z的晶体堆积模型相同,配位数为______________ ,已知X原子半径约为200pm,则晶体X的密度为__________________ g/cm3(计算结果保留两位有效数字)。
(5)XL2晶体含有层状结构,其层内有强极性共价键,层间以范德华力相连接,则XL2的晶体类型是___________ 。
(1)Q的价层电子排布式为
(2)ZR42-的配体是
(3)Y的氧化物呈如下图所示的无限链状结构,则该氧化物的化学式为

(4)X和Z的晶体堆积模型相同,配位数为
(5)XL2晶体含有层状结构,其层内有强极性共价键,层间以范德华力相连接,则XL2的晶体类型是
您最近一年使用:0次
名校
6 . 两种短周期元素X和Y,可以组成化合物XY3,当Y的原子序数为m时,X的原子序数为
①m- 4 ②m +4 ③m+8 ④m-2 ⑤m +6
①m- 4 ②m +4 ③m+8 ④m-2 ⑤m +6
| A.①②④⑤ | B.①②③⑤ | C.①②③④ | D.①②③④⑤ |
您最近一年使用:0次
2018-04-01更新
|
495次组卷
|
6卷引用:黑龙江省大兴安岭漠河县第一中学2018-2019学年高一上学期期中考试化学试题
名校
7 . 某矿石由前20号元素中的四种组成,其化学式为WYZX4。X、Y、Z、W分布在三个周期,原子序数依次增大,Y、W为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同一周期,Z单质是一种良好的半导体。则下列判断正确的是
| A.Y、Z的氧化物都有两性 | B.气态氢化物的稳定性:Z>X |
| C.原子半径:W>Y>Z>X | D.最高价氧化物对应水化物的碱性:Y>W |
您最近一年使用:0次
8 . A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C为_________ 。(填写相应的元素符号)E的电子式为 ____________ 。
(2)写出A、B的化合物与E反应的化学方程式:_____________ 。
(3)A、B两元素形成化合物属_____________ (“离子”或“共价”)化合物。
(4)写出D元素的最高价氧化物的水化物和A反应的化学方程式:______ 。
(1)C为
(2)写出A、B的化合物与E反应的化学方程式:
(3)A、B两元素形成化合物属
(4)写出D元素的最高价氧化物的水化物和A反应的化学方程式:
您最近一年使用:0次
解题方法
9 . 有A、B、C、D、E五种短周期元素,元素A的一种原子无中子,元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ne的电子层结构相同,试回答:
(1)它们的元素名称是:A__ B__ C__ D__ E__ 。
(2)A与B的化合物以______ 键结合,写出BA4的电子式___________ ;
C和E的化合物以______ 键结合,写出E2C的电子式___________ ;
(3)A、B、C、E的原子半径从大到小的顺序为(写元素符号)______________________ ;
(4)写出A和C的化合物(A2C)与C和E的化合物(E2C2)反应的化学方程式:_________________________________ 。
(1)它们的元素名称是:A
(2)A与B的化合物以
C和E的化合物以
(3)A、B、C、E的原子半径从大到小的顺序为(写元素符号)
(4)写出A和C的化合物(A2C)与C和E的化合物(E2C2)反应的化学方程式:
您最近一年使用:0次



