名校
1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_____ ;N的简单离子的核外电子排布示意图为_____ 。
(2)用电子式表示化合物YN的形成过程:_____ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:_____ 。
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_____ (填字母)。
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:_____ 。
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。
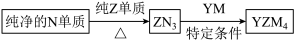
特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为_____ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_____ (填编号)。
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为_____ (用代数式表示)。
(1)Y在周期表中的位置是
(2)用电子式表示化合物YN的形成过程:
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。

特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为
您最近一年使用:0次
解题方法
2 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近一年使用:0次
解题方法
3 . 下表是元素周期表中的一部分:
根据a~i在周期表中的位置,回答下列问题:
(1)a~i的单质中,化学性质最不活泼的是______ (填化学式,下同),氧化性最强的是_______ 。
(2)a与b形成的简单化合物的电子式是___________ 。
(3)最高价氧化物对应的水化物酸性最强的是___________ (填化学式);e、f的最高价氧化物对应的水化物之间反应的离子方程式为________________________ 。
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为___________________ ,该反应中氧化剂与还原剂的物质的量之比为_________ 。
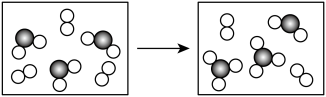
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______________________ 。
I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第1周期 | a | |||||||
| 第2周期 | b | c | d | |||||
| 第3周期 | e | f | g | h | i | |||
(1)a~i的单质中,化学性质最不活泼的是
(2)a与b形成的简单化合物的电子式是
(3)最高价氧化物对应的水化物酸性最强的是
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近一年使用:0次
名校
4 . 短周期元素W、X、Y、Z、Q、R的原子序数依次增大,c、d、e、f、h是由这些元素组成的二元化合物,自然界中硬度最大的单质和a都由X组成,b由W、Y、Q三种元素组成,d能使品红溶液褪色,是液体,上述物质的转化关系如下图所示(个别产物略去)。请回答下列问题:
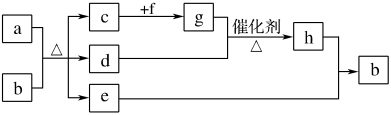
(1)R在元素周期表中的位置:_______ 。
(2)化合物f的电子式:_______ 该化合物存在的化学键种类是:_______ ;化合物c的结构式:_______ 。
(3)用电子式表示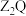 的形成过程为
的形成过程为_______ 。
(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_______ 、_______ ,这两种酸式盐相互反应的离子方程式为_______ 。
(5)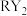 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体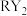 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:_______ 。
(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。

(1)R在元素周期表中的位置:
(2)化合物f的电子式:
(3)用电子式表示
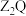 的形成过程为
的形成过程为(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
(5)
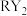 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体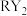 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。
| A.7.32L | B.6.72L | C.20.16L | D.30.24L |
您最近一年使用:0次
解题方法
5 . X、Y、Z、W 是原子序数依次增大的短周期元素,Y 和W同主族,且X、Z原子序数之和是Y、W原子序数之和的 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
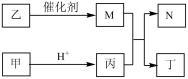
(1)W在元素周期表中的位置是_______________________ 。
(2)Y、Z、W的离子半径由大到小的顺序为__________ (用元素符号表示)。
(3)写出乙的电子式_____________ ,M 的结构式_____________________ 。
(4)丁与H2S相比沸点高的是_______ (用化学式表示);原因是_______________ 。
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理______________ (填“相同”或“不相同”);N使酸性KMnO4溶液褪色的离子方程式为 ________________________ 。
 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是
(2)Y、Z、W的离子半径由大到小的顺序为
(3)写出乙的电子式
(4)丁与H2S相比沸点高的是
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理
您最近一年使用:0次
名校
6 . 如图为元素周期表的一部分,列出了前四周期11种主族元素在周期表中的位置。

请回答下列问题:
(1)元素E的原子结构示意图为___________ ,I在元素周期表中的位置为___________ ,C与I形成的化合物的电子式为___________ 。
(2)G与J形成原子数之比为 的化合物P,P是日常生活中常见的物质,P分子的结构式为
的化合物P,P是日常生活中常见的物质,P分子的结构式为___________ ,空间构型为___________ ,P的沸点与元素K的氢化物的沸点大小关系为___________ (用化学式表示),原因是___________ 。
(3)元素D的氧化物与氢氧化钠溶液反应的离子方程式为___________ 。
(4)J、F、G、K可以形成原子个数之比为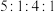 的化合物M,M的化学式为
的化合物M,M的化学式为___________ ;M中含有的化学键类型为___________ ,J、F、G、K还可以形成原子个数之比为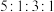 的化合物N,M与N反应的离子方程式为
的化合物N,M与N反应的离子方程式为___________ 。
(5)下列各图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________ 。

请回答下列问题:
(1)元素E的原子结构示意图为
(2)G与J形成原子数之比为
 的化合物P,P是日常生活中常见的物质,P分子的结构式为
的化合物P,P是日常生活中常见的物质,P分子的结构式为(3)元素D的氧化物与氢氧化钠溶液反应的离子方程式为
(4)J、F、G、K可以形成原子个数之比为
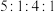 的化合物M,M的化学式为
的化合物M,M的化学式为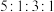 的化合物N,M与N反应的离子方程式为
的化合物N,M与N反应的离子方程式为(5)下列各图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是
 |  |  |
| A.原子半径 | B.原子最外层电子数 | C.原子序数 |
您最近一年使用:0次
7 . 下表是元素周期表中前四周期的部分元素,表中所列字母分别代表一种元素。
回答下列问题:
(1)i在元素周期表中的位置是__________ 。
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为__________ (填写离子符号)。
(3)n与o形成的化合物为__________ (填写化学式),将该化合物进行焰色试验,火焰呈__________ 色。
(4)用电子式表示g和m形成化合物的过程__________ 。
(5)将足量d的氢化物溶于水,再取少量 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为__________ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入 盐酸中。
盐酸中。
实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:
______  (选填“>”或“<”);
(选填“>”或“<”);
②利用元素周期律对上述实验结论进行解释__________ 。
(7)向 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:__________ 。
a | b | |||||||
c | d | e | f | |||||
g | h | i | j | k | l | m | ||
o | n | |||||||
(1)i在元素周期表中的位置是
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为
(3)n与o形成的化合物为
(4)用电子式表示g和m形成化合物的过程
(5)将足量d的氢化物溶于水,再取少量
 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入
 盐酸中。
盐酸中。实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:

 (选填“>”或“<”);
(选填“>”或“<”);②利用元素周期律对上述实验结论进行解释
(7)向
 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:
您最近一年使用:0次
2023-02-17更新
|
194次组卷
|
3卷引用:四川省眉山市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . X、Y、Z、Q、W、R 六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由 X、Z、Q 三种元素 组成。医学中常用QR 溶液配制生理盐水。化合物乙由X、R 两种元素组成。请回答下列问题:
(1)Z 的离子结构示意图为___________ ,由X、Z、Q 三种元素组成的化合物与 R 单质反应的离子方程式___________ 。
(2)元素 Y 在元素周期表中的位置是第___________ 周期___________ 族
(3)与R 处于同一主族气态氢化物最稳定的元素是___________
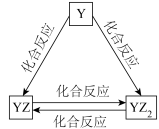
(4)Y元素的单质及其化合物能发生如图所示的转化,则 Y元素为___________ (填元素符号)。在甲溶液中通入少量YZ2气体,写出该反应的离子方程式:___________ 。
(5)W 的单质既能与甲溶液反应,又能与乙溶液反应。常温下,将 W 的单质和甲溶液混合,发生反应的离子方程式___________ 。
(1)Z 的离子结构示意图为
(2)元素 Y 在元素周期表中的位置是第
(3)与R 处于同一主族气态氢化物最稳定的元素是
(4)Y元素的单质及其化合物能发生如图所示的转化,则 Y元素为

(5)W 的单质既能与甲溶液反应,又能与乙溶液反应。常温下,将 W 的单质和甲溶液混合,发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)A在元素周期表中的位置为___________ ,画出基态B原子的轨道表示式___________ 。
(2)B的简单气态氢化物的沸点___________ (填“高于”或“低于”)PH3,原因是___________ 。
(3)A、B、C三种元素的电负性由高到低的排列次序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(5)G元素可形成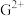 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(6)短周期元素 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是___________ (填“离子”或“共价”)化合物。推测 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物___________ (填“能”或“不能”)与 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
| A | 原子核外有6个电子 |
| B | 原子序数比 大1 大1 |
| C | 基态原子中 电子总数与p电子总数相等 电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子价层电子排布式为3s23p1 |
| F | 基态原子的最外层p 轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属,其高价氯化物的盐溶液常用于刻蚀铜制印刷电路板 |
(2)B的简单气态氢化物的沸点
(3)A、B、C三种元素的电负性由高到低的排列次序为
(4)已知元素A、B形成的
 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为(5)G元素可形成
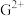 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(6)短周期元素
 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
您最近一年使用:0次
2022-07-25更新
|
963次组卷
|
3卷引用:陕西省西安市莲湖区2021-2022学年高二下学期期末质量检测化学(B卷)试题
解题方法
10 . 一种用于合成治疗免疫疾病药物的物质,其结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,乙与Q同主族,Q和W的简单离子具有相同的电子层结构。
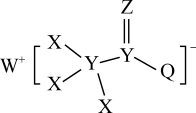
(1)W在元素周期表中的位置为_______ 。
(2)五种元素原子半径由大到小的顺序为_______ (用元素符号表。示),Z、Q、W的离子半径最小的是_______ (填离子符号)。
(3)元素W、Z可形成化合物 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:_______ (用元素符号表示)。
(4) 的水化物与Al反应的化学方程式为
的水化物与Al反应的化学方程式为_______ 。
(5)元素W的金属性_______ (填“>”或“<”)元素Na的金属性,下列方法可证明这一事实的是_______ (填字母)。
a.比较元素W的单质和Na单质分别与水反应的剧烈程度
b.比较元素W与Na最高价氧化物对应水化物碱性的强弱
c.比较常温下W的单质与Na的单质的物理状态
d.比较二者原子半径的大小

(1)W在元素周期表中的位置为
(2)五种元素原子半径由大到小的顺序为
(3)元素W、Z可形成化合物
 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:(4)
 的水化物与Al反应的化学方程式为
的水化物与Al反应的化学方程式为(5)元素W的金属性
a.比较元素W的单质和Na单质分别与水反应的剧烈程度
b.比较元素W与Na最高价氧化物对应水化物碱性的强弱
c.比较常温下W的单质与Na的单质的物理状态
d.比较二者原子半径的大小
您最近一年使用:0次



