解题方法
1 . 下图所示是科学家新合成的一种表面涂层材料化合物的结构,其中 为原子序数依次增大的短周期主族元素,只有
为原子序数依次增大的短周期主族元素,只有  在同一周期。下列说法不正确的是
在同一周期。下列说法不正确的是
 为原子序数依次增大的短周期主族元素,只有
为原子序数依次增大的短周期主族元素,只有  在同一周期。下列说法不正确的是
在同一周期。下列说法不正确的是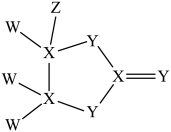
A.原子半径: |
B. 与 与 形成的所有化合物仅含有极性共价键 形成的所有化合物仅含有极性共价键 |
C. 与 与 形成的某种化合物可使澄清石灰水变浑浊 形成的某种化合物可使澄清石灰水变浑浊 |
D.最高价氧化物的水化物酸性: |
您最近一年使用:0次
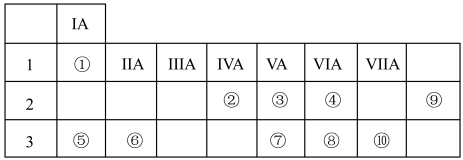
2 . 下表列出了①~⑨九种元素在周期表中的位置:
(1)元素④在周期表中所处位置_______ 。
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:_______ (写氢化物的化学式)。
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为_______ (填化学式)。
(4)元素⑧的原子结构示意图是_______ 。
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式_______ 。
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程_______ 。
(1)元素④在周期表中所处位置
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为
(4)元素⑧的原子结构示意图是
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程
您最近一年使用:0次
3 . W、X、Y、Z都是短周期元素。X、Y在元素周期表中的相对位置关系如图,W的最外层电子数是Y的最外层电子数的2倍,Z的核电荷数是W的2倍。下列说法不正确的是
A.简单离子的半径:X>W
B.最简单氢化物的稳定性:W>Z
C.最高价氧化物对应水化物的碱性;X>Y
D.X、Y、Z的最高价氧化物对应的水化物能两两发生反应
| ⅠA | ⅡA | ⅢA | ⅣA |
| X | Y |
B.最简单氢化物的稳定性:W>Z
C.最高价氧化物对应水化物的碱性;X>Y
D.X、Y、Z的最高价氧化物对应的水化物能两两发生反应
您最近一年使用:0次
名校
解题方法
4 . W、X、Y、Z四种元素在元素周期表中的相对位置如下图所示。W与Z的原子序数相差11,X的最外层电子数是内层的2倍。下列判断正确的是
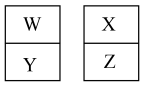
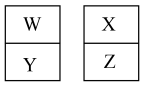
A.原子半径: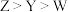 | B. 的最高正价为 的最高正价为 |
C.最高价氧化物对应的水化物的酸性: | D.W的单质在空气中燃烧生成 |
您最近一年使用:0次
解题方法
5 . X、Y、Z、W、Q为原子序数依次增大的五种短周期主族元素,最外层电子数之和为16,X与Y能形成具有10电子的微粒 ,X与Z能形成共价化合物
,X与Z能形成共价化合物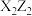 ,该化合物受热易分解,W元素的焰色为黄色。下列说法正确的是
,该化合物受热易分解,W元素的焰色为黄色。下列说法正确的是
 ,X与Z能形成共价化合物
,X与Z能形成共价化合物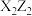 ,该化合物受热易分解,W元素的焰色为黄色。下列说法正确的是
,该化合物受热易分解,W元素的焰色为黄色。下列说法正确的是| A.元素的非金属性:Y>Z |
| B.简单离子半径:Q>W |
| C.最高价氧化物对应水化物的碱性:Q>W |
| D.X、Y、Z三种元素也可形成离子化合物 |
您最近一年使用:0次
名校
解题方法
6 . 下表列出了A~R9种元素在周期表中的位置。请回答下列问题。
(1)在这9种元素中,最外层电子数为1的元素为_____ (填元素符号),化学性质最不活泼的是_____ (填元素符号)。
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(3)F、A、D三种元素的离子半径由大到小的顺序排列为_____ (填离子符号)。
(4)用电子式表示由C和H组成的化合物的形成过程:_____ 。
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为_____ 。
(6)由E和G所形成的化合物中所含有的化学键为_____ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是
(3)F、A、D三种元素的离子半径由大到小的顺序排列为
(4)用电子式表示由C和H组成的化合物的形成过程:
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为
(6)由E和G所形成的化合物中所含有的化学键为
您最近一年使用:0次
2023-12-24更新
|
440次组卷
|
2卷引用:甘肃省武威第七中学2023-2024学年高一上学期期末考试化学试题
7 . 如图是元素周期表的一部分。回答下列问题:
(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
① 的离子结构示意图
的离子结构示意图___________ 。
②表中几种元素的最高价氧化物对应水化物酸性最强的是___________ (填化学式)。
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:___________ 。
④氰[(CN)2]是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:___________ 。
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:___________ 。
② 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)下列说法正确的是___________ (填字母)。
a.原子半径: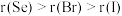
b.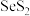 存在的化学键为极性共价键
存在的化学键为极性共价键
c.非金属性: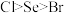
| 16 S 硫 32.06 | 17 Cl 氯 35.45 |
| 34 Se 硒 78.96 | 35 Br 溴 79.90 |
| 53 I 碘 126.9 |
①
 的离子结构示意图
的离子结构示意图②表中几种元素的最高价氧化物对应水化物酸性最强的是
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:
④氰[(CN)2]是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:
②
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:(3)下列说法正确的是
a.原子半径:
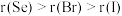
b.
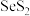 存在的化学键为极性共价键
存在的化学键为极性共价键c.非金属性:
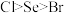
您最近一年使用:0次
解题方法
8 . A、B、C、D分别是短周期主族元素。且原子序数依次增大。已知A的最外层电子数是电子层数的3倍,A、C同主族,B的原子在短周期主族元素中原子半径最大。下列说法正确的是
| A.可以用氢氧化钠溶液吸收C的氧化物 |
| B.B2A2含有共价键,为共价化合物 |
| C.A与C形成的化合物对应的水化物一定是强酸 |
| D.C元素的非金属性比D元素的非金属性强 |
您最近一年使用:0次
2023-07-12更新
|
68次组卷
|
2卷引用:甘肃省兰州市等5地2022-2023学年高一下学期期末化学试题
名校
解题方法
9 . X、Y、Z、W、M为原子序数依次增大的短周期主族元素。已知:①元素对应的原子半径大小为X<Z<Y<M<W;②Y是组成有机物的必要元素;③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;④M的电子层数与最外层电子数相等。下列说法不正确的是
| A.Z与X形成的化合物的沸点偏高是因其分子间存在氢键 |
| B.YZ2为共价化合物,W2Z2既含有离子键又含有共价键 |
| C.W、M的简单离子半径为M>W |
| D.Z与M形成的化合物可作为耐高温材料 |
您最近一年使用:0次
名校
解题方法
10 . 元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素原子的价层电子排布式为nsn-1npn+1,则下列说法不正确的是
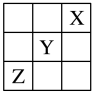

| A.Y元素在周期表的第三周期VIA族 |
| B.基态X原子的未成对电子数为3 |
| C.X元素位于周期表的p区 |
| D.Z元素原子的核外电子排布式为1s22s22p63s23p63d104s24p3 |
您最近一年使用:0次
2023-02-02更新
|
323次组卷
|
4卷引用:甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题
甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题广东省汕头市聿怀中学2022-2023学年高二上学期期末线上考试化学试题广东省河源市龙川县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题11 原子结构 原子结构与元素的性质-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)



