1 . 某中药试剂 具有泻下通便、清火消肿等功效.该药剂
具有泻下通便、清火消肿等功效.该药剂 的化学式为
的化学式为 ,
, 是原子序数依次增大的短周期元素,最外层电子数之和为14.
是原子序数依次增大的短周期元素,最外层电子数之和为14. 与
与 同主族,
同主族, 与
与 同主族,且
同主族,且 满足最高正价与最低负价的绝对值之差为4.下列说法错误的是
满足最高正价与最低负价的绝对值之差为4.下列说法错误的是
 具有泻下通便、清火消肿等功效.该药剂
具有泻下通便、清火消肿等功效.该药剂 的化学式为
的化学式为 ,
, 是原子序数依次增大的短周期元素,最外层电子数之和为14.
是原子序数依次增大的短周期元素,最外层电子数之和为14. 与
与 同主族,
同主族, 与
与 同主族,且
同主族,且 满足最高正价与最低负价的绝对值之差为4.下列说法错误的是
满足最高正价与最低负价的绝对值之差为4.下列说法错误的是A.非金属性: |
B.原子半径: |
C.由 形成的化合物既含离子键又含共价键 形成的化合物既含离子键又含共价键 |
D. 分别与 分别与 形成的化合物相互反应可能会生成 形成的化合物相互反应可能会生成 |
您最近一年使用:0次
2 . 某药物成分的结构如图所示,其中 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,且
为原子序数依次增大的短周期主族元素,且 元素原子的最外层电子数等于
元素原子的最外层电子数等于 、
、 和
和 元素原子的最外层电子数之和。下列说法正确的是
元素原子的最外层电子数之和。下列说法正确的是

 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,且
为原子序数依次增大的短周期主族元素,且 元素原子的最外层电子数等于
元素原子的最外层电子数等于 、
、 和
和 元素原子的最外层电子数之和。下列说法正确的是
元素原子的最外层电子数之和。下列说法正确的是
A.简单离子半径: |
B. 与 与 形成的化合物比 形成的化合物比 与 与 形成的化合物稳定 形成的化合物稳定 |
C. 与另外三种元素均能组成原子个数比为 与另外三种元素均能组成原子个数比为 的化合物 的化合物 |
D. 形成的单质一定属于共价晶体 形成的单质一定属于共价晶体 |
您最近一年使用:0次
名校
解题方法
3 . 一种由短周期主族元素组成的新型电池离子导体的结构如图所示,X、Y、Z原子序数依次增大,三者的核外电子数之和等于35,Y与Z位于同一周期。下列说法不正确的是
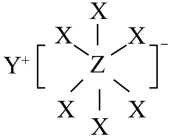
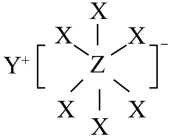
A.简单离子的半径: |
| B.同主族元素形成的简单氢化物中X的稳定性最强 |
| C.工业上常采用电解Y的氯化物溶液冶炼单质Y |
| D.Z的第一电离能大于同周期相邻的主族元素 |
您最近一年使用:0次
2023-07-18更新
|
95次组卷
|
2卷引用:山西省名校联合测评2022-2023学年高二下学期7月期末化学试题
解题方法
4 . X、Y、Z、W为原子序数依次增大的短周期主族元素,其中X、Y相邻,Y是地壳中含量最高的元素,Y、Z以原子个数比为 组成的化合物为淡黄色固体,W形成的单质可用于自来水消毒。下列说法错误的是
组成的化合物为淡黄色固体,W形成的单质可用于自来水消毒。下列说法错误的是
 组成的化合物为淡黄色固体,W形成的单质可用于自来水消毒。下列说法错误的是
组成的化合物为淡黄色固体,W形成的单质可用于自来水消毒。下列说法错误的是| A.简单离子半径:W>X>Y>Z | B.最简单氢化物的熔沸点:W>Y |
| C.X的最高价氧化物对应的水化物为强酸 | D.X、Y按原子个数比 组成的化合物为无色气体 组成的化合物为无色气体 |
您最近一年使用:0次
名校
5 . X、Y、Z、W是原子序数依次增大的短周期不同主族元素,X的2p轨道有两个未成对电子,Y元素原子半径在同周期中最大,X与Y最外层电子数之和与Z的最外层电子数相等,W元素单质常温下是淡黄色固体。下列说法正确 的是
A.第一电离能: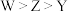 | B.简单离子半径比较: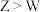 |
| C.XW2的空间结构为V形 | D.Y在元素周期表中位于p区 |
您最近一年使用:0次
2023-07-06更新
|
317次组卷
|
2卷引用:山西省应县第一中学校2022-2023学年高二下学期7月期末考试化学试题
解题方法
6 . A、B、C、D、E为前四周期不同主族的元素,原子序数依次增大。元素A可形成有机物的骨架,B、C、D位于同一周期,元素B在同周期中金属性最强,元素C的基态原子有2个未成对电子,元素D最外层电子数为A、B、E最外层电子数之和。下列说法正确的是
| A.元素第一电离能:B<D<C | B.最高价氧化物对应水化物的酸性:D>C>A |
| C.简单离子的离子半径:E<C<D | D.五种元素的单质均可在O2中燃烧 |
您最近一年使用:0次
2023-06-29更新
|
145次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题
名校
解题方法
7 . 短周期主族元素a、b、c、d,原子序数依次增大,a与氢元素形成的一种二元化合物是常用的绿色氧化剂,c元素在地壳中含量排第三位,d最外层电子数是K层电子数的3倍。下列叙述不正确的是
| A.a和b形成的二元化合物只含离子键 | B.b不一定是金属元素 |
| C.c的最高价氧化物对应的水化物是强碱 | D.简单阴离子的还原性a<d |
您最近一年使用:0次
2023-03-20更新
|
143次组卷
|
4卷引用:山西省运城市盐湖区第五高级中学2023-2024学年高一上学期期末达标化学模拟考试卷
名校
8 . X、Y、Z、R、T为短周期主族元素,其中R原子的最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断错误的是


| A.最简单氢化物的稳定性:Y<T | B.Z2Y和Z2Y2的阴、阳离子个数比相同 |
| C.最高价氧化物对应水化物的酸性:T<R | D.由Y、Z、T三种元素组成的盐不止一种 |
您最近一年使用:0次
2023-02-22更新
|
314次组卷
|
4卷引用:山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
9 . 表中列出了①~⑩所代表的十种元素在周期表中的位置,按要求填写下列空白:

(1)①、③按原子个数比为3:1组成的分子的电子式______ 。④⑤⑥三种元素的简单离子半径从大到小排序______ (用离子符号表示),元素X与⑦同一主族,X原子比⑦原子多一个电子层,X的原子结构示意图为______ 。
(2)以下组合的原子间反应最容易形成离子键的是______ (选填A、B、C、D)。
(3)写出⑥元素的最高价氧化物与氢氧化钠溶液反应的化学方程式______ ﹔磁性氧化铁溶解于元素⑩的氢化物的浓溶液发生反应的离子方程式为______ 。
(4)高铁的快速发展方便了人们的出行,工业上利用⑥的单质参与的反应焊接钢轨间的缝隙,反应的化学方程式为______ 。其中⑥的单质发生______ (填:氧化或还原)反应。
(5)只含元素①和元素⑤的化合物可在野外作供氢剂。请写出该化合物跟水反应的化学方程式______ 。1mol该化合物溶于足量水中完全反应,共转移______ mol电子。

(1)①、③按原子个数比为3:1组成的分子的电子式
(2)以下组合的原子间反应最容易形成离子键的是
| A.④和⑥ | B.①和④ | C.④和⑤ | D.⑤和⑩ |
(4)高铁的快速发展方便了人们的出行,工业上利用⑥的单质参与的反应焊接钢轨间的缝隙,反应的化学方程式为
(5)只含元素①和元素⑤的化合物可在野外作供氢剂。请写出该化合物跟水反应的化学方程式
您最近一年使用:0次
10 . 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素的最高价含氧酸能与其气态氢化物化合生成盐。下列说法不正确的是


| A.原子半径:Z>W>X>Y | B.最高价氧化物对应水化物的酸性:X>W>Z |
| C.H2ZO3是弱酸 | D.元素X、Z、W、Y的最高化合价分别与其主族序数相等 |
您最近一年使用:0次



