名校
解题方法
1 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是
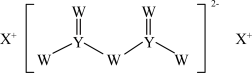

A.元素非金属性强弱的顺序为 |
B.离子半径关系 |
| C.W的简单氢化物稳定性比Y的简单氢化物稳定性低 |
| D.化合物M中W不都满足8电子稳定结构 |
您最近一年使用:0次
2024-02-27更新
|
285次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
名校
2 . 短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是P能级电于数的两倍,Z和M位于同一主族,其结构如图所示,下列说法不正确的是
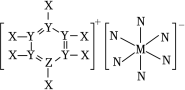

| A.原子半径:Y>Z>X |
| B.非金属性:N>M>Y |
| C.YX4和MN3的中心原子杂化方式不同 |
| D.同周期中第一电离能小于Z的元素有五种 |
您最近一年使用:0次
解题方法
3 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)②的原子结构示意图为_______ 。
(2)元素③、⑤以原子个数比为 形成的化合物含有的化学键为
形成的化合物含有的化学键为_______ 。
(3)元素③、⑨与H原子以原子个数比为 形成的化合物的电子式为
形成的化合物的电子式为_______ ,元素①、③以原子个数比为 形成的化合物的结构式为
形成的化合物的结构式为_______ 。
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是_______ ,简单氢化物的热稳定性最强的是_______ 。
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是_______ (填离子符号)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素③、⑤以原子个数比为
 形成的化合物含有的化学键为
形成的化合物含有的化学键为(3)元素③、⑨与H原子以原子个数比为
 形成的化合物的电子式为
形成的化合物的电子式为 形成的化合物的结构式为
形成的化合物的结构式为(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
4 . 现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素基态原子的价层电子排布为nsnnpn+1;C元素为周期表中电负性最大的非金属元素;D元素基态原子核外有三个电子层,最外层电子数是核外电子总数的 ,其单质可以在二氧化碳中燃烧;E元素形成的正三价离子的3d轨道为半充满状态,其合金是用量最大用途最广的金属材料;F元素基态原子的M层全充满,N层只有一个电子;G元素与A元素位于同一主族,其某种氧化物是砒霜(主要成分是As2O3)有剧毒。
,其单质可以在二氧化碳中燃烧;E元素形成的正三价离子的3d轨道为半充满状态,其合金是用量最大用途最广的金属材料;F元素基态原子的M层全充满,N层只有一个电子;G元素与A元素位于同一主族,其某种氧化物是砒霜(主要成分是As2O3)有剧毒。
(1)①C元素基态原子的价层电子排布图为___________ 。
②E3+具有___________ 种不同运动状态的的电子。
③F元素位于元素周期表的___________ 区。
(2)G元素可能的性质是___________(填标号)。
(3)根据对角线规则,Li与D具有相似性。由此可推测Li2CO3___________ 溶于水(填“难”“易”)。
(4)金属活泼性D___________ Al,第一电离能:I1(D)___________ I1(Al)(填“>”或“<”)
(5)用E的合金制造的轮船,需要在船体安装若干的镁合金或锌块,这种属于电化学保护法中的___________ 法。
 ,其单质可以在二氧化碳中燃烧;E元素形成的正三价离子的3d轨道为半充满状态,其合金是用量最大用途最广的金属材料;F元素基态原子的M层全充满,N层只有一个电子;G元素与A元素位于同一主族,其某种氧化物是砒霜(主要成分是As2O3)有剧毒。
,其单质可以在二氧化碳中燃烧;E元素形成的正三价离子的3d轨道为半充满状态,其合金是用量最大用途最广的金属材料;F元素基态原子的M层全充满,N层只有一个电子;G元素与A元素位于同一主族,其某种氧化物是砒霜(主要成分是As2O3)有剧毒。(1)①C元素基态原子的价层电子排布图为
②E3+具有
③F元素位于元素周期表的
(2)G元素可能的性质是___________(填标号)。
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
(4)金属活泼性D
(5)用E的合金制造的轮船,需要在船体安装若干的镁合金或锌块,这种属于电化学保护法中的
您最近一年使用:0次
解题方法
5 . 下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)⑧的最高价氧化物的水化物的化学式是_________ 。
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序___________ (写离子符号)。
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是___________ (填化学式)。
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(5)下列事实能判断⑤和⑥的金属性强弱的是___________ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是______ 。
a. 只具有还原性 b.Se的最低负化合价是-2价
只具有还原性 b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比 强
强
(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的最高价氧化物的水化物的化学式是
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为
(5)下列事实能判断⑤和⑥的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是
a.
 只具有还原性 b.Se的最低负化合价是-2价
只具有还原性 b.Se的最低负化合价是-2价c.Se的最高价氧化物对应水化物的酸性比
 强
强(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为
您最近一年使用:0次
6 . 下列有关元素周期表的说法中错误的是
| A.第ⅢB族到第ⅡB族10个纵行的元素都是金属元素 |
| B.0族元素原子最外层电子数均满足8电子稳定结构 |
| C.117号元素在周期表中的位置为:第七周期第ⅦA族 |
| D.在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 |
您最近一年使用:0次
解题方法
7 . W、X、Y、Z 四种短周期元素在元素周期表中的位置如图所示,其中Z位于第ⅦA族。

(1)其中最高价氧化物对应水化物酸性最强的是_______ (填化学式)。
(2)元素周期表中某区域的一些元素多用于制造半导体材料,它们是______(填标号)。
(3)Y的最简单氢化物的沸点比同主族相邻元素最简单氢化物的沸点______ 。(填“高”或“低”)
(4)W元素位于第____ 周期第___ 族,W的最高价氧化物的电子式为________ 。
(5)Y与H、Na中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物:_______ 。
(6)A是第四周期与Y同主族的元素。据此推测A不可能具有的性质是_____(填标号)。
(7)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①硝酸铯是______ 化合物(填“离子”或“共价”)。
②铯单质与H2O反应的化学反应方程式为___________ 。

(1)其中最高价氧化物对应水化物酸性最强的是
(2)元素周期表中某区域的一些元素多用于制造半导体材料,它们是______(填标号)。
| A.左下方区域的金属元素 | B.稀有气体元素 |
| C.右上方区域的非金属元素 | D.金属元素和非金属分界线附近的元素 |
(3)Y的最简单氢化物的沸点比同主族相邻元素最简单氢化物的沸点
(4)W元素位于第
(5)Y与H、Na中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物:
(6)A是第四周期与Y同主族的元素。据此推测A不可能具有的性质是_____(填标号)。
| A.在化合物中最高正化合价为+6 | B.单质可以与H2S气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(7)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①硝酸铯是
②铯单质与H2O反应的化学反应方程式为
您最近一年使用:0次
解题方法
8 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.离子半径:丁>戊>乙 |
| B.单质与氢气化合的剧烈程度:戊>丁>丙 |
C.甲和乙一定可以形成“甲乙”、“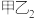 ”两种化合物 ”两种化合物 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
名校
9 . 元素X、Y、Z在周期表中的相对位置如图。已知X元素原子的价层电子排布式为 ,则下列说法错误的是
,则下列说法错误的是
 ,则下列说法错误的是
,则下列说法错误的是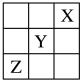
| A.Y元素原子核外d能级无电子填充 |
| B.电负性:X>Y>Z |
| C.元素的最高正价:X>Y>Z |
| D.基态Z原子的核外电子占据的最高能级的电子云轮廓图的形状为哑铃形 |
您最近一年使用:0次
2023-07-10更新
|
134次组卷
|
5卷引用:吉林省松原市前郭尔罗斯蒙古族自治县榆树实验,九台一中,前郭,农安2022-2023学年高二下学期7月期末考试化学试题
解题方法
10 . 几种主族元素在周期表中的位置如下:
(1)⑤元素的最简单氢化物是________ (填化学式),①和⑦形成的化合物中存在的化学键类型为_______ ,④和⑧形成的化合物中存在的化学键类型为________ 。
(2)①③⑥三种元素原子半径由大到小的顺序是________ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的离子结构示意图为_______ ,该元素在周期表中的位置是________ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的物质的电子式是________ ,③的单质与其反应的离子方程式为________ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是________ (填字母,下同)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑧的气态氢化物溶于水形成的酸酸性比⑦的气态氢化物溶于水形成的酸酸性强
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
(6)用电子式表示①的单质与⑨的单质形成化合物的过程:_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑨ | ⑦ | ||||
| 4 | ② | ⑧ | ||||||
(2)①③⑥三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的离子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的物质的电子式是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑧的气态氢化物溶于水形成的酸酸性比⑦的气态氢化物溶于水形成的酸酸性强
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
(6)用电子式表示①的单质与⑨的单质形成化合物的过程:
您最近一年使用:0次



