吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
吉林
高一
期末
2024-01-16
307次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学与STSE、物质结构与性质、化学实验基础
吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
吉林
高一
期末
2024-01-16
307次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学与STSE、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学与生活紧密相关,下列有关说法错误的是
| A.吉林的雾松闻名中国,雾是一种气溶胶,光束透过大雾可观察到丁达尔效应 |
| B.氘和氚用作“人造太阳”核聚变的燃料,核聚变属于化学反应 |
| C.生铁的含碳量比钢的含碳量高,合金的熔点一般比其成分金属的熔点低 |
| D.漂白粉可用于漂白棉、麻、纸张等,其长期露置在空气中会失效 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
2. 侯德榜为我国化工事业的发展做出了卓越贡献,侯氏制碱的化学反应原理为: 。下列表示反应中相关微粒的化学用语正确的是
。下列表示反应中相关微粒的化学用语正确的是
 。下列表示反应中相关微粒的化学用语正确的是
。下列表示反应中相关微粒的化学用语正确的是A.中子数为18的氯原子: |
B. 中N的化合价为:+3 中N的化合价为:+3 |
C. 的结构示意图: 的结构示意图: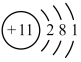 |
D. 的电离方程式: 的电离方程式: |
您最近一年使用:0次
2024-01-11更新
|
101次组卷
|
2卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
单选题
|
适中(0.65)
解题方法
3. 下列叙述正确的有
①爆炸、变色、导电一定属于化学变化
② 、
、 、CaO都能溶于水生成碱,它们都属于碱性氧化物
、CaO都能溶于水生成碱,它们都属于碱性氧化物
③ 俗称铁红,常作油漆、涂料、油墨和橡胶的红色颜料
俗称铁红,常作油漆、涂料、油墨和橡胶的红色颜料
④ 、
、 、FeS、
、FeS、 均可通过化合反应制得
均可通过化合反应制得
⑤烧碱固体、纯醋酸、乙醇均不导电,所以它们都不是电解质
⑥ 可作胃酸中和剂和食用碱
可作胃酸中和剂和食用碱
⑦往NaOH溶液中加入少量 饱和溶液,加热煮沸,制备
饱和溶液,加热煮沸,制备 胶体
胶体
①爆炸、变色、导电一定属于化学变化
②
 、
、 、CaO都能溶于水生成碱,它们都属于碱性氧化物
、CaO都能溶于水生成碱,它们都属于碱性氧化物③
 俗称铁红,常作油漆、涂料、油墨和橡胶的红色颜料
俗称铁红,常作油漆、涂料、油墨和橡胶的红色颜料④
 、
、 、FeS、
、FeS、 均可通过化合反应制得
均可通过化合反应制得⑤烧碱固体、纯醋酸、乙醇均不导电,所以它们都不是电解质
⑥
 可作胃酸中和剂和食用碱
可作胃酸中和剂和食用碱⑦往NaOH溶液中加入少量
 饱和溶液,加热煮沸,制备
饱和溶液,加热煮沸,制备 胶体
胶体| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
4. 下列各组物质的转化不是全部通过一步反应完成的是
| A.Na→NaOH→Na2CO3→NaCl | B.Al→Al2O3→Al(OH)3→A1Cl3 |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 | D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
您最近一年使用:0次
2022-04-05更新
|
509次组卷
|
7卷引用:新疆维吾尔自治区乌鲁木齐市第一中学2021--2022学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
解题方法
5. 下列离子组在给定环境下一定能大量共存的是
A.与铝反应生成氢气的溶液中: 、 、 、 、 、 、 |
B.在澄清透明的溶液中: 、 、 、 、 、 、 |
C.使紫色石蕊溶液变红的溶液中: 、 、 、 、 、 、 |
D.在碱性溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-01-11更新
|
152次组卷
|
2卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
单选题
|
适中(0.65)
6. 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A.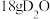 中含有的中子数为 中含有的中子数为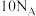 |
B. 溶液中所含 溶液中所含 数目为 数目为 |
C.常温常压下,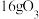 和 和 的混合气体中所含氧原子数为 的混合气体中所含氧原子数为 |
D.标准状况下,2.24L液溴与铁反应转移电子数为 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
7. 下列离子方程式正确的是
A.Na与CuSO4溶液的反应: |
B.澄清石灰水与过量NaHCO3溶液反应: |
C.向CaCl2溶液中通入CO2: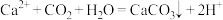 |
D.氧化铜与稀硫酸反应: |
【知识点】 离子方程式的正误判断解读 碳酸氢钠与碱反应解读
您最近一年使用:0次
单选题
|
适中(0.65)
8. 下列实验装置或操作能够达到实验目的是
| A | B | C | D |
 |  | 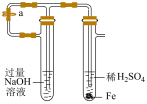 |  |
| 比较碳酸钠和碳酸氢钠的热稳定性 | 配制 稀硫酸溶液 稀硫酸溶液 | 制备并长时间看到 白色沉淀 白色沉淀 | 检验待测物中含有钾元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 高铁酸钾( )作净水剂时会产生
)作净水剂时会产生 ,该过程既能消毒杀菌,也能吸附水中悬浮物。制备
,该过程既能消毒杀菌,也能吸附水中悬浮物。制备 的一种方法的化学原理可用离子方程式表示为:
的一种方法的化学原理可用离子方程式表示为: ,下列说法错误的是
,下列说法错误的是
 )作净水剂时会产生
)作净水剂时会产生 ,该过程既能消毒杀菌,也能吸附水中悬浮物。制备
,该过程既能消毒杀菌,也能吸附水中悬浮物。制备 的一种方法的化学原理可用离子方程式表示为:
的一种方法的化学原理可用离子方程式表示为: ,下列说法错误的是
,下列说法错误的是A. 中铁元素的化合价为+6价 中铁元素的化合价为+6价 |
B. 净水时会生成 净水时会生成 胶体 胶体 |
C.由方程式可知,该条件下 的氧化性强于 的氧化性强于 |
D.反应中 作氧化剂, 作氧化剂, 被还原 被还原 |
【知识点】 氧化还原反应基本概念 氧化还原反应在生活、生产中的应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下列对图示的解释错误的是
| A | B | C | D |
NaCl的形成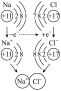 | 一些合金的硬度比其成分金属的大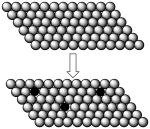 | 向 溶液中加入稀硫酸,溶液导电能力变化 溶液中加入稀硫酸,溶液导电能力变化 | NaCl溶于水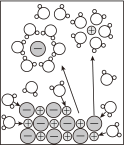 |
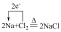 | 纯金属中加入或大或小的其他元素的原子后,改变了金属原子有规则的层状排列 | a时刻 溶液与稀硫酸恰好完全中和 溶液与稀硫酸恰好完全中和 | 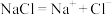 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
11. 《化学》第一册“方法导引”栏目呈现了4种学习方法,有关说法错误的是
| 选项 | 方法导引 | 内容或例子 |
| A | 认识元素及其化合物性质的视角 | 从物质类别视角分析 ,是金属氧化物,可能与酸发生反应;从化合价视角分析 ,是金属氧化物,可能与酸发生反应;从化合价视角分析 ,铁元素为+2、+3价,既具有氧化性,也具有还原性 ,铁元素为+2、+3价,既具有氧化性,也具有还原性 |
| B | 模型 | 阿伦尼乌斯提出的电离模型很好的解释了酸、碱、盐溶液的某些性质 |
| C | 实验室制取气体装置设计 | 实验室制备的氯气依次通过饱和食盐水和浓硫酸的除杂装置,可以得到干燥纯净的氯气 |
| D | 预测 | 锂和钠均为元素周期表ⅠA族元素,可预测出:在加热条件下,锂单质与氧气反应也可以生成过氧化锂 |
| A.A | B.B | C.C | D.D |
【知识点】 酸、碱、盐、氧化物解读 氯气的实验室制法解读 同主族元素性质递变规律
您最近一年使用:0次
2024-01-11更新
|
99次组卷
|
2卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
单选题
|
适中(0.65)
12. 关于卤素(用X表示)的下列叙述正确的是
A.卤素单质的颜色从 ,随着相对分子质量的增大而加深 ,随着相对分子质量的增大而加深 |
| B.HX都极易溶于水,它们的酸性随核电荷数增加而减弱 |
C.卤素单质与水反应均可用 表示 表示 |
D.X的还原性依次为 ,最高价含氧酸的酸性为 ,最高价含氧酸的酸性为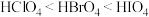 |
【知识点】 同主族元素性质递变规律理解及应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
13. 下列有关元素周期表的说法中错误的是
| A.第ⅢB族到第ⅡB族10个纵行的元素都是金属元素 |
| B.0族元素原子最外层电子数均满足8电子稳定结构 |
| C.117号元素在周期表中的位置为:第七周期第ⅦA族 |
| D.在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 |
【知识点】 元素周期表结构 “位构性”关系理解及应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
14. 某兴趣小组为测定某含铁氧化物中铁元素的百分含量,其操作流程如下:

下列说法正确的是

下列说法正确的是
| A.操作Ⅰ、操作Ⅲ均为过滤 |
B.操作Ⅱ若未使用 ,则固体d的质量小于32g ,则固体d的质量小于32g |
| C.灼烧需要的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳等 |
D.该含铁氧化物中 |
您最近一年使用:0次
2024-01-20更新
|
166次组卷
|
2卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
单选题
|
适中(0.65)
名校
15. 下列选项描述与对应图像相符的是

A.图①为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图②为 、 、 混合液中滴加盐酸产生 混合液中滴加盐酸产生 的图像 的图像 |
C.图③为 和 和 混合溶液中滴加NaOH溶液生成沉淀的图像,由图可知原混合液中 混合溶液中滴加NaOH溶液生成沉淀的图像,由图可知原混合液中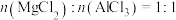 |
D.图④为 、 、 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 |
您最近一年使用:0次
2024-01-11更新
|
215次组卷
|
4卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
二、填空题 添加题型下试题
填空题
|
容易(0.94)
解题方法
16. 下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)⑧的最高价氧化物的水化物的化学式是_________ 。
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序___________ (写离子符号)。
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是___________ (填化学式)。
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(5)下列事实能判断⑤和⑥的金属性强弱的是___________ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是______ 。
a. 只具有还原性 b.Se的最低负化合价是-2价
只具有还原性 b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比 强
强
(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的最高价氧化物的水化物的化学式是
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为
(5)下列事实能判断⑤和⑥的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是
a.
 只具有还原性 b.Se的最低负化合价是-2价
只具有还原性 b.Se的最低负化合价是-2价c.Se的最高价氧化物对应水化物的酸性比
 强
强(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为
【知识点】 “位构性”关系理解及应用解读
您最近一年使用:0次
填空题
|
适中(0.65)
17. 请回答下列问题:
(1)在潜水艇和消防员的呼吸面具中, 与
与 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(2)利用 作为“腐蚀液”和覆铜板反应,制作印刷电路板的反应的离子方程式为
作为“腐蚀液”和覆铜板反应,制作印刷电路板的反应的离子方程式为______ 。
(3)“84消毒液”是生活中常用的消毒剂。某化学小组配制了500mL“84消毒液”,并在试剂瓶贴上如图所示标签。
①该“84消毒液”有效成分的物质的量浓度为____  。
。
②下列说法正确的有____ 。
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中的NaClO的物质的量浓度减小
D.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
E.定容时,若加水超过刻度线,应重新配制溶液
F.定容时,若俯视刻度线,会使所配制溶液浓度偏低
(4)曾有报道,在卫生清洁时,混合使用“84消毒液”与“洁厕灵”(主要成分是盐酸)而发生氯气中毒事件,请用离子方程式解释原因:_____ 。
(5)某溶液可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
Ⅰ.取少量该溶液,加入足量稀硫酸,无明显现象。
Ⅱ.取实验Ⅰ反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生。(已知: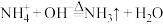 )
)
①该溶液中肯定存在的离子有______ 。
②若取原溶液进行焰色试验,焰色显黄色,则溶液中一定存在的离子有____ 种。
(1)在潜水艇和消防员的呼吸面具中,
 与
与 发生反应的化学方程式为
发生反应的化学方程式为(2)利用
 作为“腐蚀液”和覆铜板反应,制作印刷电路板的反应的离子方程式为
作为“腐蚀液”和覆铜板反应,制作印刷电路板的反应的离子方程式为(3)“84消毒液”是生活中常用的消毒剂。某化学小组配制了500mL“84消毒液”,并在试剂瓶贴上如图所示标签。
| “84消毒液” |
| 有效成分:NaClO 规格:500mL 质量分数:14.9% 密度: 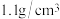 |
 。
。②下列说法正确的有
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中的NaClO的物质的量浓度减小
D.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
E.定容时,若加水超过刻度线,应重新配制溶液
F.定容时,若俯视刻度线,会使所配制溶液浓度偏低
(4)曾有报道,在卫生清洁时,混合使用“84消毒液”与“洁厕灵”(主要成分是盐酸)而发生氯气中毒事件,请用离子方程式解释原因:
(5)某溶液可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:
中的几种离子,已知各离子的物质的量浓度均相等,进行如下实验:Ⅰ.取少量该溶液,加入足量稀硫酸,无明显现象。
Ⅱ.取实验Ⅰ反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生。(已知:
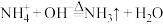 )
)①该溶液中肯定存在的离子有
②若取原溶液进行焰色试验,焰色显黄色,则溶液中一定存在的离子有
您最近一年使用:0次
三、解答题 添加题型下试题
18. 高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的 和
和 ,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取
,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取 的工艺流程如图:
的工艺流程如图:

已知: 不溶于水,也不溶于稀盐酸
不溶于水,也不溶于稀盐酸
(1)操作Ⅰ所用的玻璃仪器有:烧杯、______ 、______ 。
(2)滤渣1中除了其他不溶性杂质外,还有_____ (填化学式)。
(3)反应①的离子方程式为_______ ,检验生成物中阳离子的操作及现象是:_______ 。
(4)“沉铝”中反应的化学方程式为_______ 。
(5)沉铝后的滤液需要______ (选填“减压”、“常压”或“加压”)蒸发才能得到 固体;
固体;
(6)下列实验方案中,不能测定 和
和 混合物中
混合物中 质量分数的是_____。
质量分数的是_____。
 和
和 ,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取
,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取 的工艺流程如图:
的工艺流程如图:
已知:
 不溶于水,也不溶于稀盐酸
不溶于水,也不溶于稀盐酸(1)操作Ⅰ所用的玻璃仪器有:烧杯、
(2)滤渣1中除了其他不溶性杂质外,还有
(3)反应①的离子方程式为
(4)“沉铝”中反应的化学方程式为
(5)沉铝后的滤液需要
 固体;
固体;(6)下列实验方案中,不能测定
 和
和 混合物中
混合物中 质量分数的是_____。
质量分数的是_____。| A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物充分加热,减重b克 |
D.取a克混合物与足量 溶液充分反应,过滤、洗涤、烘干,得b克固体 溶液充分反应,过滤、洗涤、烘干,得b克固体 |
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
名校
解题方法
19.  是一种高效、安全的消毒剂。实验室制备
是一种高效、安全的消毒剂。实验室制备 的原理是用亚氯酸钠固体与纯净、干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净、干燥的氯气反应: 。如图1是实验室用于制备和收集一定量纯净的
。如图1是实验室用于制备和收集一定量纯净的 的装置(部分夹持装置已省略)。
的装置(部分夹持装置已省略)。

(1)A中装有浓盐酸的仪器名称为________ 。
(2)圆底烧瓶中发生反应的化学方程式为________ ,在该反应中浓盐酸表现的性质是______ (填序号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(3)实验中相关气体在不同溶剂中的溶解性如表所示。
E装置中的试剂是________ (填化学式)。
(4)如图是一些常用的气体收集装置,F处应选用的收集装置是______ (填序号),其中与E装置导管相连的导管口是_______ (填接口字母)。

(5) 泡腾片由
泡腾片由 、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出
、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出 。泡腾片在使用时需要加水,请补全泡腾片在水中发生反应的离子方程式:
。泡腾片在使用时需要加水,请补全泡腾片在水中发生反应的离子方程式:_____ ,___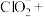 ___
___ ___
___ ___
___ ___
___ 。
。
(6)与 比较,
比较, 消毒效率是
消毒效率是 的
的____ 倍(产物均视为 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
 是一种高效、安全的消毒剂。实验室制备
是一种高效、安全的消毒剂。实验室制备 的原理是用亚氯酸钠固体与纯净、干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净、干燥的氯气反应: 。如图1是实验室用于制备和收集一定量纯净的
。如图1是实验室用于制备和收集一定量纯净的 的装置(部分夹持装置已省略)。
的装置(部分夹持装置已省略)。
(1)A中装有浓盐酸的仪器名称为
(2)圆底烧瓶中发生反应的化学方程式为
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(3)实验中相关气体在不同溶剂中的溶解性如表所示。
 |  | HCl | |
| 水 | 极易溶 | 可溶 | 极易溶 |
 | 难溶 | 易溶 | 难溶 |
(4)如图是一些常用的气体收集装置,F处应选用的收集装置是

(5)
 泡腾片由
泡腾片由 、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出
、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出 。泡腾片在使用时需要加水,请补全泡腾片在水中发生反应的离子方程式:
。泡腾片在使用时需要加水,请补全泡腾片在水中发生反应的离子方程式: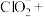 ___
___ ___
___ ___
___ ___
___ 。
。(6)与
 比较,
比较, 消毒效率是
消毒效率是 的
的 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
您最近一年使用:0次
2024-01-11更新
|
197次组卷
|
2卷引用:吉林省普通高中G6教考联盟 2023-2024 学年高一上学期期末考试化学试卷
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学与STSE、物质结构与性质、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
15
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的性质和应用 漂白粉的变质原因及检验 化学科学对人类文明发展的意义 金属与合金性能比较 | |
| 2 | 0.65 | 原子结构示意图、离子结构示意图 电离方程式 元素、核素、同位素 | |
| 3 | 0.65 | 胶体的制备 物理变化与化学变化 非电解质、电解质物质类别判断 碳酸氢钠的俗称、物理性质及用途 | |
| 4 | 0.65 | 物质的转化 钠 镁 铁 | |
| 5 | 0.85 | 限定条件下的离子共存 次氯酸及其性质 铝与强碱溶液反应 | |
| 6 | 0.65 | 22.4L/mol适用条件 氧化还原反应与NA相关推算 物质结构基础与NA相关推算 元素、核素、同位素 | |
| 7 | 0.65 | 离子方程式的正误判断 碳酸氢钠与碱反应 | |
| 8 | 0.65 | 焰色试验 碳酸钠与碳酸氢钠性质的比较 配制一定物质的量浓度的溶液的步骤、操作 | |
| 9 | 0.65 | 氧化还原反应基本概念 氧化还原反应在生活、生产中的应用 | |
| 10 | 0.65 | 物质水溶液的导电性 离子反应的发生及书写 单线桥、双线桥分析氧化还原反应 金属与合金性能比较 | |
| 11 | 0.85 | 酸、碱、盐、氧化物 氯气的实验室制法 同主族元素性质递变规律 | |
| 12 | 0.65 | 同主族元素性质递变规律理解及应用 | |
| 13 | 0.65 | 元素周期表结构 “位构性”关系理解及应用 | |
| 14 | 0.65 | 有关铁及其化合物转化的流程题型 铁及铁的氧化物混合物反应的相关计算 物质分离、提纯综合应用 | |
| 15 | 0.65 | 次氯酸及其性质 碳酸钠与盐酸的反应 氢氧化铝与强碱反应 铝盐与强碱溶液反应 | |
| 二、填空题 | |||
| 16 | 0.94 | “位构性”关系理解及应用 | |
| 17 | 0.65 | 离子方程式的书写 漂白粉和漂粉精 过氧化钠和二氧化碳反应 配制一定物质的量浓度的溶液实验的误差分析 | |
| 三、解答题 | |||
| 18 | 0.65 | 氯气与还原性化合物的反应 碳酸钠、碳酸氢钠混合物的有关求算 偏铝酸钠与二氧化碳的反应 物质分离、提纯综合应用 | 工业流程题 |
| 19 | 0.4 | 氯气的实验室制法 | 实验探究题 |



