1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最小,X、Y 、Z简单离子的核外电子排布相同,物质A的结构式如右图所示,回答下列问题:

(1)上述元素中,最高化合价数值最大的是___________ (用元素符号表示)。
(2)Y的离子结构示意图是___________ ; 其氢化物的电子式为___________ 。
(3)N、X、Y、Z简单离子的半径由大到小的顺序为___________ (用对应离子符号表示)。
(4)上述元素形成的化合物中,能腐蚀玻璃的是___________ (填化学式);生活中可用Z的单质与Y的最高价氧化物对应水化合物的反应疏通下水道,其反应的离子方程式为___________ ,该反应的还原剂与氧化剂的物质的量之比为___________ 。
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示
纯净的N单质 ZN3
ZN3 YZM4
YZM4
实验室利用YZM4遇水反应生成的氢的体积测定YZM4样品纯度。
①该反应的化学方程式___________ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是___________ (填编号)。

(1)上述元素中,最高化合价数值最大的是
(2)Y的离子结构示意图是
(3)N、X、Y、Z简单离子的半径由大到小的顺序为
(4)上述元素形成的化合物中,能腐蚀玻璃的是
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示
纯净的N单质
 ZN3
ZN3 YZM4
YZM4实验室利用YZM4遇水反应生成的氢的体积测定YZM4样品纯度。
①该反应的化学方程式
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
您最近一年使用:0次
2021-11-21更新
|
360次组卷
|
3卷引用:山东省泰安市2021-2022年高三上学期期中统考化学试题
山东省泰安市2021-2022年高三上学期期中统考化学试题山东省泰安市2022届高三上学期期中考试化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
解题方法
2 . 元素周期表前四周期的元素a、b、c、d、e的原子序数依次增大,其中a、b、c、d四种元素为短周期主族元素。a的核外电子总数与其周期序数相同,b与c同周期,c与d同族,且ba3能与abc3化合生成一种可溶性盐,该盐溶液与生石灰反应生成的气体能使湿润的红色石蕊试纸变蓝。edc4为波尔多液的主要成分之一。
回答下列问题:
(1)元素e为___________ (填元素符号),a2c的电子式为___________ 。
(2)元素a、b、c、d四种元素的简单离子半径由大到小的顺序为___________ (填离子符号)。
(3)元素a和d所形成的常见化合物的分子式为___________ ,存在的化学键类型为___________ 。
(4)写出等物质的量的bc2、dc2及足量的c2同时通入a2c中发生反应生成a2dc4和abc3的化学方程式:___________ 。
(5)单质e加入由a2c2和稀a2dc4组成的混合溶液中,溶液由无色变成蓝色,写出发生反应的离子方程式:___________ 。
回答下列问题:
(1)元素e为
(2)元素a、b、c、d四种元素的简单离子半径由大到小的顺序为
(3)元素a和d所形成的常见化合物的分子式为
(4)写出等物质的量的bc2、dc2及足量的c2同时通入a2c中发生反应生成a2dc4和abc3的化学方程式:
(5)单质e加入由a2c2和稀a2dc4组成的混合溶液中,溶液由无色变成蓝色,写出发生反应的离子方程式:
您最近一年使用:0次
2021-10-19更新
|
126次组卷
|
2卷引用:山东省德州市夏津第一中学2022届高三第一次备考监测联合考试化学试卷
名校
3 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是5种短周期主族元素的相关信息。
回答下列问题:
(1)X在元素周期表中的位置为___________ 。
(2)由Y与Z形成的一种化合物可作供氧剂,该化合物中所含化学键的类型为___________ ,该化合物的电子式为___________ 。
(3)Y、Z、Q的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(4)向 的碳酸氢盐溶液中滴加
的碳酸氢盐溶液中滴加 溶液,产生白色沉淀和气体,该条件下反应的离子方程式为
溶液,产生白色沉淀和气体,该条件下反应的离子方程式为___________ 。
(5)研究W、Q非金属性强弱的方案中不可行的是___________(填序号)。
| 元素 | 信息 |
| X | 其中一种核素在考古时常用来测定文物的年代 |
| Y | 最外层电子数是次外层电子数的3倍 |
| Z | 短周期主族元素中,其原子半径最大 |
| W | 常温下,其单质是一种黄绿色的气体 |
| Q | 最高化合价与最低化合价的代数和为4 |
(1)X在元素周期表中的位置为
(2)由Y与Z形成的一种化合物可作供氧剂,该化合物中所含化学键的类型为
(3)Y、Z、Q的简单离子半径由大到小的顺序为
(4)向
 的碳酸氢盐溶液中滴加
的碳酸氢盐溶液中滴加 溶液,产生白色沉淀和气体,该条件下反应的离子方程式为
溶液,产生白色沉淀和气体,该条件下反应的离子方程式为(5)研究W、Q非金属性强弱的方案中不可行的是___________(填序号)。
| A.比较其简单氢化物的沸点 | B.比较其单质与氢气反应的难易程度 |
| C.比较其简单阴离子的还原性 | D.比较其氧化物的水化物的酸性 |
您最近一年使用:0次
4 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)汞的原子结构示意图,汞在周期表中位于第___ 周期。
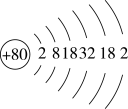
(2)氮、氧、硫3种元素对应的简单氢化物,其中最稳定的是______ (填化学式)。
(3)下列有关性质的比较能用元素周期律解释的是_______ 。
a.酸性:HClH2SO4
b.非金属性:OS
c.碱性:NaOHMg(OH)2
d.热稳定性:Na2CO3NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是______ 。
a.硒元素的最低负化合价为2价
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。
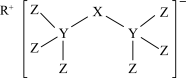
①Y的元素符号为______ 。
②X的氢化物化学式______ 。
(1)汞的原子结构示意图,汞在周期表中位于第

(2)氮、氧、硫3种元素对应的简单氢化物,其中最稳定的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HClH2SO4
b.非金属性:OS
c.碱性:NaOHMg(OH)2
d.热稳定性:Na2CO3NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为2价
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为
②X的氢化物化学式
您最近一年使用:0次
名校
解题方法
5 . 元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________ ;Z3+的离子结构示意图是____________ 。
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式__________ ;M和N气态氢化物的稳定性大小比较为________ (用化学式和“>”“<”或“=”表示)。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________ .
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_____________________________ 。
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是__________ (填化学式),示意图中转移电子的数目为______ 。
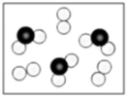


(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______________________ 。
(1)R在元素周期表中的位置是
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是



(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
2017-12-08更新
|
236次组卷
|
3卷引用:山东省烟台市2018届高三上学期期中考试化学试题
解题方法
6 . 某含氧酸盐X的化学式为ABO3。已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。
(1)若常温下A、B的单质都能与水发生反应。
①B在元素周期表中的位置是___________________ 。
②下列说法正确的是__________ (填代号)。
a.A的简单离子半径比B的简单离子半径大
b.A、B元素的最高价氧化物对应的水化物都是强电解质
c.A单质与水反应后溶液的pH比B单质与水反应后溶液的pH大
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1:3,其中一种是无氧酸盐。该反应的化学方程式为_______________________________________________ 。
(2)若X难溶于水,在空气中易氧化变质;B元素原子的最外层电子数是其电子层数的2倍。
①X能快速消除自来水中的C1O-,该反应的离子方程式为_______________________ 。
②请你设计实验验证X是否变质:___________________________________________ 。
(3)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体的电子式为______________ 。
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为________________________________________________ 。
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;b.______________________________ (任写一种)。
(1)若常温下A、B的单质都能与水发生反应。
①B在元素周期表中的位置是
②下列说法正确的是
a.A的简单离子半径比B的简单离子半径大
b.A、B元素的最高价氧化物对应的水化物都是强电解质
c.A单质与水反应后溶液的pH比B单质与水反应后溶液的pH大
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1:3,其中一种是无氧酸盐。该反应的化学方程式为
(2)若X难溶于水,在空气中易氧化变质;B元素原子的最外层电子数是其电子层数的2倍。
①X能快速消除自来水中的C1O-,该反应的离子方程式为
②请你设计实验验证X是否变质:
(3)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体的电子式为
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;b.
您最近一年使用:0次
解题方法
7 . A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大。A与E同主族,D与F同主族,且A与D能形成两种液态化合物;B的某种单质是自然界中硬度最大的物质,C与D形成的化合物是大气常见污染物之一。请回答下列问题:
(1)F在元素周期表中的位置是______ ,D、E、F三种元素其简单离子半径由大到小的顺序是_____ (用离子符号表示)
(2)元素E、F可形成多原子化合物E2Fx(x≥2).该化合物中所含的化学键类型是_______ 。
(3)元素B、C的最高价氧化物对应水化物酸性较强的是______ 。(填化学式)
(4)实验室可利用_______ (填试剂名称)清洗附着于试管内壁的F单质。
(5)写出B、E的氧化物生成D单质的化学方程式_____________ 。
(6)处理含BC-废水的方法之一是在微生物的作用下,BC-被D的单质氧化成ABD3-,同时生成C的简单氢化物,该反应的离子方程式为__________________________ 。
(1)F在元素周期表中的位置是
(2)元素E、F可形成多原子化合物E2Fx(x≥2).该化合物中所含的化学键类型是
(3)元素B、C的最高价氧化物对应水化物酸性较强的是
(4)实验室可利用
(5)写出B、E的氧化物生成D单质的化学方程式
(6)处理含BC-废水的方法之一是在微生物的作用下,BC-被D的单质氧化成ABD3-,同时生成C的简单氢化物,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 下表为元素周期表的一部分,请参照元素(1-8)在表中的位置,用化学用语回答下列问题:

(1)画出元素⑦的原子结构示意图__________ 。
(2)写出元素③的气态氢化物的电子式________ 。写出元素②的单质与元素⑧最高价含氧酸浓溶液的化学反应方程式__________ 。
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________ 。(用元素形成的酸的化学式表示)
(4)①、④、⑤、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________ 。
(5)由表中元素形成的物质X、Y、Z、M、N可发生以下反应,其中物质X、Y、N均为两种元素组成的物质。
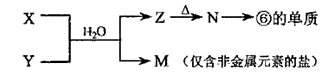
X溶液与Y溶液反应的离子方程式为_____________________ 。

(1)画出元素⑦的原子结构示意图
(2)写出元素③的气态氢化物的电子式
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(4)①、④、⑤、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(5)由表中元素形成的物质X、Y、Z、M、N可发生以下反应,其中物质X、Y、N均为两种元素组成的物质。
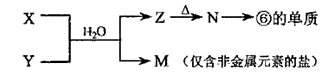
X溶液与Y溶液反应的离子方程式为
您最近一年使用:0次
9 . 已知有原子序数依次增大的A、B、C、D、E五种短周期元素和过渡元素F,其相关信息如表所示:
(1)上述六种元素中,金属性最强的元素在周期表中的位置是_______ 。
(2)分子式为B5Al2且其一氯代物只有一种的有机物的名称为_______ 。
(3)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈_______ 性;将M的浓溶液滴加到Mg(OH)2悬浊液中,描述现象并解释产生该现象的原因_______ 。
(4)D元素的最高价氧化物对应的水化物与E元素的单质反应的离子方程式为_______ 。
(5)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为_______ 。
1 | A与C形成化合物的水溶液呈碱性 |
2 | B的最高正价与最低负价的代数和为0 |
3 | D的常见化合物的焰色反应为黄色 |
4 | E是同周期中简单离子半径最小的元素 |
(2)分子式为B5Al2且其一氯代物只有一种的有机物的名称为
(3)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈
(4)D元素的最高价氧化物对应的水化物与E元素的单质反应的离子方程式为
(5)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为
您最近一年使用:0次
10 . a、b、c、d、e、f六种短周期元素,原子序数依次增大,有关信息如下。
请回答下列问题:
(1)f元素在周期表中的位置为:____________________________ 。
(2)上述六种元素中,原子半径最大的是(写元素符号)__________ 。
(3)请写出能证明f元素的非金属性比S元素的非金属性强的化学方程式:_________________ 。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
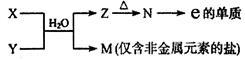
X溶液与Y溶液反应的离子方程式为____________________________ 。
物质M中存在的化学键类型为______________________
(5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗l L1.8 mol·L-1NaOH溶液和16.8 L O2(体积已换算成标准状况),则两种气体的分子式及物质的量分别为__________ 、___________ ,生成硫酸铜物质的量为_______________ 。
| 元素 | 有关信息 |
| a | 单质为密度最小的气体 |
| b | 最高价氧化物对应的水化物可与其氢化物反应,生成离子化合物 |
| c | 地壳中含量最多的元素 |
| d | 单质须保存在煤油中 |
| e | 同周期元素对应的简单离子中,离子半径最小 |
| f | 原子最外层电子数比次外层电子数少 1个 |
(1)f元素在周期表中的位置为:
(2)上述六种元素中,原子半径最大的是(写元素符号)
(3)请写出能证明f元素的非金属性比S元素的非金属性强的化学方程式:
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
物质M中存在的化学键类型为
(5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗l L1.8 mol·L-1NaOH溶液和16.8 L O2(体积已换算成标准状况),则两种气体的分子式及物质的量分别为
您最近一年使用:0次



