名校
1 . 科学家在嫦娥五号取回的月壤中发现了水及大量玻璃性质的物质,经分析,月壤中含有原子序数依次增大的短周期主族元素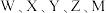 ,其中
,其中 分别位于不同周期,
分别位于不同周期,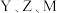 为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是
为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是 最外层电子数的2倍。下列说法正确的是
最外层电子数的2倍。下列说法正确的是
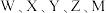 ,其中
,其中 分别位于不同周期,
分别位于不同周期,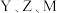 为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是
为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是 最外层电子数的2倍。下列说法正确的是
最外层电子数的2倍。下列说法正确的是A. 元素形成的化合物中的化学键为离子键 元素形成的化合物中的化学键为离子键 |
B. 的简单离子半径: 的简单离子半径: |
C.非金属性: |
D. 与 与 只能形成一种化合物 只能形成一种化合物 |
您最近半年使用:0次
名校
解题方法
2 .  是合成出的第一个稀有气体化合物,研究表明
是合成出的第一个稀有气体化合物,研究表明 属于离子化合物,关于
属于离子化合物,关于 下列推测
下列推测不合理 的是
 是合成出的第一个稀有气体化合物,研究表明
是合成出的第一个稀有气体化合物,研究表明 属于离子化合物,关于
属于离子化合物,关于 下列推测
下列推测A.可由 与 与 一定条件下反应制得 一定条件下反应制得 |
| B.具有较强的氧化性 |
C.第一个被合成,是因为氙原子与 、 、 等稀有气体原子相比较半径大,电离能小 等稀有气体原子相比较半径大,电离能小 |
| D.易溶于四氯化碳 |
您最近半年使用:0次
解题方法
3 . 前20号主族元素X、Y、Z、W的原子序数依次增大,它们的原子序数之和等于35,最外层电子数之和为13。分析试剂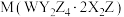 的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知
的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知 时固体的分子式为
时固体的分子式为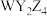 。下列叙述正确的是
。下列叙述正确的是

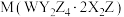 的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知
的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知 时固体的分子式为
时固体的分子式为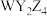 。下列叙述正确的是
。下列叙述正确的是
A.电负性: |
| B.Y的氢化物沸点一定低于Z的氢化物 |
C. 阶段失去1个 阶段失去1个 分子 分子 |
D.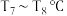 阶段生成的固体为WZ 阶段生成的固体为WZ |
您最近半年使用:0次
2023-06-01更新
|
50次组卷
|
2卷引用:江西省2022-2023学年高二下学期5月统一调研测试化学试题
4 . X、Y、Z、M、Q五种短周期元素原子序数依次增大,且只有两种金属元素。X原子无中子,Y、Z元素相邻,M元素是短周期元素中原子半径最大的,X、Z、M的原子序数之和等于Y、Q原子序数之和。下列说法不正确的是
| A.Y元素在自然界中可能存在游离态 |
| B.短周期元素中M元素的单质还原性最强 |
| C.Z元素可能形成不止一种单质 |
| D.X、M、Q均能形成多种氧化物 |
您最近半年使用:0次
2023-02-17更新
|
324次组卷
|
3卷引用:四川省眉山市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 某反应体系中反应物与生成物有:K2SO4、CaSO4、MnSO4、CaC2O4、KMnO4、H2SO4、H2O和一种未知气体X。根据上述信息回答下列问题:
(1)S原子核外电子共占据_______ 个能级,能量最高电子排布式为_______ 。
(2)下列说法正确的是_______。
(3)充填气象观测气球时,可用CaH2与H2O反应制H2,反应的化学方程式为_______ 。CaH2、BaH2属于_______ 晶体,熔点CaH2_______ BaH2(填>、<、=),从物质结构角度解释原因_______ 。
(4)下列事实能说明C、S两元素非金属性强弱的是_______。
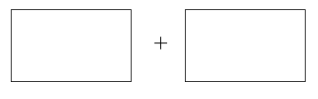
(5)已知CaC2O4在反应中失去电子,则该反应的氧化剂是_______ ,在标准状况下生成11.2L X时,有0.5mol电子转移,共消耗0.25mol CaC2O4,X的化学式为_______ 。将氧化剂和还原剂的化学式及配平后的系数填入下列方框中,并标出电子转移的方向和数目:_______ 。
(1)S原子核外电子共占据
(2)下列说法正确的是_______。
| A.CaH2和CaO2中,阴阳离子个数比相同 |
| B.O原子与S原子核外电子的伸展方向都是4种 |
| C.H2SO4在该反应中的作用和实验室与亚硫酸钠反应制SO2时相同 |
| D.原子核外电子的能级数由少到多的顺序为:H<C<O<S |
(4)下列事实能说明C、S两元素非金属性强弱的是_______。
| A.同浓度Na2CO3和Na2SO4的pH | B.浓硫酸和碳酸的氧化性 |
| C.CH4和H2S的稳定性 | D.CS2中共用电子对的偏移 |

您最近半年使用:0次
名校
解题方法
6 . 已知a、b、c、d、e、f为原子序数依次增大的前20号主族元素。a的原子半径为短周期原子中最小的,b的最高正价为同周期主族元素中最高的,c 的原子半径小于b,d的单质在空气中燃烧,产物有两种离子化合物和一种非金属单质,e的一种气态氧化物可作为高效消毒剂,f原子的核外电子总数等于a、b、d原子中所含质子数的总和。下列说法正确的是
| A.简单离子半径:e>d>b |
| B.简单氢化物的沸点:c>e |
| C.a、b两种元素组成的简单化合物能使湿润的蓝色石蕊试纸变红 |
| D.元素c、f组成的二元化合物能与水反应放出大量热 |
您最近半年使用:0次
名校
解题方法
7 . 无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在科技发展中发挥着重要的作用。完成下列填空:
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指_______ ,58是指_______ 。
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是_______ ,SiH4的空间构型为_______ 。
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为_______ ,T的电子式为_______ 。
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是_______ (选填编号)
a.SiO + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.
c.SiH4 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑
d.Si+O2 SiO2;C+O2
SiO2;C+O2 CO2
CO2
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO
 + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.

c.SiH4
 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑d.Si+O2
 SiO2;C+O2
SiO2;C+O2 CO2
CO2
您最近半年使用:0次
解题方法
8 . 固体X由4种元素组成的化合物,它是一种重要的催化剂。某学习小组开展了如图实验进行探究:
实验一:
实验二:
已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素___ ,X的化学式____ 。
(2)写出固体X与氢氧化钠溶液反应的化学方程式____ 。
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式____ 。
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是____ 。为了观察溶液A中的水合金属阳离子为浅紫色,可以采取____ 的措施。
实验一:

实验二:

已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素
(2)写出固体X与氢氧化钠溶液反应的化学方程式
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是
您最近半年使用:0次
名校
解题方法
9 . 如图是某元素形成物质的“价—类”图,图中显示各物质之间的转化关系。其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D的大16,回答下列问题:
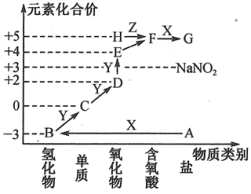
(1)写出下列物质的化学式:C.____ ;H_____ 。
(2)实验室制取B的化学方程式为_____ ,可用____ 试纸检验B是否集满。在B的催化氧化反应中,氧化剂与还原剂的物质的量之比为_____ 。
(3) 都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:
都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:____ 。
(4)写出 溶液与F的稀溶液反应的离子方程式:
溶液与F的稀溶液反应的离子方程式:_____ 。
(5)已知 在空气中会氧化变质(部分转化为G),取部分变质后的固体样品
在空气中会氧化变质(部分转化为G),取部分变质后的固体样品 与
与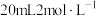 的酸性
的酸性 溶液恰好完全反应(
溶液恰好完全反应( 全部转化为
全部转化为 ),则样品中
),则样品中 的纯度为
的纯度为___ 。

(1)写出下列物质的化学式:C.
(2)实验室制取B的化学方程式为
(3)
 都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:
都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:(4)写出
 溶液与F的稀溶液反应的离子方程式:
溶液与F的稀溶液反应的离子方程式:(5)已知
 在空气中会氧化变质(部分转化为G),取部分变质后的固体样品
在空气中会氧化变质(部分转化为G),取部分变质后的固体样品 与
与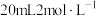 的酸性
的酸性 溶液恰好完全反应(
溶液恰好完全反应( 全部转化为
全部转化为 ),则样品中
),则样品中 的纯度为
的纯度为
您最近半年使用:0次
2022-05-04更新
|
134次组卷
|
2卷引用:辽宁省凌源市三校2021-2022学年高一下学期4月检测化学试题
名校
解题方法
10 . 麻黄素是中枢神经兴奋剂,结构简式如图所示,其组成元素Y、X、W、Z为原子序数依次增大的前两周期主族元素。
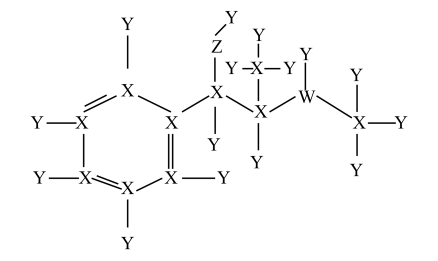
下列说法不正确的是

下列说法不正确的是
| A.由Y、W、Z三种元素形成的化合物一定能抑制水的电离 |
| B.简单氢化物沸点:Z>W>X |
| C.原子半径:X>W>Z>Y |
| D.X、W、Z都可以分别与Y形成既含极性键又含非极性键的共价化合物 |
您最近半年使用:0次
2022-03-07更新
|
194次组卷
|
3卷引用:湘豫名校联考2022届高三下学期3月理科综合能力测试化学试题



