名校
解题方法
1 . 在遭遇冰雪灾害时,常使用一种融雪剂其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是___ ,电子式是___ ,该物质中化学键类型是__ 。
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图___ ;是D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的电子式为___ ,化学键类型为___ (填“离子键”或“共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成___ ,其化学键类型为___ ;加热时生成___ ,其化学键类型为____ ,电子式为___ 。
(1)该融雪剂的化学式是
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成
您最近一年使用:0次
2020-10-10更新
|
428次组卷
|
9卷引用:北京市人大附中2017-2018学年下学期高一第一次月考 化学试卷
北京市人大附中2017-2018学年下学期高一第一次月考 化学试卷人教版2017-2018学年高一化学必修二同步训练:第一章 物质结构 元素周期律山西省祁县中学2017-2018学年高一下学期第一次月考化学试题人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第三节 化学键高一必修第一册(苏教2019)专题5 第二单元 微粒之间的相互作用力2(已下线)4.3.1 离子键(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)黑龙江省讷河市拉哈一中2020-2021学年高一下学期3月月考化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020-2021学年高一上学期期末化学试题(已下线)易错专题29 化学键-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)
名校
解题方法
2 . 下表是元素周期表的一部分,请用化学用语回答有关问题:
(1)⑥的氢氧化物中,所含化学键的类型是______ 。
(2)①和④可形成化合物,用电子式表示其形成过程______ 。
(3)⑦的最高价氧化物的水化物与⑧的最高价氧化物的水化物反应的离子方程式为_____ 。
(4)研究物质的性质差异性是学习的重要方法之一。②、③、⑧、⑨四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种酸的是______ 。
(5)能说明元素⑤的非金属性强于元素⑨的非金属性的实验事实是_____ (填字母)。
A.两种单质的熔沸点不同
B.两种单质与氢气化合的难易程度
C.比较这两种元素的最高价氧化物的水化物的酸性
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)⑥的氢氧化物中,所含化学键的类型是
(2)①和④可形成化合物,用电子式表示其形成过程
(3)⑦的最高价氧化物的水化物与⑧的最高价氧化物的水化物反应的离子方程式为
(4)研究物质的性质差异性是学习的重要方法之一。②、③、⑧、⑨四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种酸的是
(5)能说明元素⑤的非金属性强于元素⑨的非金属性的实验事实是
A.两种单质的熔沸点不同
B.两种单质与氢气化合的难易程度
C.比较这两种元素的最高价氧化物的水化物的酸性
您最近一年使用:0次
名校
解题方法
3 . 周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同;基态b原子的核外电子占据3个能级,且最高能级轨道为半充满状态;c的最外层电子数是内层电子数的3倍;d的原子序数是c的两倍;基态e原子3d轨道上有4个单电子。
回答下列问题:
(1)b、c、d电负性最大的是___ (填元素符号)。
(2)b单质分子中σ键与π键的个数比为___ 。
(3)a与c可形成两种二元化合物分子,两种物质可以任意比互溶。其中一种不稳定,可分解产生c的单质,该化合物分子中的c原子的杂化方式为___ ;这两种物质的互溶物中,存在的化学键有___ (填序号)。
①极性共价键 ②非极性共价键 ③离子键 ④金属键 ⑤氢键 ⑥范德华力
(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的酸是___ (填化学式,下同);酸根呈正三角形结构的酸是___ ,试从两者结构特点判断该酸分子与酸根离子的稳定性:酸分子___ 酸根离子(填“>”或“<”)。
(5)元素e在周期表中的位置是___ 区;e的一种常见氯化物中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在,结构式为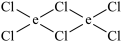 ,请补写e的元素符号并用“→”表示出其中的配位键
,请补写e的元素符号并用“→”表示出其中的配位键___ 。
回答下列问题:
(1)b、c、d电负性最大的是
(2)b单质分子中σ键与π键的个数比为
(3)a与c可形成两种二元化合物分子,两种物质可以任意比互溶。其中一种不稳定,可分解产生c的单质,该化合物分子中的c原子的杂化方式为
①极性共价键 ②非极性共价键 ③离子键 ④金属键 ⑤氢键 ⑥范德华力
(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的酸是
(5)元素e在周期表中的位置是
 ,请补写e的元素符号并用“→”表示出其中的配位键
,请补写e的元素符号并用“→”表示出其中的配位键
您最近一年使用:0次
2019-12-02更新
|
516次组卷
|
4卷引用:北京市十一学校2023-2024学年高三一模化学试题
北京市十一学校2023-2024学年高三一模化学试题山东省潍坊市2020届高三9月月考化学试题山东省潍坊市2019—2020学年高三上学期10月质量检测化学试题(已下线)易错点15 化学键-备战2023年高考化学考试易错题
名校
4 . 如表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
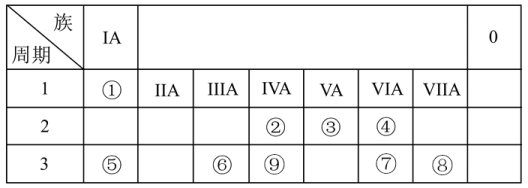
(1)第三周期中元素非金属性最强的元素的原子结构示意图为____________ 。
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)___________ 。
(3)用电子式表示④的简单氢化物的形成过程______________ 。
(4)下列可以判断⑤和⑥金属性强弱的是_________
a.⑤单质的熔点比⑥单质低
b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈
d.⑤最高价氧化物的水化物的碱性比⑥强
(5)由表中①、③、④、⑥、⑧元素形成的常见物质Z、M、N可发生以下反应:
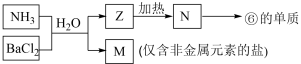
a.M中所含的化学键种类为(若含共价键,请标明极性或非极性)___________ 。
b.N→⑥的单质的化学方程式__________________ 。

(1)第三周期中元素非金属性最强的元素的原子结构示意图为
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)
(3)用电子式表示④的简单氢化物的形成过程
(4)下列可以判断⑤和⑥金属性强弱的是
a.⑤单质的熔点比⑥单质低
b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈
d.⑤最高价氧化物的水化物的碱性比⑥强
(5)由表中①、③、④、⑥、⑧元素形成的常见物质Z、M、N可发生以下反应:

a.M中所含的化学键种类为(若含共价键,请标明极性或非极性)
b.N→⑥的单质的化学方程式
您最近一年使用:0次
2019-09-12更新
|
481次组卷
|
5卷引用:【全国百强校】北京市第四中学2017-2018学年高一下学期期末考试化学(选考)试题
名校
5 . 几种主族元素(过渡元素略去)在周期表中的位置如下:
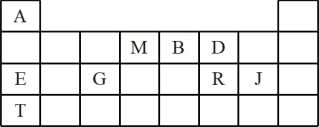
(1) A的元素符号是________ 。
(2) D在周期表中的位置是_________________________________ 。
(3) E、G、T的原子半径由大到小的顺序是_________ (填元素符号)。
(4)硒元素(34Se)与D同主族,其非金属性比D_________ (填“强”或“弱”),从原子结构角度解释其原因:___________________________________________________________________ 。
(5) R元素的原子结构示意图为_________________ 。
(6) E、G、J三种元素最高价氧化物对应水化物两两之间能反应,离子方程式分别为:H+ +OH-=H2O、_________________________________ 、______________________ 。
(7) E、D两元素能形成原子个数比2:1和1:1的两种化合物。2:1 型化合物的电子式为______________________________ 。1:1型化合物的化学式以及所含化学键类型是_____________________________ 。
(8)A与M形成的分子可能是______________ (填字母序号)。


(1) A的元素符号是
(2) D在周期表中的位置是
(3) E、G、T的原子半径由大到小的顺序是
(4)硒元素(34Se)与D同主族,其非金属性比D
(5) R元素的原子结构示意图为
(6) E、G、J三种元素最高价氧化物对应水化物两两之间能反应,离子方程式分别为:H+ +OH-=H2O、
(7) E、D两元素能形成原子个数比2:1和1:1的两种化合物。2:1 型化合物的电子式为
(8)A与M形成的分子可能是

您最近一年使用:0次
9-10高一下·北京·期末
解题方法
6 . 甲、乙、丙、丁是四种短周期元素,它们的原子序数依次增大,其中甲和丙、乙和丁分别是同主族元素,又知乙、丁两元素的原子核中质子数之和是甲、丙两元素原子核中质子数之和的2倍,甲元素的一种同位素核内无中子。
(1)写出甲、乙、丙三种元素组成的化合物的电子式________ ,指出其中含有的化学键的类型_______ 、_______ 。
(2)写出乙与丙按原子个数比1:1组成的化合物与水反应的化学方程式_________ 。
(3)用甲元素的单质与乙元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特质的防止透过的隔膜,在A极通入甲的单质,B极通入乙的单质,则A极是该电池的_______ 极,B极的电极反应式是 ___________
(1)写出甲、乙、丙三种元素组成的化合物的电子式
(2)写出乙与丙按原子个数比1:1组成的化合物与水反应的化学方程式
(3)用甲元素的单质与乙元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特质的防止透过的隔膜,在A极通入甲的单质,B极通入乙的单质,则A极是该电池的
您最近一年使用:0次



