解题方法
1 .  分子中化学键类型为
分子中化学键类型为_______ ; 分子的空间填充模型为
分子的空间填充模型为_______ 。
 分子中化学键类型为
分子中化学键类型为 分子的空间填充模型为
分子的空间填充模型为A. B.
B.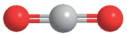
您最近一年使用:0次
2 . 目前,全世界镍(Ni)的消费量仅次于铜、铝、铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___________ 晶体;基态Ni原子的电子排布式为___________ 。
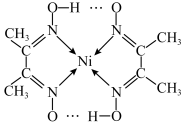
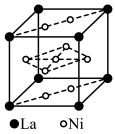
(2)某配合物结构如图所示,分子内含有的作用力有___________ (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键___________ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)某配合物结构如图所示,分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
您最近一年使用:0次
3 . 下列化合物中既存在离子键,又存在极性键的是
| A.H2O | B.NH4Cl | C.Na2O | D.Na2O2 |
您最近一年使用:0次
名校
4 . 下列各组物质中,含有化学键类型都相同的是
| A.HI和NaI | B.NaI和KOH |
| C.CO2和HCl | D.Cl2和NaBr |
您最近一年使用:0次
2024-03-08更新
|
227次组卷
|
3卷引用:江苏省盐城市响水县清源高级中学2023-2024学年高二上学期期中化学试卷(必修)
5 . 所有的分子中都存在化学键。( )
您最近一年使用:0次
6 . 下列说法中错误的是
| A.根据对角线规则,B和Si的性质具有相似性 |
| B.电负性越大的原子,对键合电子的吸引力越大 |
C.气体单质分子中,一定含有 键 键 |
| D.金属焰色试验的原理是电子跃迁释放能量 |
您最近一年使用:0次
2023-12-26更新
|
340次组卷
|
2卷引用:陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 如图所示,a为乙二胺四乙酸(EDTA),易与金属离子形成整合物,b为EDTA与Ca2+形成的鳌合物。下列叙述正确的是
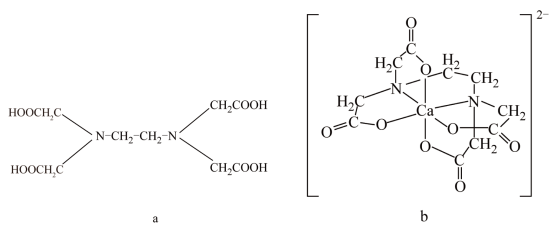

| A.a和b中N原子均采取sp3杂化 |
| B.b中Ca2+的配位数为4,配位原子是C原子 |
| C.a和b中C原子杂化方式相同 |
| D.b中含有共价键、离子键和配位键 |
您最近一年使用:0次
8 . 反应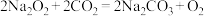 可用于呼吸面具供氧。下列说法正确的是
可用于呼吸面具供氧。下列说法正确的是
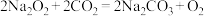 可用于呼吸面具供氧。下列说法正确的是
可用于呼吸面具供氧。下列说法正确的是A.N的外围电子排布式为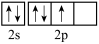 | B.Na2O2的电子式为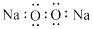 |
| C.Na2CO3含离子键和共价键 | D.中子数为10的氧原子可表示为16O |
您最近一年使用:0次
名校
解题方法
9 . 下列说法中正确的是
| A.NH3和BF3分子中所有原子的最外层都达到了8电子稳定结构 |
| B.Na2O2、NaClO中所含化学键类型完全相同 |
| C.等物质的量的CaC2和NaCN中含有的共用电子对数不相等 |
| D.汽车防撞气囊中的NaN3分解:2NaN3=2Na+3N2↑有离子键、共价键的断裂,有金属键、共价键的形成 |
您最近一年使用:0次
名校
解题方法
10 . 明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。
(1)基态Zn原子核外的最高能层符号是___________ 。
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有___________ (填编号),乳酸锌中C原子的杂化方式有___________ 。
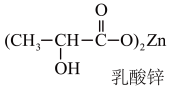
A离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
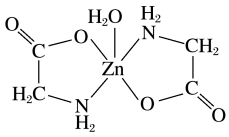
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是___________ , 的配位数为
的配位数为___________ ;甘氨酸易溶于水,试从结构角度解释___________ 。
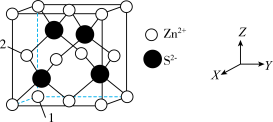
(4)Zn与S形成某种化合物的晶胞如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为___________ 。
②已知晶胞参数为apm,阿伏伽德罗常数为 ,求该晶胞的密度
,求该晶胞的密度
___________  (写计算表达式)。
(写计算表达式)。
(1)基态Zn原子核外的最高能层符号是
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有

A离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是
 的配位数为
的配位数为
(4)Zn与S形成某种化合物的晶胞如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为
②已知晶胞参数为apm,阿伏伽德罗常数为
 ,求该晶胞的密度
,求该晶胞的密度
 (写计算表达式)。
(写计算表达式)。
您最近一年使用:0次



