真题
解题方法
1 . ⅣA族元素具有丰富的化学性质,其化合物有着广泛的应用。回答下列问题:
(1)该族元素基态原子核外未成对电子数为_____ ,在与其他元素形成化合物时,呈现的最高化合价为_____ 。
(2) 俗称电石,该化合物中不存在的化学键类型为
俗称电石,该化合物中不存在的化学键类型为_____ (填标号)。
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷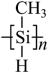 ,其中电负性最大的元素是
,其中电负性最大的元素是_____ ,硅原子的杂化轨道类型为_____ 。
(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因:_____ 。
(5)结晶型 可作为放射性探测器元件材料,其立方晶胞如图所示。其中
可作为放射性探测器元件材料,其立方晶胞如图所示。其中 的配位数为
的配位数为_____ 。设 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为_____  (列出计算式)。
(列出计算式)。
(1)该族元素基态原子核外未成对电子数为
(2)
 俗称电石,该化合物中不存在的化学键类型为
俗称电石,该化合物中不存在的化学键类型为a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷
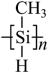 ,其中电负性最大的元素是
,其中电负性最大的元素是(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因:
| 物质 | 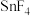 |  |  | 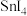 |
熔点/ | 442 | 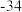 | 29 | 143 |
 可作为放射性探测器元件材料,其立方晶胞如图所示。其中
可作为放射性探测器元件材料,其立方晶胞如图所示。其中 的配位数为
的配位数为 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为 (列出计算式)。
(列出计算式)。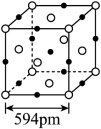
您最近一年使用:0次
解题方法
2 . 下列物质所形成的晶体中只含有离子键的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
3 . 下列属于离子晶体并含有共价键的是
| A.CH3OH | B.Mg3N2 | C.NH4Cl | D.SiO2 |
您最近一年使用:0次
解题方法
4 . 按要求回答下列问题:
(1)根据价层电子对互斥模型,H2S 、SO2 、SO3 的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(2)晶体中H2O 和 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为___________ ,试判断 H2O 和  的键角大小关系并说明原因:
的键角大小关系并说明原因:___________ 。
(3)成语“信口雌黄 ”中的雌黄分子式为 As2S3,分子结构如图,As 原子的杂化方式为___________ , 雌黄和 SnCl2 在盐酸中反应转化为雄黄(As4S4)和 SnCl4 并放出 H2S 气体。___________ 。
(5)Zn2+的核外电子排布式为___________ ,在元素周期表中,该元素在___________ (填“s”“p”“d”“f”或“ds”)区。。
(6)S8与热的浓NaOH 溶液反应的产物之一为Na2S3,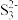 的空间结构为
的空间结构为___________ 。
(7)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,则[H2F]+ 的空间结构为___________ 。
(8)Na3AsO4 中含有的化学键类型包括___________ ; 的空间结构为
的空间结构为 ___________ 。
(1)根据价层电子对互斥模型,H2S 、SO2 、SO3 的气态分子中,中心原子价层电子对数不同于其他分子的是
(2)晶体中H2O 和
 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为 的键角大小关系并说明原因:
的键角大小关系并说明原因:(3)成语“信口雌黄 ”中的雌黄分子式为 As2S3,分子结构如图,As 原子的杂化方式为

(5)Zn2+的核外电子排布式为
(6)S8与热的浓NaOH 溶液反应的产物之一为Na2S3,
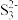 的空间结构为
的空间结构为(7)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,则[H2F]+ 的空间结构为
(8)Na3AsO4 中含有的化学键类型包括
 的空间结构为
的空间结构为
您最近一年使用:0次
解题方法
5 . 下列各种物质的晶体中,化学键类型和晶体类型均完全相同的是
A. 和 和 | B. 和 和 |
C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
6 . 下列物质中含有非极性共价键的是
A. | B. | C.Ar | D. |
您最近一年使用:0次
解题方法
7 . 含巯基(-SH)有机化合物Ⅰ是重金属元素汞的解毒剂,化合物Ⅱ是一种强酸。下列说法不正确的是
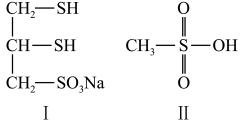
| A.在Ⅱ中各原子最外层均有8电子 | B.在Ⅱ中含有σ键和π键 |
| C.在Ⅰ中存在离子键与共价键 | D.在Ⅱ中硫氧键的键能不完全相同 |
您最近一年使用:0次
名校
解题方法
8 . 随原子序数的递增,八种短周期元素的原子半径、最高正价或最低负价的变化如图所示。下列叙述正确的是
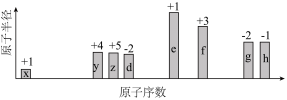
| A.原子形成的简单离子半径的大小顺序为d>e>f |
| B.d、e组成的化合物都只含离子键 |
| C.x、z、d组成的化合物都是共价化合物 |
| D.e、f、g最高价氧化物对应的水化物互相都能发生反应 |
您最近一年使用:0次
解题方法
9 . 下列物质中,含有极性共价键的离子晶体是
| A.CaCl2 | B.K2SO4 | C.Na2O | D.Na2O2 |
您最近一年使用:0次
10 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近一年使用:0次



