1 .  是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
1.基态Mn原子的价电子轨道表示式为___________ ;其核外有___________ 种不同能量的电子。
2.氯酸钾熔融状态下的电离方程式为___________ ;双氧水的电子式为___________ 。
 是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。1.基态Mn原子的价电子轨道表示式为
2.氯酸钾熔融状态下的电离方程式为
您最近一年使用:0次
解题方法
2 . 锰、铬、铜、铁四种元素的基态原子中,有五个未成对电子的原子核外电子排布式为___________ 。
您最近一年使用:0次
名校
解题方法
3 . 下图为“点击化学”的一种反应
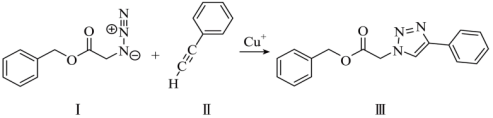
(1)基态 的价层电子排布式为
的价层电子排布式为___________ 。
(2)写出I中C、N、O的原子半径大小(按从小到大排列)___________ ;
(3)画出基态N原子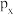 轨道的电子云轮廓图
轨道的电子云轮廓图___________ ;
(4)从绿色化学角度分析,该反应的优点在于(写出一点即可)___________ 。

(1)基态
 的价层电子排布式为
的价层电子排布式为(2)写出I中C、N、O的原子半径大小(按从小到大排列)
(3)画出基态N原子
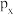 轨道的电子云轮廓图
轨道的电子云轮廓图(4)从绿色化学角度分析,该反应的优点在于(写出一点即可)
您最近一年使用:0次
2023高三·全国·专题练习
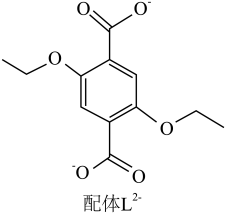
4 . 配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn4O]6+构成。
(1)基态Zn2+的电子排布式为______ 。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为______ 形;每个L2-中采取sp2杂化的C原子数目为______ 个,C与O之间形成σ键的数目为______ 个。

(1)基态Zn2+的电子排布式为
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为
您最近一年使用:0次
2023高三·全国·专题练习
5 . 谷氨酸[HOOC—CH(NH2)—CH2—CH2—COOH]的钠盐——谷氨酸钠(C5H8NO4Na)是味精的主要成分,谷氨酸分子中C原子的杂化方式为___________ ,C原子与O原子所形成的化学键中σ键与π键的数目比N(σ)∶N(π)=___________ ,π键的特征是两块电子云呈___________ 对称。
您最近一年使用:0次
6 . (2021·山东卷)基态F原子核外电子的运动状态有___________ 种。
您最近一年使用:0次
7 . 某国产电动汽车推出的“刀片电池”具有强环境适应性,更安全可靠。“刀片电池”正极材料使用了磷酸亚铁锂(LiFePO4)。磷酸亚铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
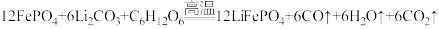
(1)铁是26号元素,它是___________ 。(选填编号)
a.主族元素b.副族元素c.短周期元素d.长周期元素
磷元素的原子核外有___________ 种运动状态不同的电子。
(2)上述方程式中,CO2的电子式为___________ ,属于第二周期的元素,原子半径由小到大排列___________ 。
(3)反应中的氧化剂是___________ ;当有0.1molLiFePO4生成时,转移电子的数目为___________ 个。
磷酸亚铁锂也可以用(CH3COO)2Fe、NH4H2PO4和LiOH为原料制备。
(4)NH4H2PO4溶于水形成的溶液中存在:c(H+)+c( )=c(OH-)+c(H2PO
)=c(OH-)+c(H2PO )+
)+___________ 。
(5)请解释(CH3COO)2Fe溶于水显酸性的原因___________ 。
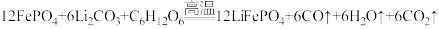
(1)铁是26号元素,它是
a.主族元素b.副族元素c.短周期元素d.长周期元素
磷元素的原子核外有
(2)上述方程式中,CO2的电子式为
(3)反应中的氧化剂是
磷酸亚铁锂也可以用(CH3COO)2Fe、NH4H2PO4和LiOH为原料制备。
(4)NH4H2PO4溶于水形成的溶液中存在:c(H+)+c(
 )=c(OH-)+c(H2PO
)=c(OH-)+c(H2PO )+
)+(5)请解释(CH3COO)2Fe溶于水显酸性的原因
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . 回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______ 形象化描述。在基态 原子中,核外存在
原子中,核外存在_______ 对自旋相反的电子。
(3)黄铜是人类最早使用的合金之一,主要由 和
和 组成。第一电离能
组成。第一电离能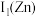
_______ (填“大于”或“小于”) 。原因是
。原因是_______ 。
(4)元素铜与镍的第二电离能分别为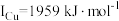 、
、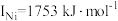 ,
,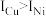 的原因是
的原因是_______ 。
(5)比较离子半径:
_______ (填“大于”“等于”或“小于”) 。
。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
 原子中,核外存在
原子中,核外存在(3)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。第一电离能
组成。第一电离能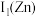
 。原因是
。原因是(4)元素铜与镍的第二电离能分别为
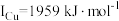 、
、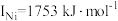 ,
,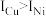 的原因是
的原因是(5)比较离子半径:

 。
。
您最近一年使用:0次
9 . 点击化学的代表反应为铜催化的叠氨-炔基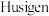 环加成反应,
环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:
(1)基态 核外电子排布式为
核外电子排布式为_______ ;基态O原子未成对电子有_______ 个。
(2)F、O、N、C的第一电离能从小到大的顺序是_______ 。
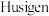 环加成反应,
环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:(1)基态
 核外电子排布式为
核外电子排布式为(2)F、O、N、C的第一电离能从小到大的顺序是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
10 . 电子云轮廓图形和电子运动状态的判断。
(1)[2018·全国卷Ⅱ,35(1)节选]基态S原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)[2017·全国卷Ⅰ,35(2)基态K原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(3)[2021·山东,16(1)]基态F原子核外电子的运动状态,有_______ 种。
(1)[2018·全国卷Ⅱ,35(1)节选]基态S原子电子占据最高能级的电子云轮廓图为
(2)[2017·全国卷Ⅰ,35(2)基态K原子中,核外电子占据的最高能层的符号是
(3)[2021·山东,16(1)]基态F原子核外电子的运动状态,有
您最近一年使用:0次



