名校
解题方法
1 . 下列有关说法正确的是
| A.电子云通常用小点的疏密来表示,小点密表示在该空间的电子数多 |
B.已知 的价电子排布式为 的价电子排布式为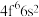 , , 的价电子排布式为 的价电子排布式为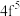 |
C. 的核外电子排布式为 的核外电子排布式为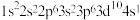 ,所以 ,所以 位于s区 位于s区 |
D.原子光谱的特征谱线用于鉴定元素,从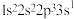 跃迁至 跃迁至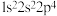 时吸收能量 时吸收能量 |
您最近半年使用:0次
2021-02-15更新
|
344次组卷
|
6卷引用:湖北省孝感市2019-2020学年高二上学期期末质量联合检测化学试题
名校
解题方法
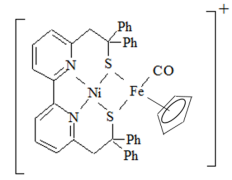
2 . (1)Ni2+和Fe2+可形成如图所示的配合物离子,其中铁的一个配体为茂环阴离子( ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为______ ,配合物离子中铁周围的价电子数共有______ 个,S元素的杂化方式为______ ,该配合物离子中的 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为______ (用Ⅰ或Ⅱ表示)。
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为______ 。基态Cs原子中电子占据的能量最高的轨道是______ ,能量最低的空轨道是______ 。
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(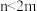 ),则可以形成大π键,表示为
),则可以形成大π键,表示为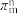 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为______ 。
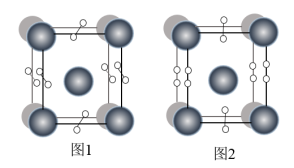
(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有______ 种。若K之间底面上的最近距离为a pm,竖直方向上为c pm,图2表示的晶体密度为______  ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
 ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(
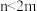 ),则可以形成大π键,表示为
),则可以形成大π键,表示为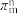 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有
 ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
您最近半年使用:0次
2021-01-03更新
|
576次组卷
|
4卷引用:八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)
八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题
3 . 下列关于氢元素的说法中不正确的是
| A.氢元素是宇宙中最丰富的元素 |
| B.氢原子核外电子的电子云轮廓图是球形 |
| C.氢元素与其他元素形成的化合物都是共价化合物 |
| D.氢原子光谱是氢原子的电子跃迁产生的 |
您最近半年使用:0次
4 . 按原子核外电子排布,可把周期表里的元素划分成5个区。以下元素中属于ds区的是
| A.钙 | B.镍 | C.锌 | D.硒 |
您最近半年使用:0次
2020-10-13更新
|
243次组卷
|
4卷引用:湖北省武汉市五校联合体2019-2020学年高二下学期期中考试化学试题
湖北省武汉市五校联合体2019-2020学年高二下学期期中考试化学试题(已下线)1.1 原子结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)福建省莆田第七中学2020-2021学年高二下学期期中考试化学(A卷)试题河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题
5 . 下列表达方式或说法正确的是
A.CO2的分子模型示意图: |
B.p-p-π键电子云模型: |
C.某元素原子的电子排布图: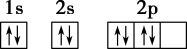 |
D.乙烯分子的比例模型: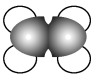 |
您最近半年使用:0次
2020-09-15更新
|
143次组卷
|
2卷引用:河北省唐山市玉田县第一中学2019-2020学年高二第二次阶段性考试化学试题
6 . 下列说法正确的是( )
| A.所有原子的任一能层的s电子的电子云轮廓图都是球形,只是半径大小不同 |
| B.各原子能级之间的能量差完全一致,这是量子力学中原子光谱分析的理论基础 |
| C.1s电子云界面图是一个球面,小黑点的疏密程度来表示电子在空间出现概率大小 |
| D.原子中电子在具有确定半径的圆周轨道上像火车一样高速运转着 |
您最近半年使用:0次
解题方法
7 . 下列有关说法正确的是( )
A.水合铜离子的模型如图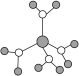 ,该微粒中存在极性共价键、配位键、离子键 ,该微粒中存在极性共价键、配位键、离子键 |
B.CaF2晶体的晶胞如图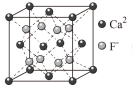 ,距离F-最近的Ca2+组成正四面体 ,距离F-最近的Ca2+组成正四面体 |
C.氢原子的电子云图如图 ,氢原子核外大多数电子在原子核附近运动 ,氢原子核外大多数电子在原子核附近运动 |
D.金属Cu中Cu原子堆积模型如图 ,为面心立方最密堆积,Cu原子的配位数均为12,晶胞空间利用率68% ,为面心立方最密堆积,Cu原子的配位数均为12,晶胞空间利用率68% |
您最近半年使用:0次
2020-04-05更新
|
287次组卷
|
3卷引用:山东省枣庄三中、高密一中、莱西一中2020届高三下学期第一次在线联考化学试题
山东省枣庄三中、高密一中、莱西一中2020届高三下学期第一次在线联考化学试题湖北省龙泉中学、宜昌一中2021届高三下学期2月联合考试化学试题(已下线)第38讲 晶体结构与性质(精练)-2022年一轮复习讲练测
解题方法
8 . 有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1) 原子的核外电子排布式:
原子的核外电子排布式:___________________ 。
(2) 元素在元素周期表中的位置
元素在元素周期表中的位置________ ;离子半径:
____  (填“大于”或“小于”)
(填“大于”或“小于”)
(3) 原子的电子排布图是
原子的电子排布图是______ ,能量最高的电子为______ 轨道上的电子,其轨道呈______ 形。
(4) 的结构示意图是
的结构示意图是________________ 。
(5) 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为________ ,与 最高价氧化物对应的水化物反应的化学方程式为
最高价氧化物对应的水化物反应的化学方程式为________________ 。
(6)举一实例说明 元素的非金属性比
元素的非金属性比 元素的强
元素的强_______________
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B |  与 与 同周期,其最高价氧化物的水化物呈两性 同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)
 原子的核外电子排布式:
原子的核外电子排布式:(2)
 元素在元素周期表中的位置
元素在元素周期表中的位置
 (填“大于”或“小于”)
(填“大于”或“小于”)(3)
 原子的电子排布图是
原子的电子排布图是(4)
 的结构示意图是
的结构示意图是(5)
 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为 最高价氧化物对应的水化物反应的化学方程式为
最高价氧化物对应的水化物反应的化学方程式为(6)举一实例说明
 元素的非金属性比
元素的非金属性比 元素的强
元素的强
您最近半年使用:0次
名校
解题方法
9 . 下列叙述中,正确的是
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.如果某一基态原子3p轨道上仅有2个电子,它们自旋方向必然相反 |
| D.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
您最近半年使用:0次
2020-01-07更新
|
73次组卷
|
6卷引用:湖北省宜昌市葛洲坝中学2018-2019学年高二下学期期中考试化学试题
名校
10 . 下列叙述不正确 的是
| A.“量子化”就是不连续的意思,微观粒子运动均有此特点 |
| B.光谱分析的基本原理是每种元素都有自己的特征谱线 |
| C.原子中的电子在具有确定半径的圆周轨道上像火车一样高速运转着 |
| D.电子由2p能级跃迁到3s能级时,原子的吸收光谱可通过光谱仪直接摄取 |
您最近半年使用:0次
2019-10-17更新
|
213次组卷
|
4卷引用:宁夏银川市银川二中2019-2020学年高二上学期第一次月考化学试题



