名校
解题方法
1 . 元素周期表中铋元素的数据见图,下列说法不正确的是

| A.铋原子s轨道的形状是球形的,p轨道的形状是哑铃形 |
| B.铋元素的相对原子质量是209.0 |
| C.铋原子6p能级中6px、6py、6pz轨道上各有一个电子 |
| D.铋原子最外层有5个能量相同的电子 |
您最近半年使用:0次
2022-10-01更新
|
434次组卷
|
10卷引用:贵州省黄平县且兰高级中学2018-2019学年高二上学期12月份考试化学试题
贵州省黄平县且兰高级中学2018-2019学年高二上学期12月份考试化学试题安徽省郎溪中学2018-2019学年高二下学期第一次月考化学试题宁夏回族自治区吴忠市吴忠中学2019-2020学年高二下学期期中考试化学试题(已下线)第1讲 原子结构 核外电子排布鲁科版2019选择性必修2第1章综合检测卷山西省怀仁市大地学校2020-2021学年高二下学期第三次月考化学试题海南省东方市东方中学2021-2022学年高二下学期期中考试化学试题黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题山西省朔州市怀仁市大地学校2021-2022学年高二上学期第四次月考化学试题山东省青岛一中2023-2024学年高一下学期4月月考化学试卷
解题方法
2 . 下列描述碳原子结构的化学用语正确的是
A.碳-12原子: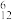 C C |
B.原子结构示意图: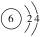 |
C.原子核外能量最高的电子云图: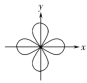 |
D.原子的轨道表示式: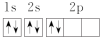 |
您最近半年使用:0次
2022-07-31更新
|
665次组卷
|
8卷引用:2015届上海市普陀区高三一模化学试卷
2015届上海市普陀区高三一模化学试卷(已下线)上海市普陀区2015届高三12月质量调研(一模)化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)(已下线)【知识图鉴】单元讲练测选择性必修2第1章01讲核心(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
3 . 有关氮原子核外p亚层中的电子的说法错误的是
| A.能量相同 | B.电子云形状相同 |
| C.电子云伸展方向相同 | D.自旋方向相同 |
您最近半年使用:0次
2021-12-27更新
|
366次组卷
|
4卷引用:上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题
上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题(已下线)第37练 原子结构-2023年高考化学一轮复习小题多维练(全国通用)上海市嘉定区2022届高三一模化学试题福建省漳平第二中学2021-2022学年高二下学期第一次月考化学试题
4 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X与Y位于不同周期,Y与W位于同一主族,Y、Z原子的最外层电子数之和等于它们的内层电子总数之和,W在同周期主族元素的基态原子中第一电离能最大。下列说法错误的是
| A.与X同主族的元素的基态原子最外层电子所占轨道呈球形 |
| B.Y、Z、W均位于元素周期表的p区 |
| C.Z与W可形成多种化合物 |
| D.Z的最高价氧化物对应的水化物为强酸 |
您最近半年使用:0次
2021-12-10更新
|
680次组卷
|
6卷引用:山东省2020年届高考全真模拟(泰安三模)化学试题
山东省2020年届高考全真模拟(泰安三模)化学试题(已下线)第十一单元 物质结构与性质(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)第1.2.1讲 原子结构与元素周期表-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)山东省日照市五莲县2021-2022学年高二上学期期中考试化学试题山东省日照市莒县、五莲县、岚山区2021-2022学年高二11月联合考试化学试题(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)
5 . 在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
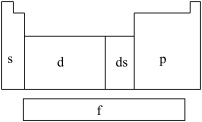
(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为___________ ,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近半年使用:0次
2021-12-04更新
|
551次组卷
|
9卷引用:同步君 选修3 第一章 第二节 原子结构与元素周期表
(已下线)同步君 选修3 第一章 第二节 原子结构与元素周期表高中化学人教版 选修三 第1章 原子结构与性质 原子结构与元素周期表山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(已下线)1.2.1 原子结构与元素周期表(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第1课时 原子核外电子排布的周期性2.2.1原子核外电子排布的周期性 课后
20-21高二·全国·课时练习
解题方法
6 . 在基态多电子原子中,关于核外电子能量的叙述错误的是
| A.最易失去的电子能量最高 |
| B.同一个电子层上的不同能级上的原子轨道,能量大小不同 |
| C.p轨道电子能量一定高于s轨道电子能量 |
| D.在离核最近区域内运动的电子能量最低 |
您最近半年使用:0次
20-21高二·全国·课时练习
7 . 电子作为微观粒子,其运动特征与宏观物体的运动特征有着明显的区别,下列关于电子运动特征的叙述中,正确的是
| A.电子的运动根本就不存在运动轨迹 |
| B.电子在原子核周围的空间内围绕原子核做圆周运动,只不过每一个圆周的半径不同而已 |
| C.电子的运动速率特别快,所以其能量特别大 |
| D.电子的运动速率特别快,运动范围特别小,不可能同时准确地测定其位置和速度 |
您最近半年使用:0次
12-13高二下·山东济南·期中
名校
8 . 玻尔理论、量子力学理论都是对核外电子运动状态的描述,根据对它们的理解,判断下列叙述正确的是
| A.因为s轨道的形状是球形的,所以s电子做圆周运动 |
| B.3px、3py、3pz的差异之处在于三者中电子(基态)的能量不同 |
| C.在同一能级上运动的电子,其运动状态肯定相同 |
| D.原子轨道和电子云都是用来形象地描述电子运动状态的 |
您最近半年使用:0次
2021-02-16更新
|
331次组卷
|
7卷引用:2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷
(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷河南省信阳市2016-2017学年高二下学期期中考试化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第37练 原子结构-2023年高考化学一轮复习小题多维练(全国通用)(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第1节 原子结构模型河北省邯郸市大名县第一中学2021-2022学年高二上学期第二次月考化学试题
名校
解题方法
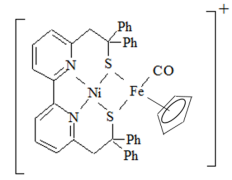
9 . (1)Ni2+和Fe2+可形成如图所示的配合物离子,其中铁的一个配体为茂环阴离子( ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为______ ,配合物离子中铁周围的价电子数共有______ 个,S元素的杂化方式为______ ,该配合物离子中的 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为______ (用Ⅰ或Ⅱ表示)。
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为______ 。基态Cs原子中电子占据的能量最高的轨道是______ ,能量最低的空轨道是______ 。
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(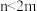 ),则可以形成大π键,表示为
),则可以形成大π键,表示为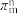 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为______ 。
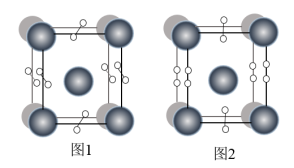
(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有______ 种。若K之间底面上的最近距离为a pm,竖直方向上为c pm,图2表示的晶体密度为______  ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
 ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(
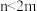 ),则可以形成大π键,表示为
),则可以形成大π键,表示为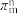 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有
 ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
您最近半年使用:0次
2021-01-03更新
|
576次组卷
|
4卷引用:八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)
八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题
2020高三·全国·专题练习
10 . (1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近半年使用:0次



