名校
解题方法
1 . 根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式:___________ ;写出基态 原子的价层电子排布图:
原子的价层电子排布图:___________ ;
(2)Mg基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了___________ 。
(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更___________ (填“强”或“弱”),从物质结构角度说明其原因:___________ 。
(1)写出基态S原子的核外电子排布式:
 原子的价层电子排布图:
原子的价层电子排布图:(2)Mg基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更
您最近一年使用:0次
名校
解题方法
2 . 氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)基态N原子的价电子轨道表示式为_______ ,基态N原子中电子占据最高能级的电子云轮廓图为_______ 形; 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是_______ ,分子中的N原子杂化方式为_______ 。
(2)B元素在周期表中的位置_______ ,B的第一电离能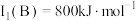 ,判断
,判断
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是_______ 。
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(1)基态N原子的价电子轨道表示式为
 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是(2)B元素在周期表中的位置
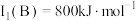 ,判断
,判断
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是
您最近一年使用:0次
3 . 回答下列问题:
(1)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。回答下列问题:
①基态Fe原子中,核外存在_______ 个运动状态不同的电子,Sm的价层电子排布式为4f 66s2, Sm3+价层电子排布式为_______ 。
②基态F原子的价电子轨道表达式为_______ 。
(2)基态Zn原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(3)Cu2+基态原子核外电子排布式为_______ 。
(4)下列状态的镁中,电离最外层一个电子所需能量最大的是_______ (填标号)。
(1)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。回答下列问题:
①基态Fe原子中,核外存在
②基态F原子的价电子轨道表达式为
(2)基态Zn原子核外占据最高能层电子的电子云轮廓图形状为
(3)Cu2+基态原子核外电子排布式为
(4)下列状态的镁中,电离最外层一个电子所需能量最大的是_______ (填标号)。
A. | B.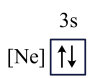 |
C.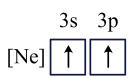 | D. |
您最近一年使用:0次
2023-02-12更新
|
305次组卷
|
2卷引用:安徽省安庆市第二中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
4 . (1)Cu的价电子排布图______ ,钾的最高能层符号______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是______ 。
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO______ MgO HF______ HCl Si______ SiC K______ Ti
(4)某金属晶体堆积方式为面心立方堆积,其配位数为______ ;一个该金属晶胞中含有______ 个该金属原子。
(5)NH3与NH4+的键角大小,NH3______ NH4+(用“>、<、=”比较),原因是______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO
(4)某金属晶体堆积方式为面心立方堆积,其配位数为
(5)NH3与NH4+的键角大小,NH3
您最近一年使用:0次
5 . (1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,违反了泡利原理的是___ ,违反了洪特规则的是___ 。
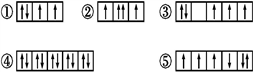
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为___ ;其最高价氧化物对应水化物的化学式是___ 。

(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
您最近一年使用:0次



