名校
解题方法
1 . 短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,X 核外电子只有 1 种运动状态,Y、W 的 2p 轨道均含有 2 个未成对电子,M 是与X 不同主族的金属元素,N 的氢氧化物具有两性,下列说法正确的是
| A.电负性:Z<Y<W |
| B.Y 的氢化物沸点不一定低于W 的氢化物 |
| C.第一电离能:M<N |
| D.N 的单质可以在高温下还原 M 的氧化物 |
您最近一年使用:0次
2023-01-06更新
|
638次组卷
|
5卷引用:天津市南开中学2022-2023学年高二上学期期末考试化学试题
2 . 根据原子结构与性质的相关知识,请回答下列问题:
(1)基态S原子电子占据最高能层的符号是______ ,最高能级的电子云轮廓图为______ 形。
(2)电负性As______ Se(填“大于”或“小于”)。
(3) 基态核外电子排布式为
基态核外电子排布式为______ ,基态磷原子的核外价电子排布图为______ 。
(4)铜元素在元素周期表中的位置是______ ,位于元素周期表的______ 区。
(5)C、N、O的第一电离能由大到小的顺序为______ 。
(6)已知 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、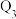 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。
(1)基态S原子电子占据最高能层的符号是
(2)电负性As
(3)
 基态核外电子排布式为
基态核外电子排布式为(4)铜元素在元素周期表中的位置是
(5)C、N、O的第一电离能由大到小的顺序为
(6)已知
 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、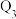 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。A.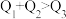 | B.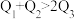 | C.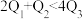 | D.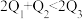 |
您最近一年使用:0次
3 . 回答下列问题:
(1)氟原子激发态的电子排布式有______ ,其中能量较高的是______ 。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的______ 区,写出该基态原子电子排布式为______ 。
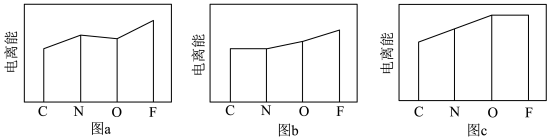
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是______ (填标号),判断的根据是______ ;第三电离能的变化图是______ (填标号)。
(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
①元素的电负性:Z______ W(填“大于”“小于”或“等于”)。
②简单离子半径:W______ Y(填“大于”“小于”或“等于”)。
③氢化物的稳定性:X______ Z(填“大于”“小于”或“等于”)。
(1)氟原子激发态的电子排布式有
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
| 0.1 mol∙L−1溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
2023-01-03更新
|
426次组卷
|
2卷引用:天津市和平区2022-2023学年高二上学期期末质量调查化学试卷
4 . 根据元素周期表中完整周期元素的性质,填写下列空白。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其基态原子的简化电子排布式为_______ ,有_______ 个未成对电子,有_______ 个能级,能量最高的能级符号为_______ 。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ ,原子中所有电子占有_______ 个轨道,核外共有_______ 个不同运动状态的电子。
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显_______ 性(填“酸”、“碱”或“中”),用离子方程式解释其原因_______ 。
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为_______ 。电解一段时间后,阴极区pH_______ (填“增大”、“减小”或“不变”)
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为
您最近一年使用:0次
解题方法
5 . 硒(Se)的原子序数为34,与氧、硫同主族,下列说法正确的是
| A.硒的最高价是+6价,所以只有一种氧化物SeO3 |
| B.H2Se的热稳定性比H2S差,还原性比H2S弱 |
| C.氧、硫、硒三种元素的电负性递减 |
| D.原子序数为33的元素是砷(As),则砷原子的第一电离能小于硒原子的第一电离能 |
您最近一年使用:0次
名校
解题方法
6 . 现有四种元素基态原子的电子排布式如下。则下列比较正确的是
① ;②
;② ;③
;③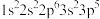 ;④
;④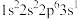
①
 ;②
;② ;③
;③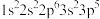 ;④
;④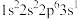
| A.第一电离能:③>①>④ | B.离子半径:④>①>② |
| C.电负性:①>②>④ | D.最高正化合价:①=③>④ |
您最近一年使用:0次
2022-09-02更新
|
699次组卷
|
7卷引用:天津市第一中学2020-2021学年高二下学期期中考试化学试题
2022高三·全国·专题练习
7 . 短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
| A.X能与多种元素形成共价键 | B.简单氢化物沸点: |
C.第一电离能: | D.电负性: |
您最近一年使用:0次
2022-07-06更新
|
9664次组卷
|
33卷引用:天津市和平区2022-2023学年高二下学期期末质量调查化学试题
天津市和平区2022-2023学年高二下学期期末质量调查化学试题天津市第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)(已下线)综合01 物质结构与性质压轴80题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)天津市第五十五中学2023-2024学年高二下学期期中学情调研化学试卷吉林省长春外国语学校2021-2022学年高二下学期期末考试化学试题吉林省长春市第五中学2022-2023学年高二上学期期末考试化学试题河南省鹤壁市高中2022-2023学年高二下学期第一次段考化学试题 天津市静海区第一中学2023-2024学年高三上学期12月月考化学试题河北省遵化市第一中学2023-2024学年高二上学期月考2化学试题吉林省长春市第二实验中学2023-2024学年高二下学期开学考试化学试题天津市和平区2023-2024学年高三下学期第一次质量调查化学试卷内蒙古呼和浩特市剑桥中学2023-2024学年高二下学期3月月考化学试题河北省石家庄市第一中学2023-2024学年高二下学期5月月考化学试题(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编(已下线)2022年辽宁省高考真题化学试题(部分试题)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)2022年辽宁高考真题化学试题(已下线)2022年辽宁省高考真题变式题(1-10)(已下线)第29讲 原子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)北京清华附中2022-2023学年高三上学期10月统练(三)化学试题(已下线)易错点13 原子结构与核外电子排布-备战2023年高考化学考试易错题(已下线)第36讲 原子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)回归教材重难点12 原子、分子和晶体结构再归纳-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2022年辽宁高考真题化学试题变式题(选择题1-5)(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)江西省宜春市宜丰中学2023-2024学年高三上学期11月期中考试化学试题湖南省浏阳景雅高级中学2024届高三下学期5月全真仿真模拟考试化学试题
名校
解题方法
8 . 氨基酸是构成人体必备蛋白质的基础,某氨基酸的结构简式如图所示。下列有关说法正确的是
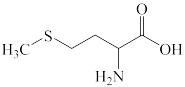

| A.第一电离能:O>N>C>H |
| B.基态氧原子的电子有8种空间运动状态 |
C.该分子中碳原子的杂化类型有sp、 和 和 |
| D.键的极性大小:N-H<O-H<F-H |
您最近一年使用:0次
2022-04-06更新
|
1558次组卷
|
7卷引用:天津市第三中学2022-2023学年高二下学期3月阶段性质量检测化学试题
名校
9 . 科学家通过观察金星的酸性云层,分析出金星存在磷化氢气体,从而推测金星可能存在生命的迹象。下列关于P元素的说法中,不正确 的是
| A.第一电离能:P<S | B.原子半径:S<P |
| C.非金属性:P<S | D.电负性:P<S |
您最近一年使用:0次
2022-03-10更新
|
818次组卷
|
7卷引用:天津市南开区2021-2022学年高二上学期期末考试化学试题
解题方法
10 . 回答下列问题:
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是____ ,氮元素原子核外有____ 个未成对电子,最外层有____ 种能量不同的电子。

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是____ (填编号)。
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是____ 。
②写出铜的基态原子的电子排布式____ 。
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有____ (填元素符号)。
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是
②写出铜的基态原子的电子排布式
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有
您最近一年使用:0次



